原子は電気的に中性の系です。これは、同じ数の陽子(正の粒子)と電子(負の粒子)があることを意味します。ただし、原子、または結合した原子のグループには、電子を失ったり獲得したりする能力があります。これが起こると、イオンが形成されたと言います。したがって、次のように概念化できます。
イオンは、電子の数とは異なる数の陽子を持つ原子、または原子のグループです。

カチオン: 1 つ以上の電子 (負の粒子) を失い、その結果、正に帯電したときのイオンの名前です。
例:
最初は中性のナトリウム原子。電子を失うとイオン、ナトリウムカチオンになります。

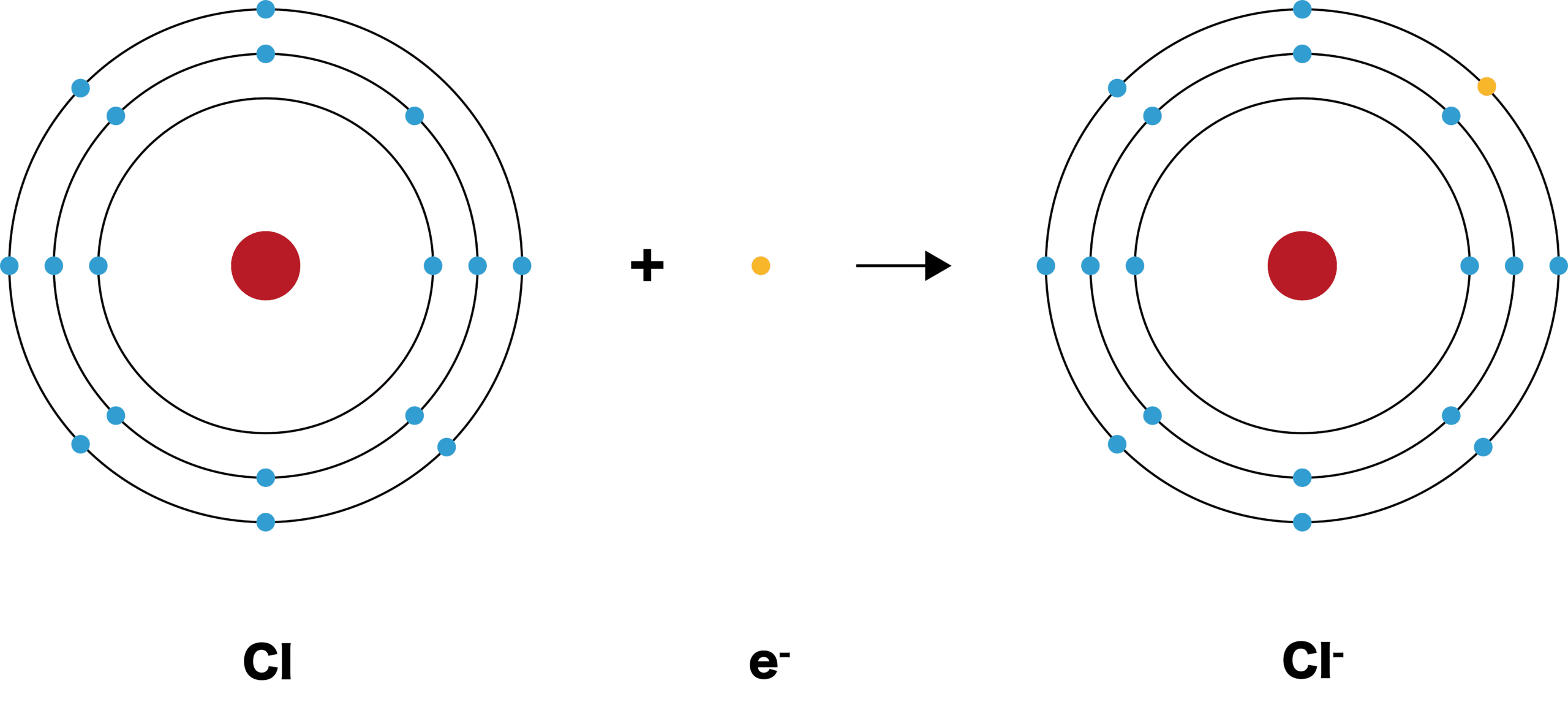
アニオン: 1 つ以上の電子を受け取ると、マイナスに帯電するイオンの名前です。
例:
中性の塩素原子。電子を受け取った後、塩化物カチオンというイオンになります。
引用されているケースは、1 つの元素だけで形成される単純なイオンの例です。他の例としては、K+、Ag + 、Ca 2+ 、Al 3+ 、Pb 4+ 、F – 、O 2- 、N 3- 、C 4-などがあります。
ただし、電子を獲得または失った化学元素の原子のグループによってイオンが形成される場合、それらは複合イオンと言われます。
複合カチオンの例:NH 4 + 、H 3 O +

複合アニオンの例: SO 4 2- 、P 2 O 7 4-
このテーマに関するビデオレッスンをぜひご覧ください。

.jpg)
