テキスト「共有結合、分子結合、または同極結合」では、共有結合は、安定を維持するために電子を獲得する傾向がある原子によって形成され、相互に電子の対を共有することが示されました。限られた決まった数の原子間でこのタイプの結合のみが発生すると、分子または分子化合物が形成されます。
分子の例としては次のようなものがあります。
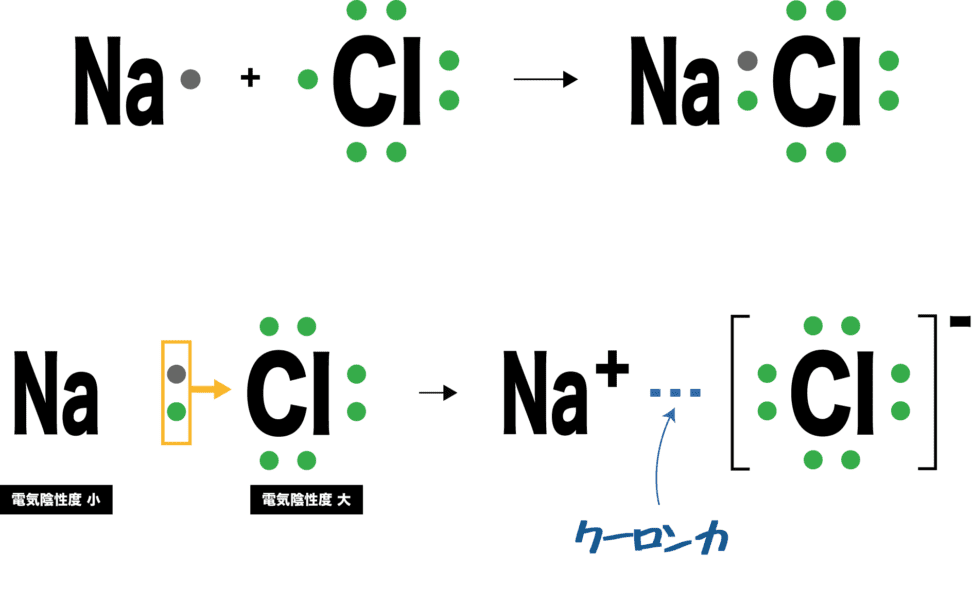
上記の例が示すように、分子化合物は室温で3 つの物理状態 (砂糖などの固体、水などの液体、二酸化炭素や窒素などの気体) で見られます。しかし、これらの化合物はイオン性化合物ほど相互に引き合う力が弱いため、ほとんどが沸点の低い気体や液体として存在します。
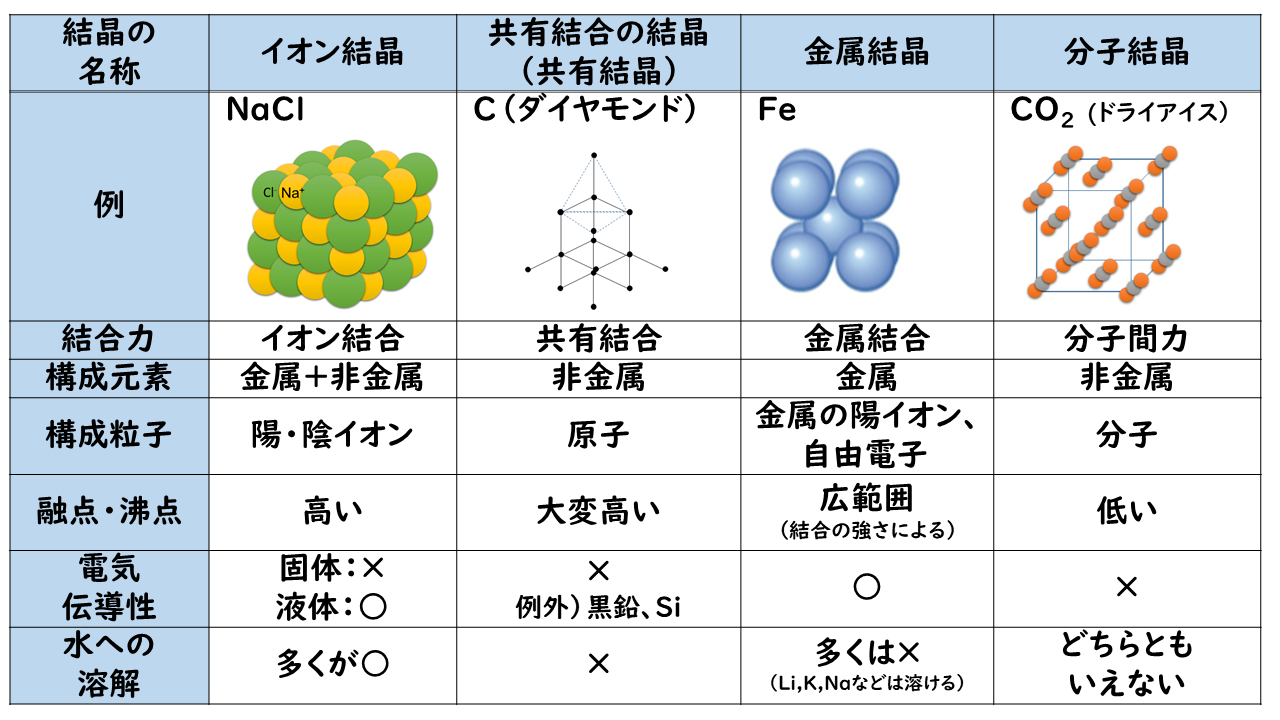
イオン性物質と比較して、共有結合性化合物の融点と沸点ははるかに低くなります。これは、分子間の引力が弱いため、分子を分離して物理的状態を変化させるために必要なエネルギーが少なくて済むためです。
分子化合物を相互に比較すると、分子間力の種類が融解温度と沸騰温度に影響を与え、次の順序で上昇することがわかります。
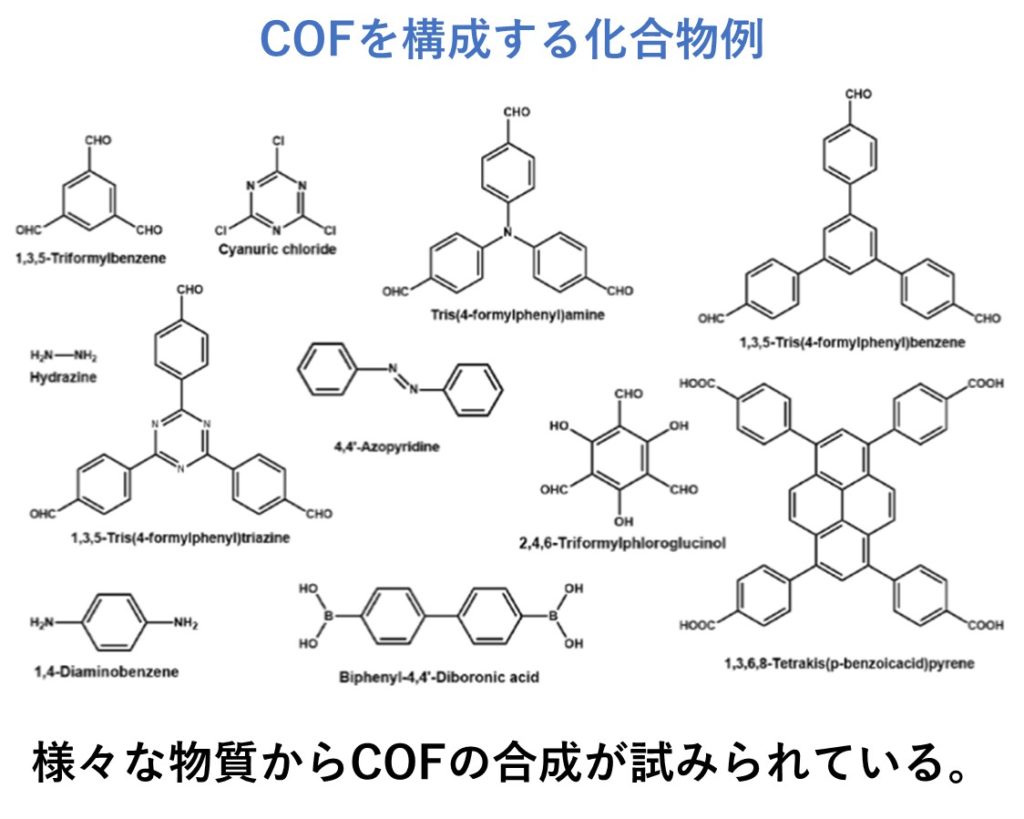
水素結合 > 永久双極子 > 誘導双極子
たとえば、水は最も強い種類の分子間力、つまり水素結合を実行し、海面での沸点は 100 °C です。塩素 (C? 2 ) は誘起双極子相互作用を起こし、沸点ははるかに低く、-33.97 °C に相当します。
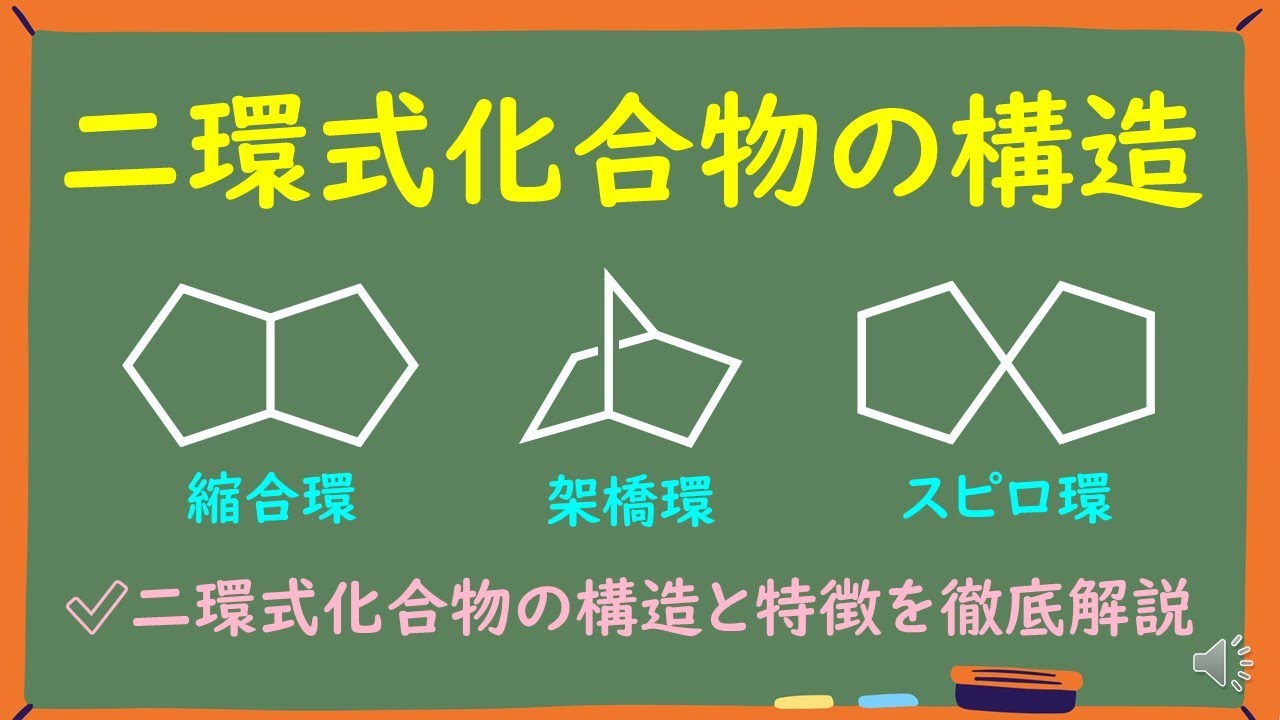
ここで、同じ種類の分子間力を生成する 2 つの化合物を比較すると、分子量が大きい方が融点と沸点が高くなります。たとえば、プロパン (C 3 H 8 ) も誘起双極子相互作用を行いますが、そのモル質量 (44 g/mol) は塩素 (71 g/mol) よりも低いため、沸点も低くなります (- 42℃)。
しかし、特定の元素の原子が電子の共有によって結合し、分子を形成せず、非常に多くの原子 (通常は不定数) を含む高分子を形成することもあります。これらは共有結合または共有結合ネットワーク化合物です。

いくつかの例は次のとおりです。
これらは通常の温度と圧力の条件下ではすべて固体であり、モル質量が非常に高い値を示すため、融点と沸点も非常に高くなります。例を挙げると、ダイヤモンドの沸点は 4,826.85 °C であり、これは昇華する温度です。
固体状態ではよく電気を伝導するグラファイトを除いて、共有結合化合物と分子化合物はどちらも電気を伝導しません。これは、電子の移動を可能にする二重結合または共役パイ (π) 結合を持つ六角形の環を形成するその構造によって起こります。さらに、炭素はsp 2混成(平坦)をとり、「巣」のように重なり合うシートを形成します。つまり、炭素は平行です。そして、異なる面の結合は弱く、面間の電子の移動、つまり電気の移動が可能になります。


.jpg)