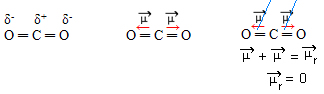極性分子とは、電気陰性度に差があり、外部電場の存在下で自らの向きを変える分子のことですが、非極性分子は、電子がすべての分子に対称的に分布しているため、電気陰性度に差がありません。 、電場の存在下ではガイドしません。
たとえば、水は極性があるため、ガラス棒を羊毛でこすってプラスに帯電させたままにし、滴り落ちる水に近づけると、ガラス棒に引き寄せられることがわかります。水分子のマイナス極はロッド上のプラス電荷に引き付けられます。
分子が極性か非極性かを調べるには、次の 2 つの要素を観察する必要があります。
- 分子内の各結合の原子間の電気陰性度の差。
- その幾何学的形状は何ですか。
単体物質(同じ化学元素の原子で構成されている) は、オゾン (O 3 ) を除いてすべて無極性です。このような分子の例としては、O 2 、H 2 、N 2 、P 4 、S 8があります。
ただし、物質が構成されている (複数の元素で構成されている) 場合は、分子が極性か非極性かを判断するために、分子の幾何学的形状のタイプを確認する必要があります。
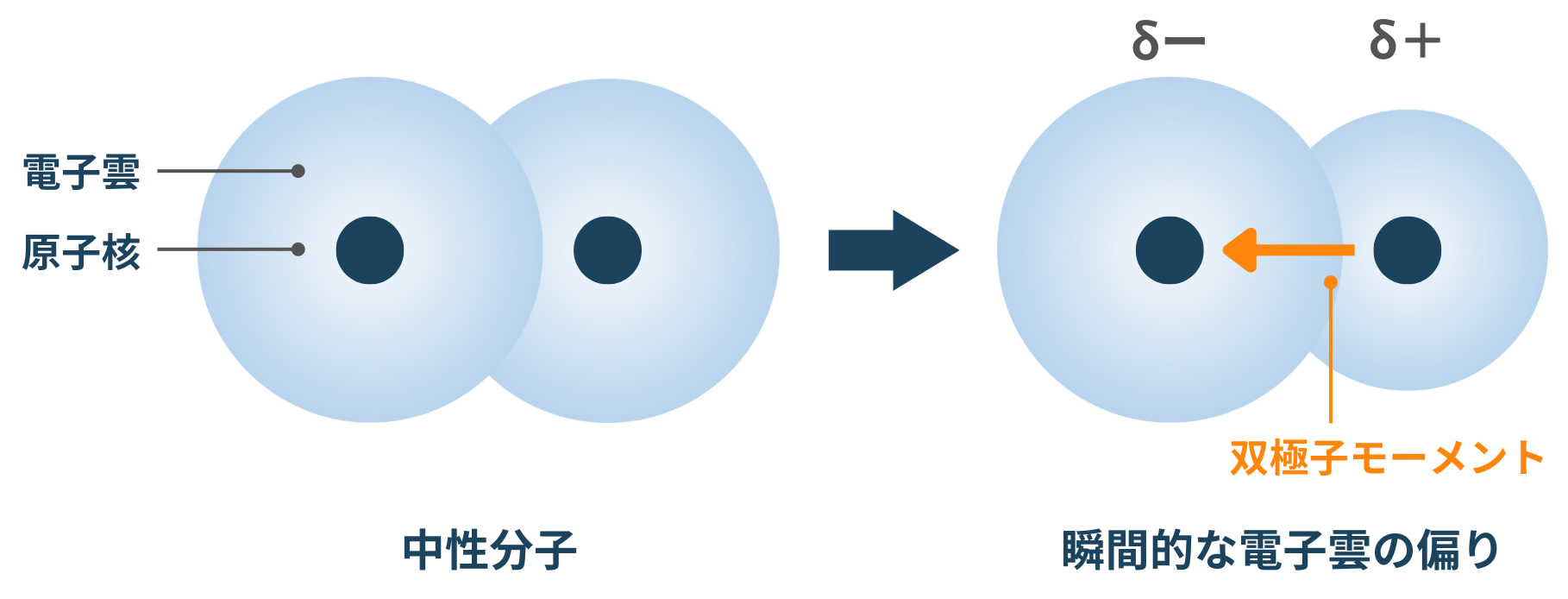
原子間の電気陰性度に差がある場合、分子内に電気双極子が現れます。電気陰性度の高い原子はより強く電子を引き寄せ、部分的に負の電荷(δ – )を持ちますが、他の元素の原子はより強く電子を引き寄せます。部分的に正の電荷 (δ + ) を持って残ります。
各極性結合のベクトルの合計は、双極子モーメントまたは合成双極子モーメントと呼ばれる結果のベクトルであり、次のように記号化されます。 。
この結果として得られる双極子モーメントは部分電荷の強さを示し、分子の極性を決定するのに役立ちます。その値がゼロに等しい場合、これは分子が極性であることを示します。ただし、値がゼロ以外の場合、それは極性分子です。
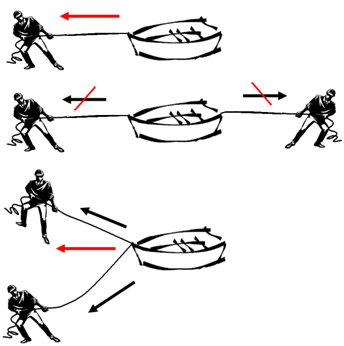
ベクトル (記号の上の矢印で表されます) は、モジュール内の値、その方向、およびその方向の決定によって特徴付けられる量です。結果として得られるベクトルの操作方法を理解するために、たとえを立ててみましょう。
人がロープを使って湖でボートを引いているところを想像してください。ボートには他に力が働いていないことを考えると、ボートは人が加えた力の方向に進みます。この方向がベクトルに相当します。しかし、ボートを引く人が 2 人いる場合、ボートの軌道は加えられた力の間の合成ベクトルによって決まります。たとえば、同じ強さで反対方向に引っ張っている場合、一方のベクトルが他方のベクトルを打ち消し、ボートが静止したままになる場合、結果のベクトルはヌル (ゼロに等しい) になります。しかし、以下の 3 番目の図に従ってボートが牽引している場合、ボートが移動する方向は、結果として得られるベクトルの方向になります。
同じ推論を使用して、結果として得られる分子の双極子モーメントを決定します。いくつかの例を参照してください。
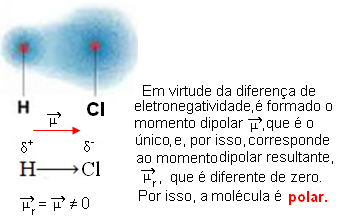
- HCℓ: 直線形状。
塩素は水素よりも電気陰性度が高いため、電子は塩素に引き寄せられ、次の電気双極子が形成されます。
- CO 2 : 線形幾何学。
酸素は炭素よりも電気陰性度が高く、電子を引き寄せて 2 つの双極子モーメントを生じます。炭素には自由電子がないため、各酸素に引き寄せられる結合内の電子は、できる限り互いに遠くなるように配置され、分子は 180 度の直線的な角度を保ちます。
双極子モーメントベクトルは同じ強度で反対方向であるため、それらは互いに打ち消し合い、結果として生じる双極子モーメントはゼロに等しくなります。したがって、分子は無極性です。
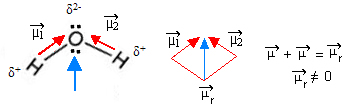
- H 2 O: 角度幾何学。
酸素は中心原子であり、最も電気陰性であり、電子対をそれ自体に引き寄せます。その電荷は負 (δ 2- ) になり、各水素の電荷は正 (δ + ) になります。酸素には 2 対の自由電子があるため、分子は 104.5 度の角度を持ちます。したがって、2 つの双極子モーメントの合計により非ゼロの双極子モーメントが得られ、このため水分子は極性になります。