このタイプの電気分解は、自然界に孤立して存在しない年間数百万トンの金属を製造するために工業的に広く使用されており、これらの金属は医薬品、食品、繊維製品、石油誘導体の製造の原料として機能します。これはイオンの電荷を中和することによって行われ、このようにして単体の物質が得られます。
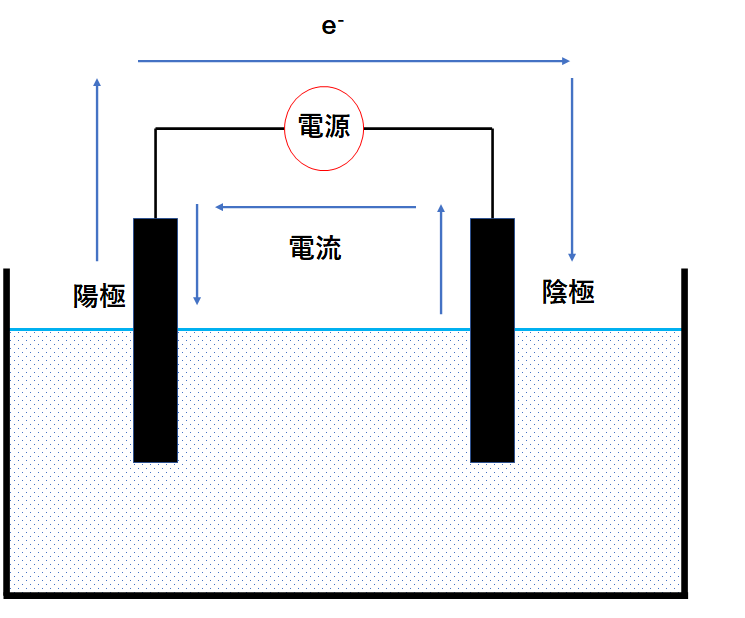
このプロセスはイオン結合の逆であるため、自発的ではありません。この場合、カチオンは与えられた電子を受け取り、アニオンは受け取った電子を与えます。これが起こるためには、発電機を通る電流であるエネルギーの供給が必要です。

火成電気分解は高温で発生します。これは、系内でイオンが自由になるためにイオン性物質が溶ける、つまり液体状態になり、通常、これらの化合物の融点が非常に高いためです。これが、このプロセスが「火成」と呼ばれる理由です。ラテン語で「ígneus」という言葉は燃える、炎症を意味するからです。

したがって、このプロセスには水が存在しません。
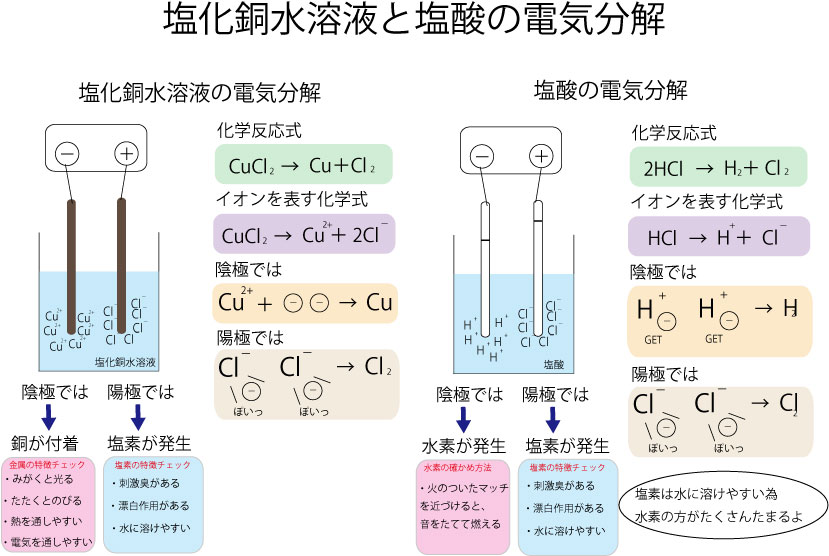
塩化ナトリウム – 食塩 (NaCl) の火成電気分解がどのように起こるかを以下で観察してください。

以下の半反応に従って、カソードでは Cl – イオンが還元され、アノードでは Na +イオンが酸化されます。
カソードでの半反応: Na ++ e- → Na 。 (2)
アノードでの半反応: 2 Cl- → Cl 2 + 2e-____
全体の反応: 2 Na + + 2 Cl- → 2 Na + Cl 2
このプロセスでは、工業にとって非常に重要な 2 つの単体物質、金属ナトリウム (Na) と塩素ガス (Cl 2 ) を得ることができることに注意してください。


