一般化学や物理化学で物質の物理状態、物理状態の変化、気体の研究などの内容を学習する際に、 「気体状態」と「蒸気状態」という用語があることにすでに気づいたかもしれません。
たとえば、水が蒸発すると言うとき、それは液体の状態から蒸気の形になったと言います。しかし、空気中に存在する酸素に言及するとき、それが蒸気であるとは言わず、むしろ気体であるか、または気体の形態であるとは言いません。
したがって、 「結局のところ、蒸気と気体の違いは何ですか?」という疑問が生じます。
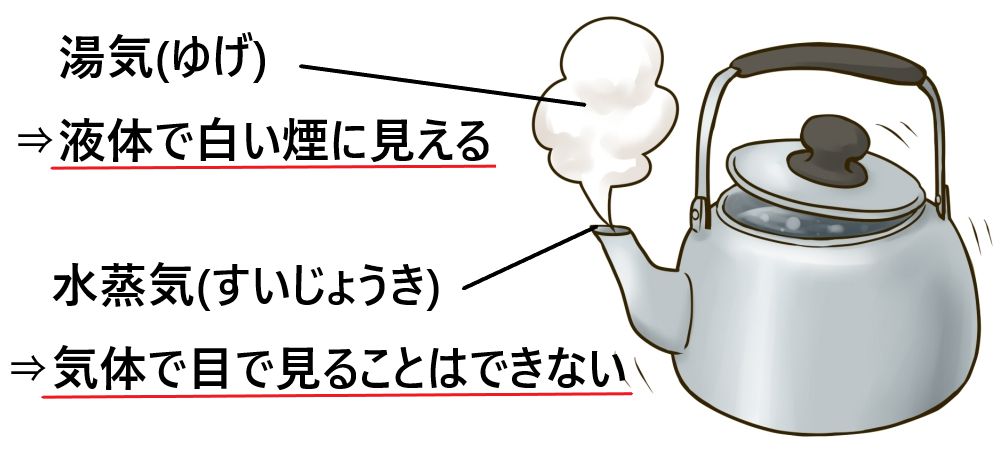
蒸気とは、システムの圧力を上げるか温度を下げると、物質が容易に液化する、つまり液体に戻る状態です。

たとえば、蒸発した水を圧縮すると液体に戻ります。あるいは、ご飯を炊くときのように、温度を下げることもできます。沸騰温度に達すると、水は蒸発します。しかし、温度が低い鍋の蓋に触れると液体に戻ります。別の例は、冷たい液体の入ったグラスやボトルの周りに形成される水滴です。これらの水滴は空気中に存在する水蒸気であり、温度が低いガラスやボトルに触れると凝縮します。

これは、蒸気が対応する液体または固体と平衡状態にあることを意味します。
気体は流体状態にあり、その状態を変化させるには、これら 2 つのプロセス (圧力の増加と温度の低下) を同時に使用する必要があります。
これにより、すべての蒸気は気体であると言えますが、すべての気体が蒸気であるわけではありません。
気体と蒸気を区別するための重要なステップは、その臨界温度を知ることです。臨界温度とは、圧力を高めるだけでは気体の状態を液体に変えることができないため、それを超える温度では物質が気体の形でのみ存在できます。

このようにして、次のようになります。
臨界温度は物質ごとに異なります。水の場合、その値は 374℃です。したがって、この温度以下では水は蒸気の状態ですが、それ以上の温度では水は気体になります。このように、あらゆる物質に言えることですが、水は蒸気状態と気体状態では性質が異なります。


