各金属は、他の金属の能力とは異なり、電子を供与する独自の能力を持っています。この反応性の違いは、たとえば鉄と金の酸化を比較するとわかります。鉄は空気中で容易に酸化し、時間の経過とともに錆びます。金はほとんど酸化しません。
金は腐食性物質に対する優れた耐性があるため、詰め物や歯のインプラントに推奨されます。唾液中に存在する物質の腐食に抵抗するためです。さらに、紀元前 1400 年に遡るファラオのミイラの石棺は金で覆われており、現在でも見ることができます。

これは、さまざまな金属の山を分析するときにも見ることができます。たとえば、同じ銅電極 (硫酸銅 (CuSO 4 ) の溶液が入った容器に浸漬された銅板) を使用した 2 つの異なるバッテリーを見てみましょう。
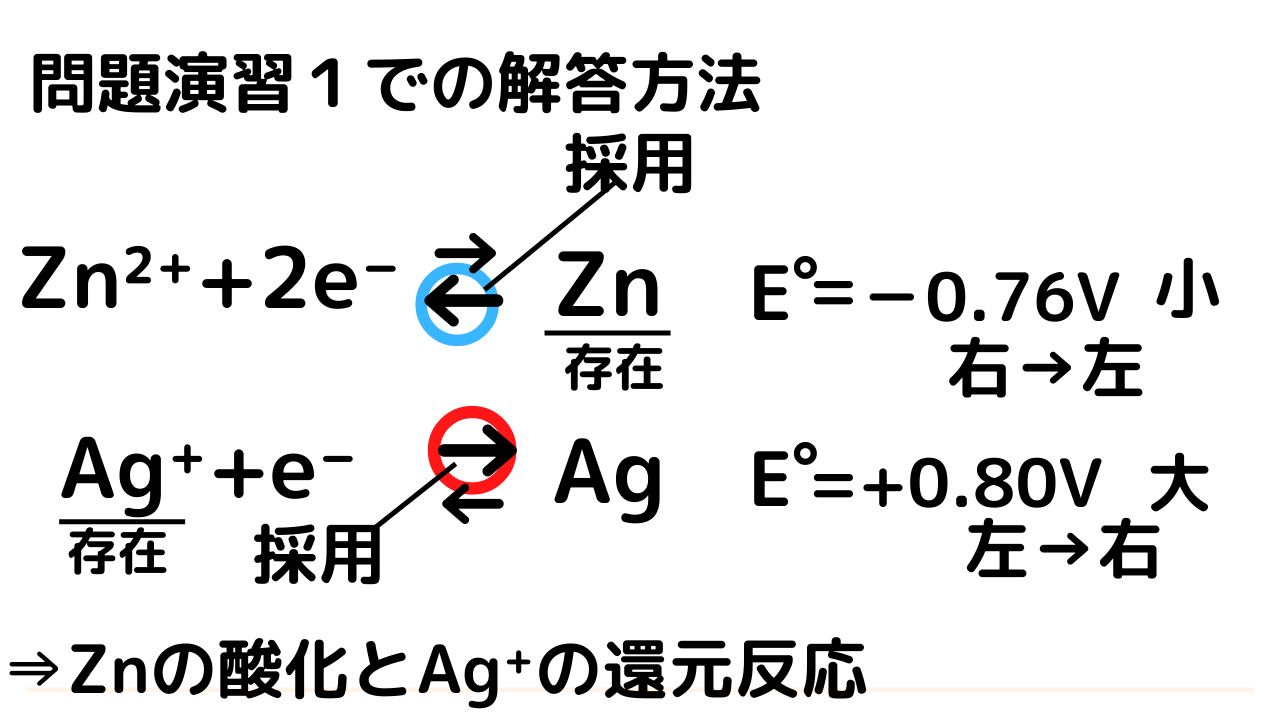
最初のセル (左側) では、亜鉛電極が酸化するためアニオン (セルの負極) として機能し、カソード (正極) である銅に電子を与えます。減らすこと。これは、このスタック内で発生する半反応と、以下に示す全体的な反応によって示されます。
アノード半反応: Zn (s) → Zn 2+ (aq) + 2 e-
カソード半反応: Cu 2+ (aq) + 2e- →Cu (s) ____________
全体的な電池反応: Zn (s) + Cu 2+ ( aq) → Zn 2+ (aq) + Cu (s)
2 番目のケースでは、銅が銀電極に電子を与えるため、銅が陽極として機能します。したがって、銀は電子を受け取る陰極になります。
アノード半反応: Cu (s) → Cu 2+ (aq) + 2e-
カソード半反応: 2 Ag + (aq) + 2e- → Ag (s) ______
全体的な電池反応: Cu (s) + 2Ag + (aq) → Cu 2+ (aq) + Ag (s)
これは、亜鉛が銅や銀と比較して最も酸化しやすいことを理解するのに役立ちます。銀は最も減らしやすいです。したがって、これら 3 つの元素の還元電位 (E red )*または標準還元電位 (E 0 red ) は、次の昇順に従います。
したがって、細胞内で特定の金属が酸化するかどうか、またはそのイオンが還元されるかどうかを知りたい場合は、まずその細胞内に他のどの金属が存在するかを確認する必要があります。
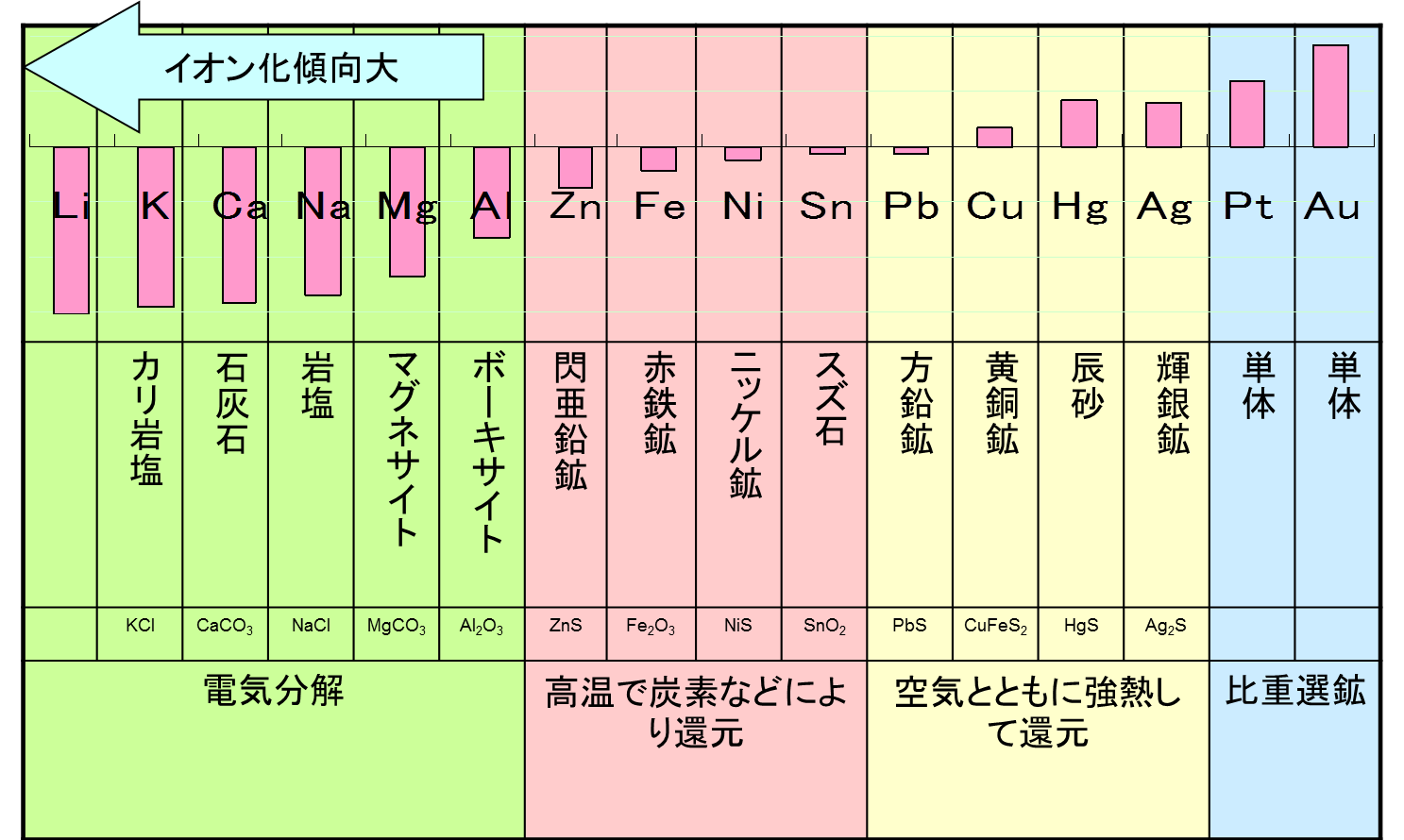
還元電位は酸化電位と同じ値ですが、符号が反対になります。以下に、いくつかの金属の還元電位を示す表を示します。
*IUPAC (国際純粋応用化学連合) は、酸化電位ではなく、標準の還元電位で作業することが望ましいとアドバイスしています。
このテーマに関するビデオレッスンをぜひご覧ください。




.jpg)