エントロピーは、系内の原子および分子の無秩序の程度に関連する物理量であり、粒子 (原子および分子) が取り得る可能な配置の数を示します。

熱損失が生じるプロセスでは、システムの秩序が生じ、その結果、エントロピーが減少します。熱の増加があるプロセスでは、システムの無秩序が生じ、その結果、エントロピーが増加します。
エントロピーについてのまとめ
- エントロピーは、システム内の原子や分子の無秩序の程度に関連する物理量であり、そのシステム内で原子や分子がどのように配列されているかを示します。
- エントロピーは、保存則に従わない、自発的、自然、拡張的なプロセスとして特徴付けることができます。
- エントロピーの変化は、正、負、またはゼロになります。
- エントロピーの変化は、熱量と温度の変化に依存します。
- 一定温度でのプロセスにおけるエントロピーの変化は、熱量を温度で割った値を変化させることで計算できます。
- 熱機関の効率はエントロピー公式を使用して求めることができます。
- エンタルピーは、一定の大気圧下での化学反応における熱変化を扱います。
エントロピーとは何ですか?
エントロピーは、気体の初期状態と最終状態のみに依存する状態関数であり、システムがある状態から別の状態に移行する方法には依存しません。エントロピーという命名法は、「変化、変換」を意味するギリシャ語の「 εντροπία 」に由来しており、物理学者で数学者のルドルフ・クラウジウス (1822-1888) によって初めて導入されました。
統計物理学の観点から、エントロピーは、系の原子と分子が配置される可能性のある方法の総量として定義されます。この統計的解釈は、物理学者で数学者のジェームズ・マクスウェル (1831-1879) による気体の運動理論に関する研究に基づいて、物理学者のルートウィング・ボルツマン (1844-1906) と科学者のジョシアン・ギブス (1839-1903) によって定式化され、貢献しました。物理学、統計力学の新しい分野の開発へ。

エントロピーの例
- 氷が溶けると、分子はより秩序だった状態から無秩序な状態になり、エントロピーが増加します。
- 水を凍らせると、分子はより無秩序な形態から秩序ある形態に変化し、エントロピーが減少します。
- 観測証拠を通じて、宇宙が膨張しており、その結果、エントロピーが増大していることがわかっています。
- 香水、アルコール、アセトンのボトルを開けると、その分子は分散し、組織化された状態から無秩序な状態になります。

エントロピーの種類
エントロピーの変化は、正、負、またはゼロになります。
- 正のエントロピー変動: システムの無秩序が増大し、自然界で自然発生的に発生していることを示します。
- 負のエントロピー変動: システムの無秩序が減少し、自然界では自然発生的に発生しないため、それが発生するにはシステムにエネルギーを転送する必要があることを示します。
- ゼロエントロピー変化:あらゆる断熱過程 (熱交換が存在しない過程) について、システムが絶対ゼロに達し、すべての原子の動きが停止したことを示します。これは、理論的な過程である完全な極低温の状態です。自然界では発生しません。
エントロピーの特徴
エントロピーにはいくつかの特有の特性があります。
- エントロピーは自発的、自然かつ拡大するプロセスです。
- 熱的に隔離されたシステムのエントロピーは、不可逆的なプロセスで常に増加します。
- 熱的に隔離されたシステムのエントロピーは、可逆プロセスでは一定のままです。
- 断熱されたシステムのエントロピーは決して減少しません。
- エントロピーは、可逆的な断熱過程では変化しません。
- エントロピーの変化は、熱の形でシステムに伝達されるエネルギー、またはプロセス中にシステムから除去されるエネルギーに比例し、温度に反比例します。
- エントロピーは、エネルギーや電荷のような保存則に従いません。

エントロピーの公式
等温プロセス (一定温度における) のエントロピーは、次の式を使用して計算できます。
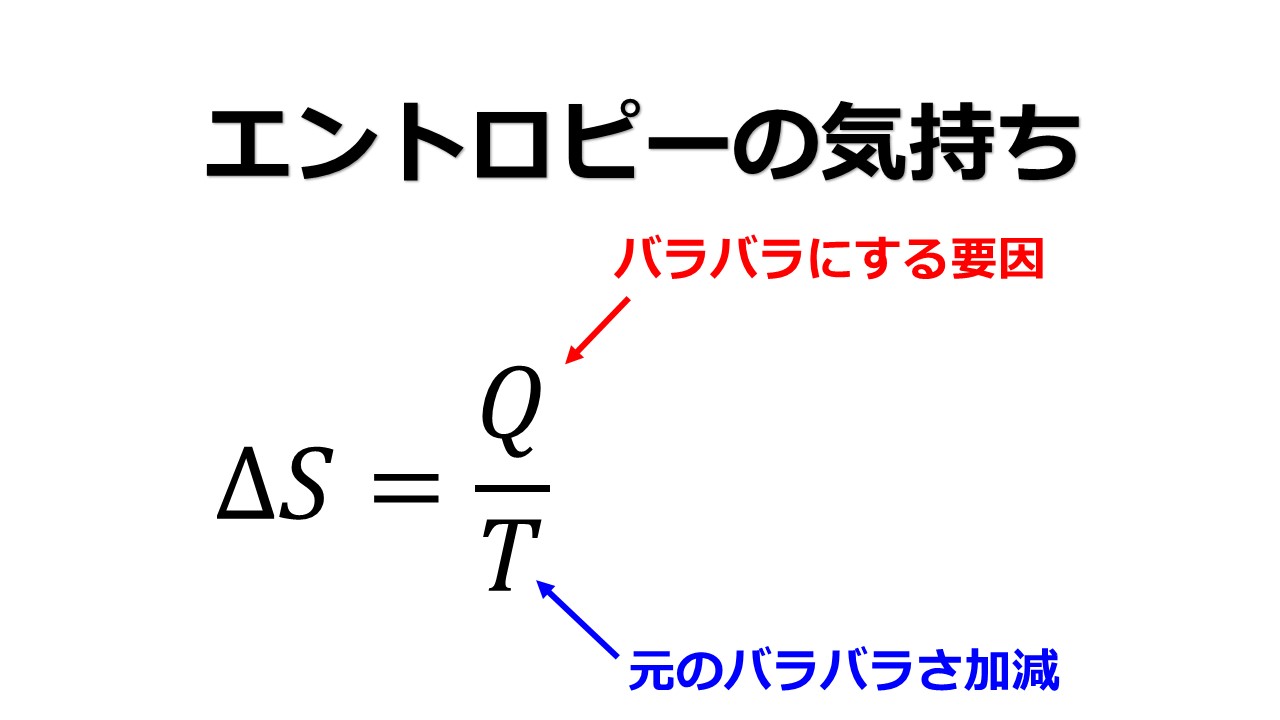
\(ΔS=\frac{ΔQ}{T}\)
- ΔS → エントロピー変化、 [J/K]で測定。
- ΔQ → 熱の形でシステムに伝達されるエネルギー、またはプロセス中にシステムから除去されるエネルギー。ジュール[J]で測定されます。
- T → ケルビン[K]で測定される温度。
統計的な観点から、エントロピーは次の式を使用して計算されます。
\(S=k\cdot ln\ W\)
- S → ボルツマン エントロピー、 [J/K]で測定。
- k → ボルツマン定数、 1.4 ∙ 10 -23 J/Kに相当します。
- W → システムで可能なマイクロステートの数。

エントロピー、熱力学、熱機関の関係
熱力学第 2 法則は、熱機関とカルノー サイクルを扱いますが、エントロピーの研究から自然に得られます。次のような方法で、エントロピーの公式が得られます。 熱平衡における可逆過程で熱に変換されたエネルギー量を決定できる式を得ることができます。
\(\frac{\left|Q_F\right|}{\left|Q_Q\right|}=\frac{T_F}{T_Q}\)
- \(\left|Q_F\right| \) → ジュール [ J ] で測定される冷熱源の熱モジュール。
- \(\left|Q_Q\right| \) → ジュール [ J ] で測定される熱源の熱モジュール。
- TF → ケルビン [ K ] で測定される冷熱源の温度。
- TQ → ケルビン [ K ] で測定される熱源の温度。
この式を使用すると、冷熱源と熱源の温度、または冷熱源と熱源の熱の観点から熱機械の効率を計算することができます。
サイクル中に常に熱損失が発生するため、熱機関の効率が 100% であることはなく、プロセスのエントロピーの変化は正になります。これを念頭に置いて、物理学者、数学者、機械技術者のサディ カルノー (1796 ~ 1832) は、熱機関から最大効率を得る理想的な熱力学サイクルであるカルノー サイクルを定式化しました。このサイクルでは、エントロピー変化はゼロでなければなりません。

エンタルピーとエントロピー
エンタルピーとエントロピーは別個の状態関数です。エントロピーはシステム内の無秩序のレベルを表しますが、エンタルピーは一定の大気圧の条件下での化学反応における熱変化を表します。エンタルピー変化が正の場合、システムは周囲から熱を受け取り (吸熱プロセス)、エンタルピー変化が負の場合、システムは周囲に熱を失います (発熱プロセス)。
