の計算は、多くの高校生にとって常に大きな難関です。このテーマについて学生が理解しやすいように、いくつかのヒントをまとめました。
ここで紹介するヒントは、電気分解が火成電気分解 (材料が溶けているとき) か水電気分解 (材料が水に溶解しているとき) であるかどうかを考慮していませんが、一般に次のことを目的としています。
- 電気分解を実行するために必要な電荷の決定;
- プロセス中に堆積する金属の質量の計算。
- 電気分解に関与する金属のNOX の測定。
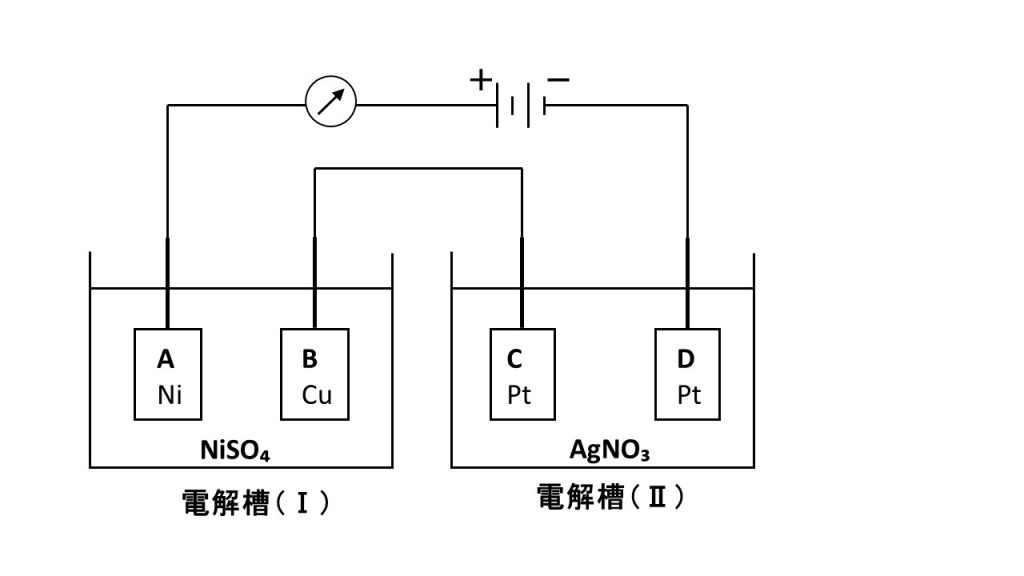
第 1 のヒント: よく使用される数式
電気分解を伴う計算で最もよく使用される式は次のとおりです。
使用される負荷を計算するには:
Q=それ
Q = 負荷
i = 現在
t = 時間
使用される金属のグラム当量を計算するには、次のようになります。
E = M
k
E = グラム当量
M = 分子量 (M)
k = 関与する電子の数 (NOX)
m = QE
96500
m = 電気分解で堆積する質量
注: 1 ファラデーは 96500 ℃ に等しいため、次のようになります。
m = QE
F
F = ファラデー
グラムに相当する式に代入すると、次のようになります。
m = i.tE
96500
注:電気分解を直列に行う場合の式:
m1 = m2 = m3
E1E2E3
インデックス 1、2、および 3 は、電気分解中に析出する各金属を表します。
ヒント 2: 原子モルが関与する電気分解に必要な電荷
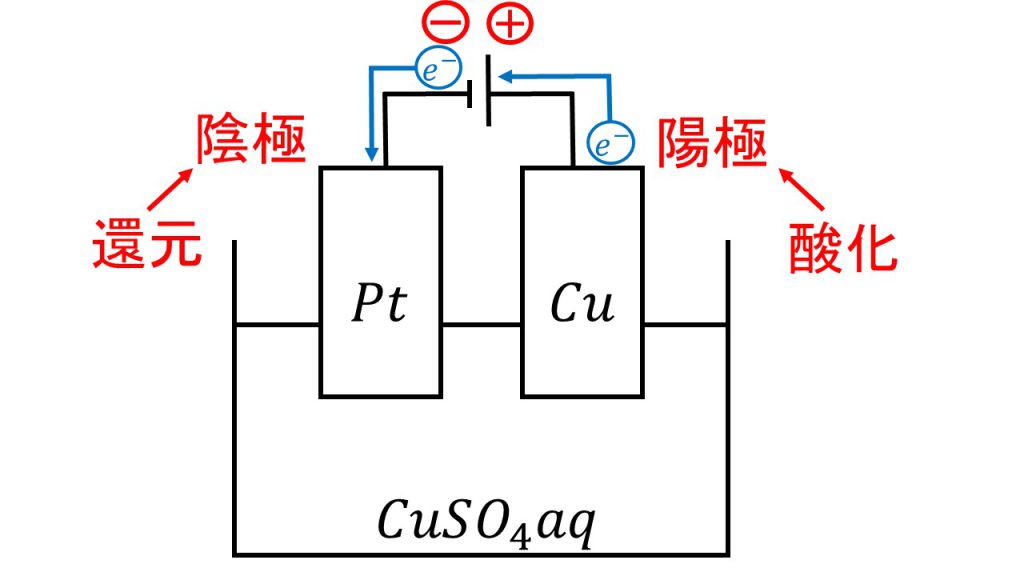
これは、演習で堆積されたモル数のみが提供され、この堆積に必要な料金が疑問視される場合に発生します。
式を使用する必要はありません。単純な 3 の法則を使用して電子のモル数を求め、電子のモル数に関連する電荷を求めます。
注記。 : 1 ファラデーは常に 1 モルの電子を表します。
例を参照してください。
例: (UFAL) 硫酸銅 I (Cu2SO4) の溶液の電気分解で 2 mol の銅原子が析出するのに必要な電荷はいくらですか: データ: 1 ファラデーは 1 mol の電荷量に相当します。電子の。
1st)電子のモル数を求める:
銅の電荷は (名前に示されているように) +1 であり、式には 2 つの原子があるため、1 モルの銅原子は 2 モルの電子に等しくなります。
1モルの銅原子 → 2モルの電子
銅原子 2 モル → x
1.x = 2.2
x = 4 モルの電子
2)電荷を見つける:
1ファラデー → 1モルの電子
y → 4 モルの電子
1.y =1.4
y = 4ファラデー
ヒント 3: 時間と電流から堆積した質量を求める
- 運動によって電気分解に使用される時間と電流が得られると発生します。
- 時間は常に秒単位で使用する必要があります。
- 金属のグラム当量を決定することが常に重要です。
例: (UFPB) 10 A の電流が AgNO3 を 16 分 5 秒間通過したときに析出する金属の質量はいくらですか? (Ag の MA = 108 g/mol)
1 番目)鉄のモル質量を鉄の +1 電荷 (常に固定) で割ることによってグラム当量を決定します。
E = M
k

E = 108
1
E = 108
2 番目)時間を秒に変更します (60 を掛けるだけです)。
t = 16.60 +5
t = 960 + 5
t = 965 秒
3)式ではグラムに相当する電流と時間を使用します。
m = itE
96500
m = 10,965,108
96500
m = 1042200
96500
m = 10.8g
4 番目のヒント: 使用する物質と電荷の式に基づく堆積質量の計算
- それは、運動が物質の配合と使用された負荷を提供するときに起こります。
- 物質の式を使用して、使用された金属の NOX を求めます (k)。
- 電荷がファラデーで与えられる場合、次の式を使用します。
m = QE
F
注記。 : F は常に 1 であることを思い出してください。
例: (UFRGS-RS) 0.1 ファラデーの電荷が通過するときに、FeCl 3水溶液を含む電解槽の陰極に析出する鉄の質量はいくらですか?データ: Fe = 55.8
1st)金属の NOX を決定する
イオン性化合物があるため、式中の 1 である Fe と 3 である Cl の量は、それらの電荷の交差から生じます。したがって、FeのNOX(k)は+3となります。
2)ファラデー単位の電荷 (Q) (0.1)、鉄のモル質量 (M)、および ok を式で使用します。
m = QE
F
m = QM
FK

m = 0.1.55.8
1.3
m = 5.58
3
m = 1.86g
5 番目のヒント: 金属の堆積質量から NOX を計算する
これは、運動によって電気分解中に析出した金属の塊と、プロセス中に使用された電荷が提供されるときに発生します。
例: (ITA-SP) 原子量 119 の金属 2.975g の電解析出には 9650 ℃が必要です。この金属の NOX は何ですか?
1)演習では質量、電荷、原子質量が得られるので、次の式を使用するだけです。
m = QE
96500
注: E は約 OK の M であるため、次のようになります。
m = QM
96500.k
2.975 = 9650.119
96500.k
2,975.96500.k = 9650.119
287087.5.k = 1148350
k = 1148350
287087.5
k = 4
6 番目のヒント: 電流と時間に基づいた一連の電気分解で析出する質量の計算。
- これは、演習によって電流と時間が提供され、直列に接続された少なくとも 2 つの槽で電気分解が行われたことが通知されるときに発生します。
- 最初に、プロセスに関与する各金属のグラム当量を決定し、次にそのうちの 1 つを選択し、次の式を使用してその質量を決定するのは興味深いことです。
m = itE
96500
- 最後に、直列電解計算式を使用して、他の金属の質量を決定します。
m1 = m2 = m3
E1E2E3
例: (Unimontes) 直列に接続された 3 つの電解槽に 4 A の電流を 40 分 12 秒間流して、図に従って析出した金属の質量を計算します。データ: Cu = 63.5 u;銀 = 108 単位; Fe = 56u。
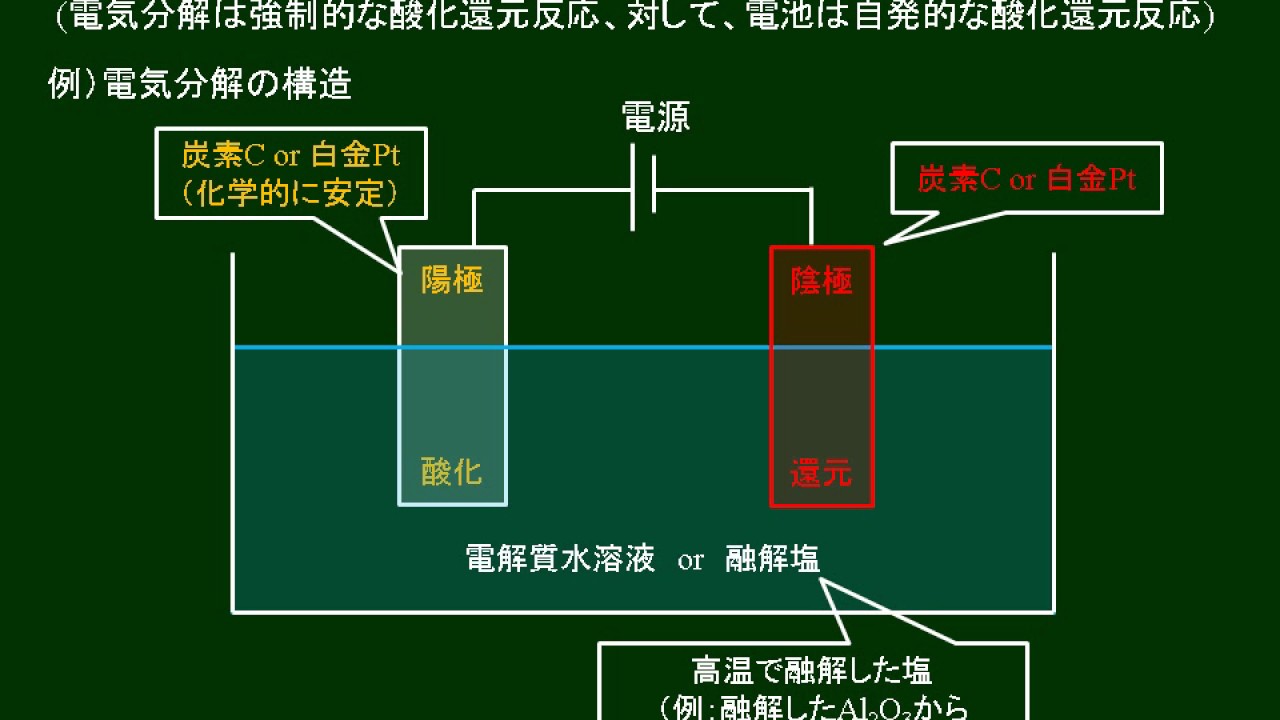
1st)モル質量を電荷で割ることにより、各金属のグラム当量を決定します。
- 銅用
E Cu = M Cu
kCu
そしてCu = 63.5
2
そしてCu = 31.75
- シルバーの場合
E Ag = M Ag
kAg
そしてAg = 108
1
そしてAg = 108
- 鉄用
E Fe = M Fe
k Fe
Fe = 55.8
3
Fe = 18.67
2番目)時間を分から秒に変換します
t = 40.60 + 12
t = 2400 + 12
t = 2412秒
3)銅、銀、鉄のグラム当量、時間、電流を使用して質量を決定します。
銅の場合:
m Cu = itE
96500
m Cu = 4.2412.31.75
96500
mCu = 306324
96500

mCu = 3.17g
シルバーの場合:
mCu = mAg
EcuEAg
3.17 = mAg
31.75 108
31.75.m Ag = 3.17.108
31.75.m Ag = 342.36
mAg = 342.36
31.75
mAg = 10.78g
鉄の場合:
m Cu = m Fe
そして、 cuとfe
3.17 = mFe
31.75 18.67
31.75.m Fe = 3.17。 18.67
31.75.m Fe = 59.1839
m Fe = 59.1839
31.75
m Fe = 1.86 g
この主題に関連するビデオ レッスンをぜひご覧ください。

.jpg)