500 mL の水に 5.0 g の塩 (NaCl) が含まれており、よく混合した後、溶液の体積が 500 mL のままであることに気づいたとしましょう。この実験から、次のデータを見つけることができました。
溶質の質量 (m 1 ) = 5.0 g

溶媒容量 (V 2 )= 500 mL
溶液量 (V) = 500.0 mL
添字 1 は溶質を指すのに使用され、添字 2 は溶媒を指すのに使用され、溶液を指す場合は添字を使用することに注意してください。
同じ量の水に溶かした塩をさらに加えると、溶液はより濃縮されると言えます。逆もまた真です。つまり、同じ体積の溶液により少ない質量の塩を溶解した場合、濃度は低くなります。
したがって、化学溶液の一般的な濃度 (C) または質量濃度は、溶質の質量 (m 1 ) と溶液の体積 (V) の間に存在する関係であると結論付けることができます。
次の数式を使用して一般的な濃度を計算できます。
この式を使用して、冒頭で述べた溶液の濃度を調べてみましょう。ただし、まず、国際単位系 (SI) で使用される単位を確認してください。
m 1 = グラム (g)
V = リットル (L)
C = g/L
体積単位はリットルであることに注意してください。したがって、mL (ミリリットル) 単位の溶液の体積をリットル (L) に変換する必要があります。
1L ———– 1000mL
× ———– 500mL
x = 0.5L
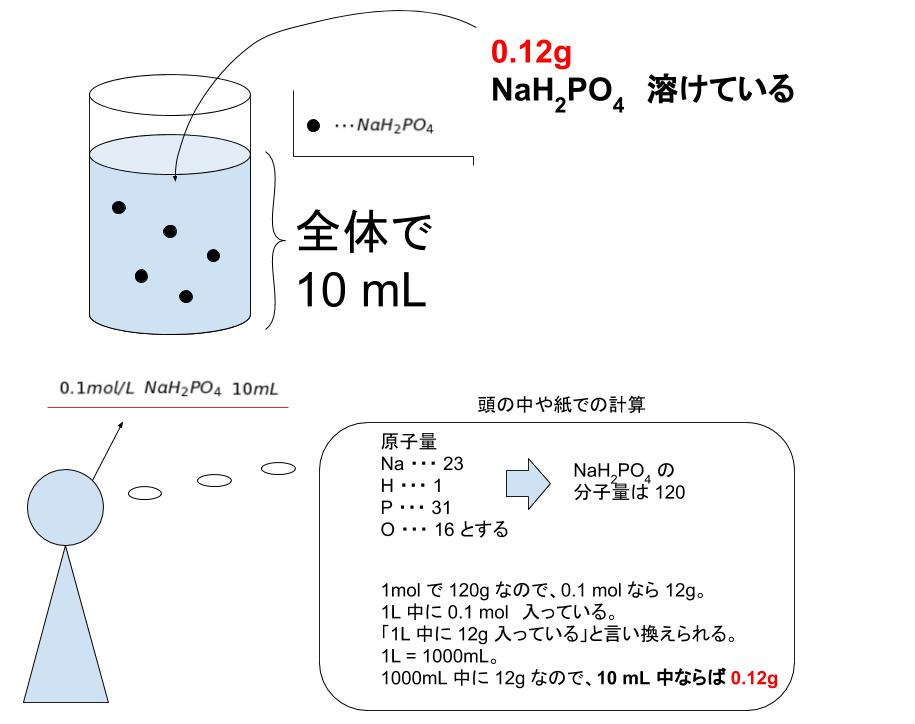
このデータを式に代入できます。
C = m1
v
C = _ 5.0 g
0.5L
C = 10 g/L
これは、溶液1リットル中に10gの塩が含まれていることを意味します。
一般濃度の SI 単位は g/L です。ただし、この量は、溶質の質量と溶液の体積の関係を示す他の単位 (g/mL、g/m 3 、mg/L、kg/mL など) を使用して表すこともできます。
再び調製した NaCl 溶液に戻り、それを 3 つのアリコート、つまりそれぞれ 0.1 L、0.3 L、0.4 L を含む 3 つの異なる溶液サンプルに分割したとします。溶解した NaCl の質量は、これらのそれぞれのレートは、次の 3 つの単純なルールを使用して計算されます。
第 1 レート: 第 2 レート: 第 3 レート:
0.5L —– 5.0g 0.5L —– 5.0g 0.5L —– 5.0g
0.1 L —– y 0.3 L —– w 0.4 L —– z
y = 1.0 g w = 3.0 g z = 4.0 g
ここで、これらの各アリコートについて共通濃度を再度計算するとどうなるかを見てみましょう。
第 1 レート: 第 2 レート: 第 3 レート:
C = _ 1.0 g C = _ 3.0 g C = _ 4.0 g
0.1L 0.3L 0.4L
C = 10 g/L C = 10 g/L C = 10 g/L
気づきましたか?濃度は初期濃度と同じです。溶質または溶媒の量を変更しない場合、溶液のどのアリコートでも濃度は同じになります。これは、体積が小さくなると、それに比例して溶解溶質の質量も小さくなるために起こります。したがって、質量濃度は溶液の量に依存しません。
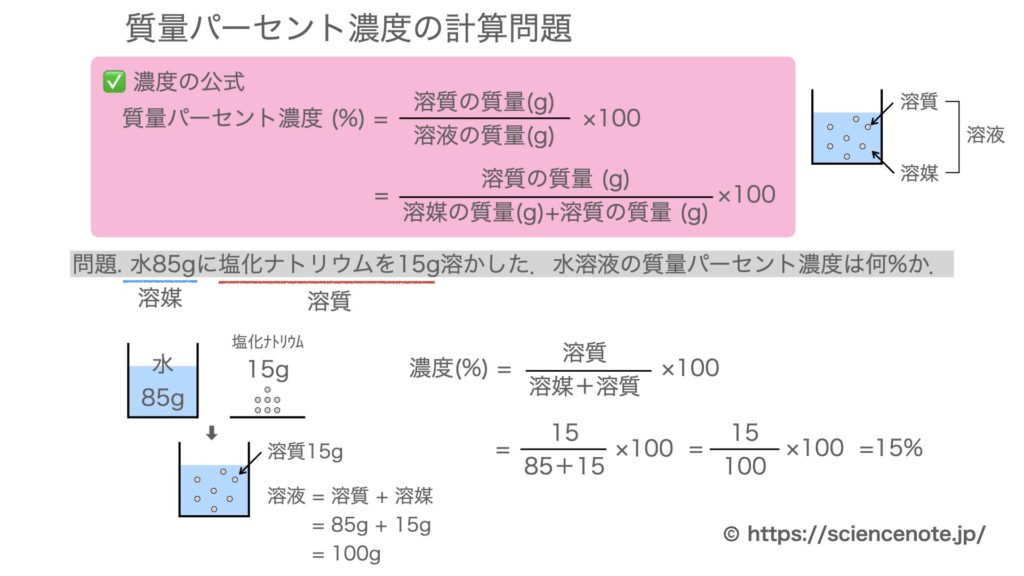
一般的な濃度は日常生活で広く使用されています。たとえば、国家交通法は以前、血中アルコール濃度が 0.6 g/L 以上の者に対する罰則を規定していました。現在、飲酒検査で血液中にアルコールが検出された場合、法律で定められた罰則が科せられる可能性があります。血中のアルコール濃度が人にどのような影響を与えるか、また飲酒検知器がこれをどのように検出するかを理解するには、 「飲酒検知器の化学原理」というテキストを参照してください。
さらに、液体である多くの食品、医薬品、洗浄・衛生材料の栄養表示には、溶解成分の濃度が表示されています。たとえば、下のラベルには、100 mL の食品には 9.0 g の炭水化物が含まれていると記載されています。
この食品の炭水化物濃度を確認してください。
C = m1
v
C= _9.0g
0.1L
C = 90g/L
これは、対象となる食品 1 リットルあたり、90 グラムの炭水化物が摂取されることを意味します。
関連するビデオレッスン:




