分子を形成する共有結合は、水素原子、非金属、半金属間の電子対の共有によって行われます。たった 2 つの原子で構成されている非常に単純な分子があります。しかし、いくつかの原子間の結合によって形成される分子もあります。
それぞれの共有ペアは化学結合に対応します。共有結合の数、および特定の分子を構成する原子の数と種類を示すために、化学式による表現が使用されます。

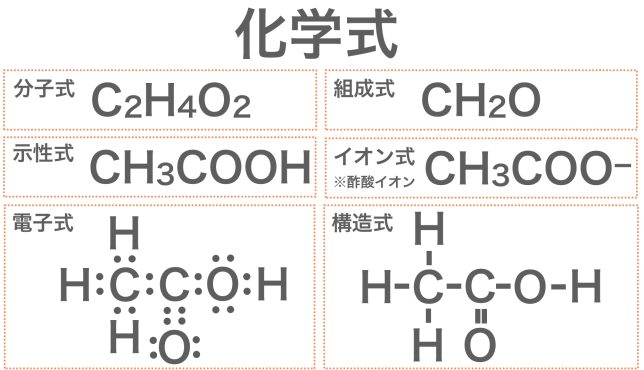
共有結合性化合物を表すために使用される主な化学式は、分子式、電子式またはルイス式、平面構造式の 3 つです。それぞれを参照してください。
- 分子式: 3 つの中で最も単純であり、簡単に言うと、どの化学元素がその記号によって関係しており、各元素の原子の数がインデックス (記号の右側の下付き数字) によって分子を形成しているかを示します。元素記号)。
たとえば、水分子は 2 つの水素原子と 1 つの酸素原子の間の 2 つの結合によって形成されます。したがって、その分子式はH 2 Oで与えられます。
共有結合化合物の分子式と、このテキストで後ほど説明する他の化学式を決定する方法を知るには、まず元素が属する周期表内の族またはグループを知る必要があります。これに基づいて、価電子殻 (最後の電子殻) に電子がいくつあるか、したがって接続の数を知る必要があるかを知ることができます。
オクテット理論では、化学元素が安定するには 8 個の電子、または 2 個の電子 (水素など電子殻を 1 つしか持たない原子の場合) が必要であると言われています。
理解していただくために、もう一度水の場合を考えてみましょう。酸素は 16 または 6 A ファミリーに属します。これは、酸素の最後の殻に 6 つの電子があり、安定するにはさらに 2 つの電子が必要であることを意味します。一方、水素は 1 または 1 A ファミリーに属し、唯一の電子殻に電子を 1 つだけ持ち、安定するにはさらに 1 つの電子を必要とします。
したがって、一対の電子を共有して水素と酸素を結合すると、水素は安定しますが、酸素は安定しません。原子価殻には電子が 7 個しかなく、さらに 1 個必要になります。このようにして、さらにもう 1 つの水素が結合します。これが、水分子が 2 つの水素原子と 1 つの酸素原子を持っている理由です。
これに基づいて、他の公式を見てください。
- 電子式またはルイス式:この式は、アメリカの化学者ギルバート N. ルイス (1875-1946) によって提案されたことからその名前が付けられました。このタイプの式は、どの元素が含まれるか、関与する原子の数を示すだけでなく、各原子の価電子殻内の電子と電子対による結合の形成も示すため、興味深いものです。
各電子はドットで表され、価電子殻電子は要素の周囲に表されます。共有される電子の各対は化学結合であり、電子は結合された原子の各対に共通する電子圏の領域に属し、次のように表されます。
たとえば、炭素は 14 または 4 A ファミリーに属するため、最後の殻に 4 つの電子があり、安定するにはさらに 4 つの電子が必要です。すでに述べたように、酸素は 16 または 6 A 族に属し、最後の殻に 6 つの電子を持ち、安定するにはさらに 2 つの電子が必要です。したがって、次のようになります。
この化合物の分子式は CO 2です。
- フラット構造式またはクーパー構造式:元素間の結合を示し、 2 つの原子間で共有される各電子対はダッシュ (?) で表されます。
2 つの原子は、1 対の電子、2 対の電子、最大 3 対の電子を共有できます。表現は、以下に示すモデルに従って行われます。
上の例では、二重結合が 2 つあります。
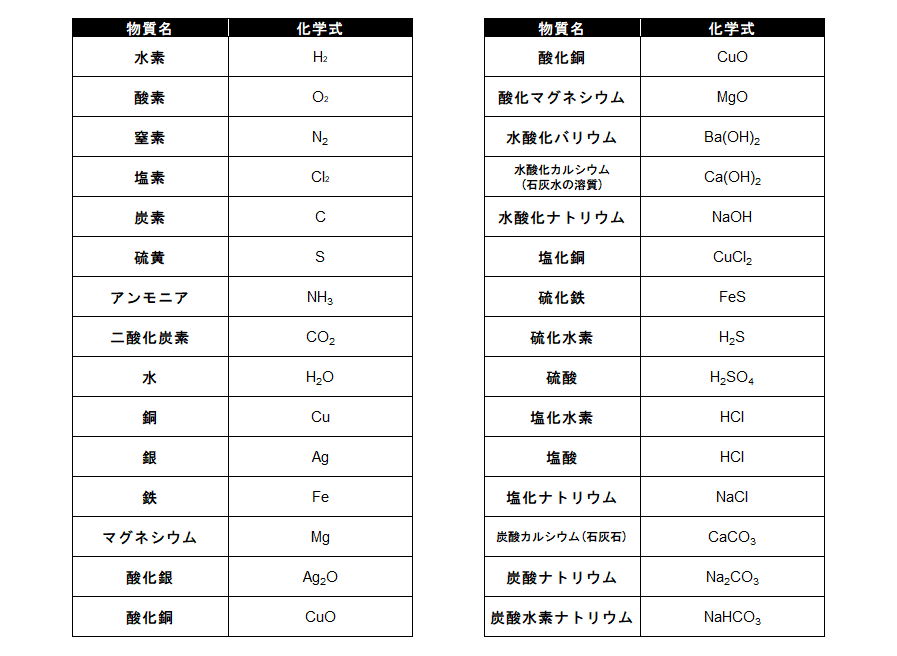
その他の例については、以下の表を参照してください。

関連するビデオレッスン:



