酸化還元反応とは何かということは「酸化還元」というテキストで詳しく説明されていますが、簡単に言うと酸化と還元が同時に起こるのが特徴です。
しかし、反応に直面した場合、それが酸化還元であるかどうかを識別できるようにするにはどのような手順が必要でしょうか?
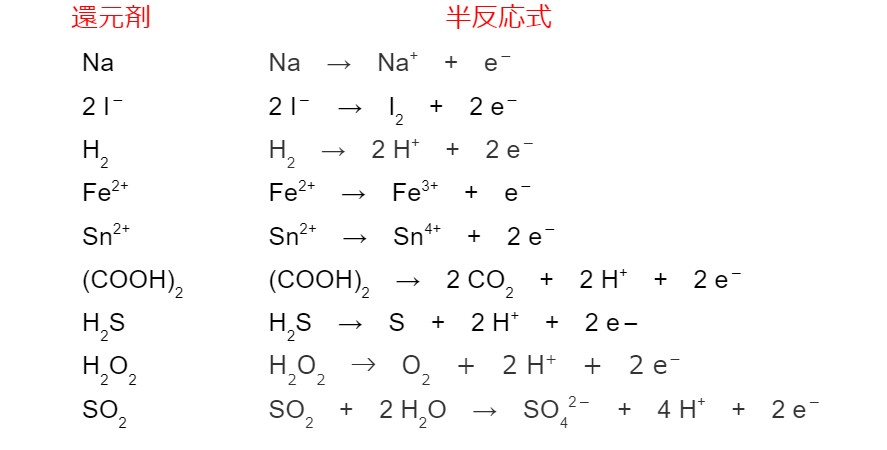
最初のポイントは、反応に存在する各原子および/またはイオンのNox (酸化数) を計算することです。これは、Nox の変化をすぐに認識できないことが多いためです。化学種の Nox を決定する方法に関する質問については、「 酸化数 (Nox) の決定」のテキストをお読みください。

例を見てみましょう:
+1 -2 0 +1 -2 +1 +6 -2 +1 -1
H 2 S + Br 2 + H 2 O → H 2 SO 4 + HBr
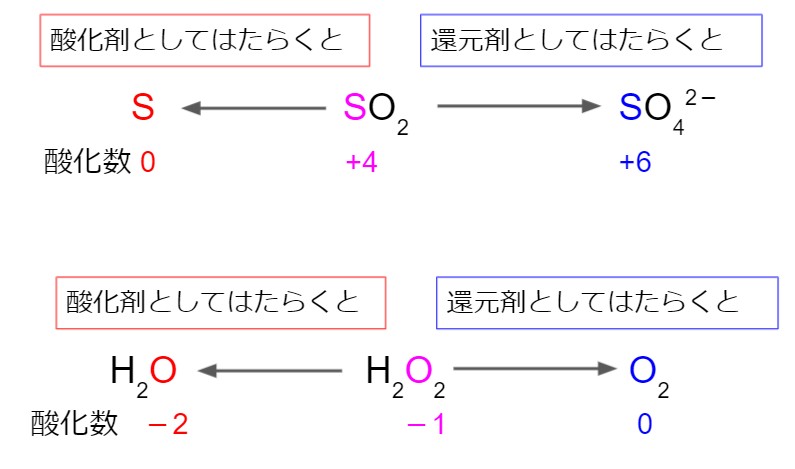
2 番目のステップは、Nox に変化があるかどうかを観察し、どの物質が酸化し、どの物質が還元したかを判断することです。
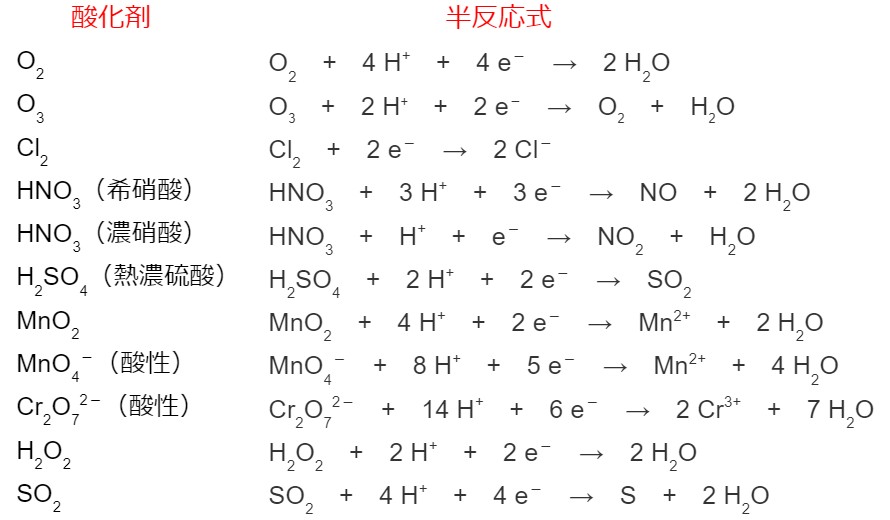
上記の場合、硫黄 (S) は、NOx が -2 から +6 に増加するにつれて酸化、つまり電子を失ったことに注意してください。一方、臭素は還元されて電子を獲得し、その Nox は 0 から -1 に減少しました。したがって、次のようになります。


硫黄が失った電子は臭素によって受け取られ、したがって硫黄は臭素の還元を引き起こし、したがって硫黄は還元剤です。臭素ではその逆が起こり、硫黄から電子を受け取って酸化を引き起こします。したがって、臭素は酸化剤です。

