共有結合は常に水素原子間、非金属間、または非金属と水素間で発生します。それらが発生すると、次のように表されます。
単結合 (?):シグマ ( σ )と呼ばれる結合を表します。
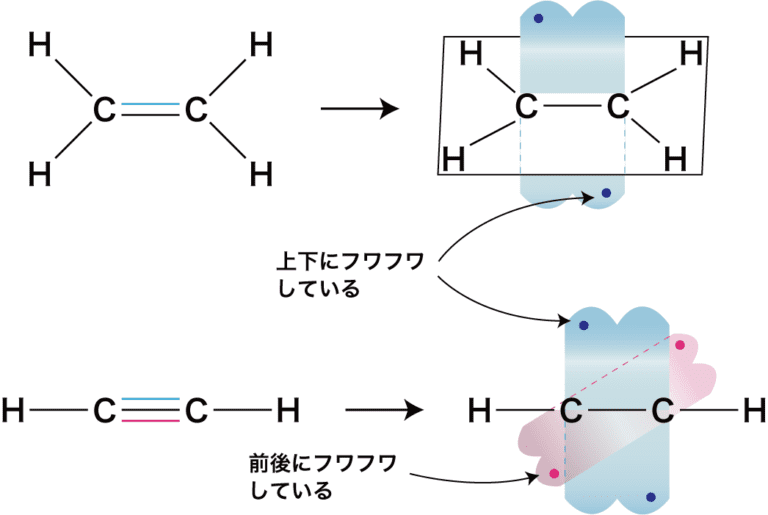
二重結合 (=): 2 つの結合を表します。1 つはシグマ (σ) で、もう 1 つはパイ ( π )です。
三重結合 (≡): 1 つのシグマと2 つのパイ ( π ) の3 つの結合を表します。
共有結合は、ある原子の不完全な軌道(電子が 1 つある)が別の原子の不完全な軌道に相互侵入するときに発生します。パイ結合は、特に、p 軌道が平行軸上の別の p 軌道と相互貫入するときに発生します。
N 2分子 (窒素ガス) の例を参照してください。
N ≡ N
この分子 ( N 2 ) には三重結合があり、結合の 1 つがシグマ結合で、他の 2 つの結合がシグマ結合であるため、両方の窒素原子の 2 つの不完全軌道が平行軸上で相互貫入していると言えます。パイ型。それを証明するには、窒素の原子番号 (7 電子) を取得し、その電子分布を作成します。
1秒2
2秒2 2p3

その電子分布を観察すると、第 2 レベル (2p) の p サブレベルに窒素が 3 つの不完全軌道を持っていることがわかります。
窒素の p 副準位の 3 つの不完全な原子軌道
p 軌道は不完全であるため、模式図は次のようになります。
p 軌道は常にヘリックスで表されます

パイ結合は平行軌道間で発生するため、N 2分子に含まれる 2 つの窒素を考慮すると、これらの軌道 (赤と青) が何であるかがわかります。
N 2を形成する窒素原子の軌道
注: 2 つの空白軌道は同じ軸上で相互貫入し、シグマ結合を形成します。
これら 2 つの窒素原子間のパイ結合は、次のように 2 つの垂直軌道 (赤) と 2 つの斜めの軌道 (青) の間に作られる円弧 (黒) によって表現されます。

N 2分子に存在するパイ結合の表現




.jpg)