熱力学は、熱の獲得、損失、または欠如に関連する気体の状態変数 (圧力、温度、体積) の変化を研究する熱学の分野です。熱力学には 2 つの主要な法則があります。 1 つ目は、ガスの内部エネルギーを、ガスが受け取ったまたは放出した熱と、この熱によって行われる仕事に関連付けます。第 2 法則は、機械の効率、つまり受け取った熱を仕事に変換する能力に関係します。しかし、エネルギーは常に環境に失われるため、完璧な機械は存在しません。
熱力学に関するまとめ
熱力学では、システム内の熱の獲得、損失、または欠如によるガスの変化を研究します。
熱力学の第一法則は、システムの内部エネルギーが獲得される熱とそれによって実行される仕事に関連していることを決定します。
熱力学の第 2 法則により、システムから常にエネルギーが伝達されるため、完全な熱機関は存在しないことがわかります。
熱力学には、第 1 法則と第 2 法則に加えて、熱力学第 0 法則と熱力学第 3 法則という 2 つの非公式の法則があります。
熱力学の基本概念は、システム、外部環境、状態変数、気体変換などの構成要素の特定の表記法です。
熱力学は日常生活に広く応用されています。すべての内燃エンジンは、熱力学の法則の適用例です。

熱力学とは何ですか?
熱力学はの分野であり、その主な研究対象は、熱がシステムの状態変数にどのように影響するかです。熱は運動中の熱エネルギーです。つまり、熱は温度差がある場合にのみ存在します。システムのすべてのコンポーネントが同じ温度に達した瞬間、熱はゼロになります。

熱力学の法則
熱力学には 2 つの主要な法則または原則があります。
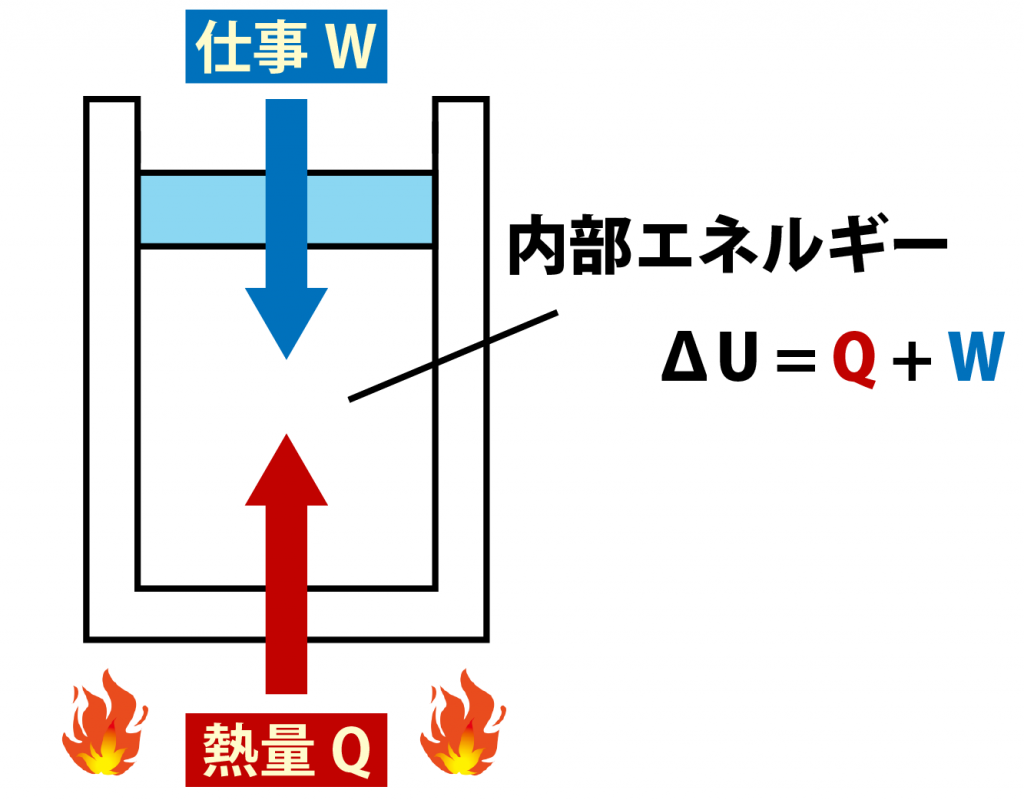
熱力学の第一法則:この原理は、システムの内部エネルギーが、ガスが受け取る熱またはガスが放出する熱とガスが実行する仕事の差に等しいと決定します。気体が熱を得ると、その温度が上昇し、その温度上昇により内部エネルギーも増加します。温度が上昇すると、ガスの体積も増加し、その結果、ガスが入っている容器の壁を移動させる仕事をします。
熱力学の第 2 法則:システムのすべてのコンポーネントが同じ温度になるまで、熱は常に温度の高い物体または環境から温度の低い別の場所に流れると決定します。これによりシステムのエントロピーが増加します。エントロピーはその構成要素の混乱または無秩序の尺度です。
ただし、これら 2 つの法則に加えて、熱力学には 2 つの非公式の法則があります。
熱力学の第 0 法則: 2 つ以上の物体と環境が同じ温度にある場合、系全体は平衡状態になるため、温度が高くても低くても熱は発生しないと述べています。
熱力学の第 3 法則: システムが絶対零度(ゼロ ケルビン、または -273 °C) に到達することは不可能であると述べています。この温度では、ガスを構成するすべての粒子が静止しているため、エントロピーはゼロに非常に近くなります。
重要:関連する観察として、冷たさと熱さの概念は熱感覚を扱うものであり、生物によって異なる可能性があるため、科学的には存在しません。したがって、身体がどれだけ暑いか寒いかを測定することはできません。測定できるのは熱の有無、または温度の測定です。

熱力学の概念
熱力学には独自の概念がいくつかあります。主なものを以下に挙げます。
システム:問題の分析または研究の対象となる物体、物体と環境のセット。
外部環境:システムの一部ではないもの。
状態:システムがその温度、占有空間、および占有しているコンテナの壁にかかる圧力に関連した状態。
状態変数:熱の獲得、損失、または欠如によって変化する可能性のあるガスの特性であり、この場合は圧力、温度、体積です。
ガス変換:これらは、熱に関連するガスの状態変数によって起こる変化です。温度が一定に保たれる場合、それは等温変態です。圧力が一定の場合は等圧変換です。体積が一定の場合、等積変換または等体積変換です。そして、ガスと外部環境との間に熱交換がなく、温度が変化する場合、それは断熱変態です。
熱機械:機械がエネルギーを伝達または変換できるあらゆる装置であると考えると、熱機械は、タスクを実行するために熱を別の種類のエネルギーに変換する機械です。

熱力学の公式
→ 熱力学の第一法則
熱力学第 1 法則では、系の内部エネルギーの変化 (記号 ΔE、ジュール J で測定) は、ガスが受け取るか与えられる熱 (記号 Q、ジュール J で測定) と気体に与えられる熱の差に等しいと述べています。彼によって実行された仕事(記号 W 、ジュール J で測定)。
\(∆E=QW\)
気体が熱を受けるとQは正になります。負ければマイナスになる。気体が膨張すると仕事Wは正になります。収縮すると仕事はマイナスになります。
エネルギーの変化はガスの温度に関係します。したがって、等温変換では、温度が一定である場合、温度はゼロになり、熱と仕事が等しいとして方程式が書き直されます。
Q = W
等容積変換では、容積は一定であり、仕事は容積の変化に関連します。したがって、仕事はゼロとなり、内部エネルギーは熱と等しくなります。
\(∆E\) = Q
断熱変態では、ガスと媒体の間に熱交換が存在せず、Q はゼロになります。したがって、気体が膨張すると内部エネルギーは減少するため、内部エネルギーは負の仕事に等しくなります。
\(∆E\) = -W
例:
ガスは円筒形の容器に封入されており、可動ピストンによって密閉されています。 5.4KJの熱を受けて膨張しピストンを押し、3900Jの仕事をします。気体の内部エネルギーはどのように変化したのでしょうか?
解決:
問題のあるデータを抽出します。
Q = 5.4 KJ (熱を受けたので正)
W = 3900 J (ガスが膨張したため正)
\(∆E\) = ?
KJ を J に変換する必要があります。1 KJ は 1000 J に相当するため、これを行うには 1000 を掛けます。
Q = 5.4 KJ · 1000 = 5400 J
\(∆E=QW\)
\(ΔE=5400-3900\)
\(∆E=1500\ J\)
→ 熱力学第二法則
熱力学の第 2 法則は、熱エンジンの効率 (記号 η) に関連しています。効率は、仕事 W と熱源によって受け取られる熱係数 Q Cとの比であり得ます。
\(η=\frac{W}{Q_c }\)
パーセンテージに関しては、結果に 100% を掛けます。
\(η=\frac{W}{Q_c\cdot100%}\)
熱源 Q Cによって提供される熱は、冷熱源 Q F (この場合は環境) に与えられる熱と仕事の合計に相当します。
\(Q_C=W+Q_F\)
効率は、1 とマシンの有効電力 P Uと総電力 P Tの比の差であることに注意してください。
\(η=1-\frac{P_U}{P_T }\)
熱源 T Cと冷源 T F (機械から熱を受け取る) の温度に関して、効率は次の方程式のように書くことができます。
\(η=1-\frac{T_F}{T_C }\)
例
エンジン内の特定のガスは 40,000 J の熱を受け取り、冷たい熱源により 16,000 J を失いました。このエンジンの効率は何パーセントですか?
解決:
データの抽出:
Q C = 40000 J
Q F = 16000 J
η = ?
収入を計算するには、まず仕事を取得する必要があります。
\(Q_C=W+Q_F\)
\(40000=幅+16000\)
方程式の辺を逆転すると、次のようになります。
\(W+16000=40000\)
\(W=40000-16000=24000\ J\)
\(η=\frac{W}{Q_c}\cdot100\%\)
\(η=\frac{24000}{40000}\cdot100\%=0.6\cdot100\%=60\%\)
\(η=60\%\)

熱力学の応用
熱力学は人間の日常生活に広く関与しています。この例としては、自動車の内燃機関の動作が挙げられます。タンク内の燃料は、電子噴射による火花によって燃焼します。この燃焼によってエンジンを構成するピストンが膨張し、車が動くようになります。熱が媒体に伝わった後、このプロセスが繰り返されます。

圧力鍋もその一例で、内部の液体が熱を受けて部分的に気体状態になります。次に、ガスは熱を受け取り続け、その温度が上昇します。容器は柔軟性に欠けるため、容器内の圧力が高まり、余分な蒸気が鍋上部の出口から放出されます。
こちらもご覧ください:
