温度ごとに、同じ物質には最大蒸気圧があります。これは基本的に、蒸気状態にある分子の数が最大となり、それ以上変化しない飽和度であり、液体部分と動的平衡状態に入り、次のような影響を及ぼします。液面にかかる圧力。
動的平衡状態にあるということは、蒸気状態になった分子が同じ数だけ液体状態に戻ることを意味します。
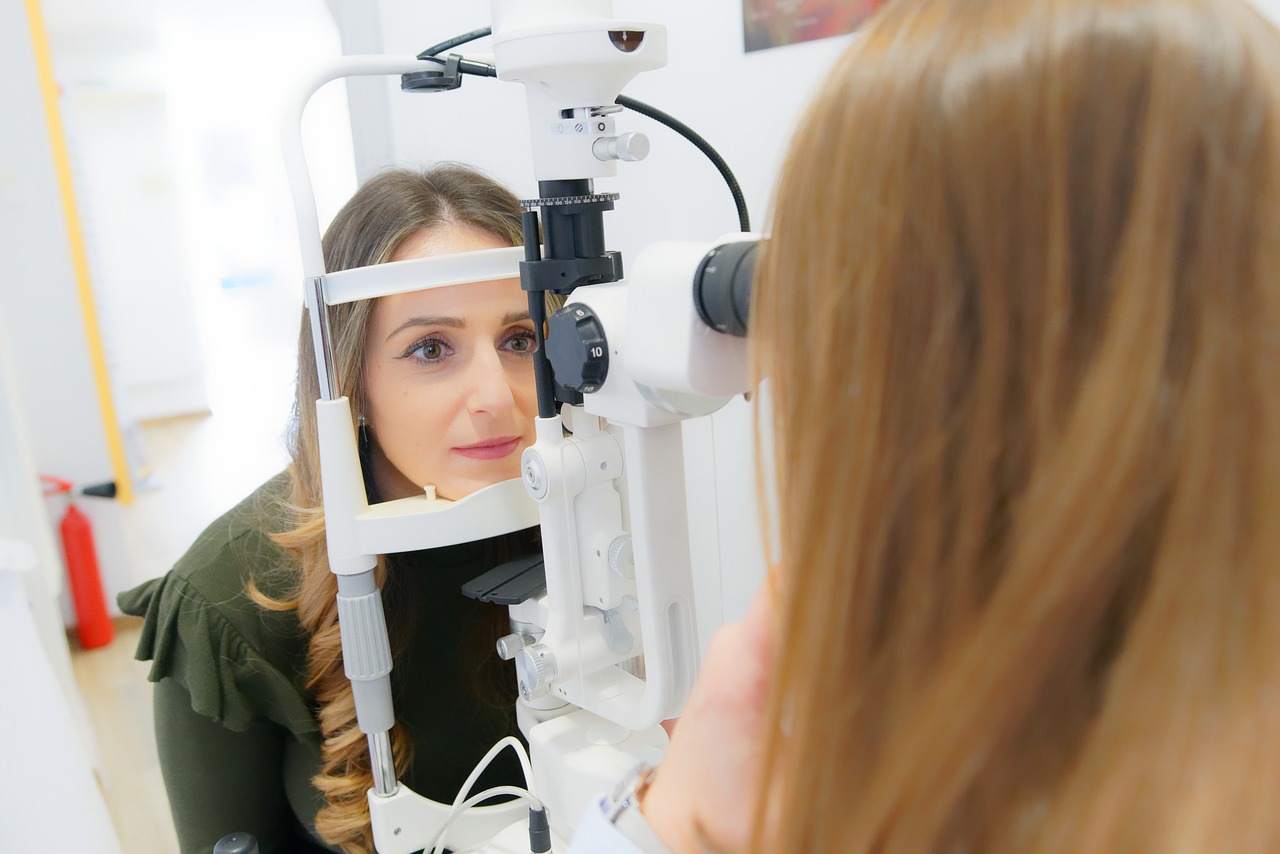
ただし、純粋な液体に不揮発性の溶質を追加すると、最大蒸気圧は低下します。 私たちはこの現象を眼圧効果と呼び、この特性の研究は眼圧検査または眼圧測定と呼ばれます。
たとえば、コーヒーを作るときに、沸騰し始めた量の水に砂糖を加えると、沸騰が止まることに気づいたことがありますか?なぜこのようなことが起こるのでしょうか?眼底鏡検査が説明します。
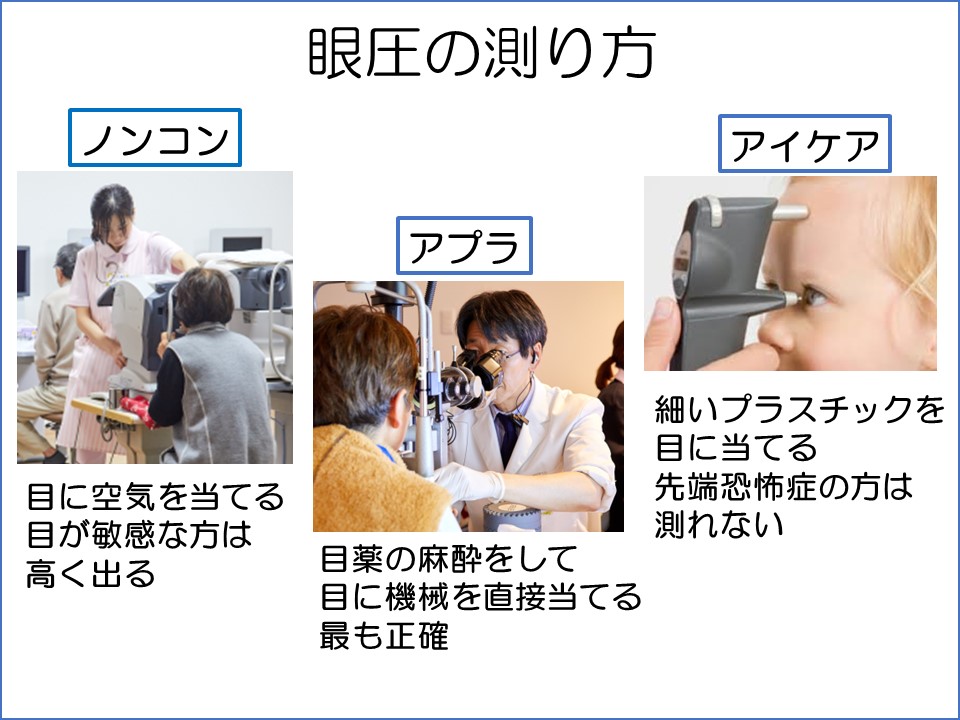
温度が上昇すると、水分子は分子間結合を破壊し、液体の塊から逃げるのに十分なエネルギーを受け取ります。しかし、砂糖を加えると、その分子は水分子と相互作用し、分子間相互作用の量が増加します。こうすることで、蒸気状態になりにくくなります。沸騰するには、より多くのエネルギーを水分子に供給する必要があり、これはシステムの温度をさらに上昇させることを意味します。
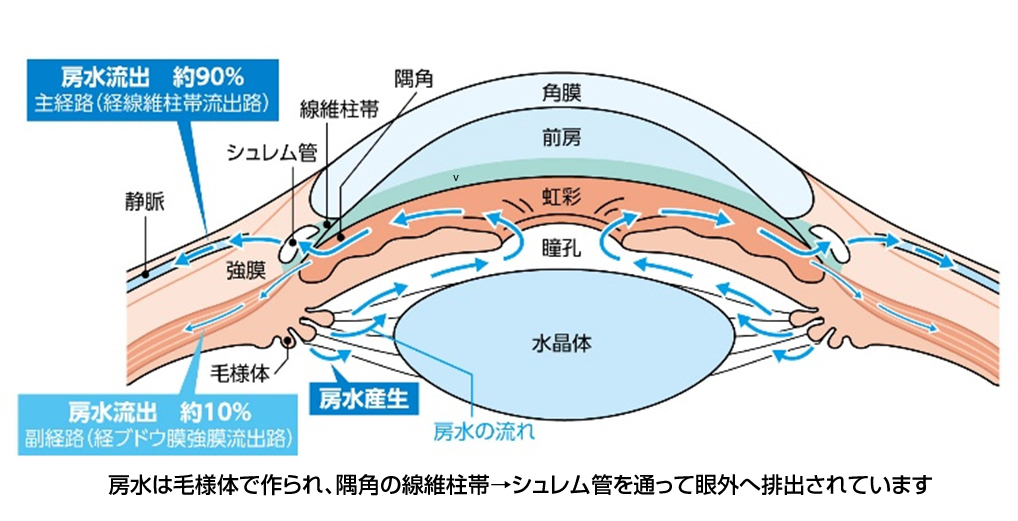
この現象は沸点に近い点だけでなく、液体のあらゆる温度でも発生します。特定の温度で、溶質を添加する前後の液体の蒸気圧を比較すると、純粋な液体の最大蒸気圧が常に溶液の最大蒸気圧よりも大きくなることがわかります。
さらに、私たちが常に観察するもう 1 つのことは、より濃縮された溶液はより希薄な溶液よりも常に小さいということです。つまり、砂糖を追加するほど、蒸気圧はより大きく減少します。これは、液体の蒸気圧が溶液中に分散している溶質粒子のモル数に反比例することを示しています。
これが、眼圧検査が総合的な特性である理由です。つまり、それは物質の性質ではなく、所定の体積の溶媒に加えられる粒子の量に依存します。たとえば、スクロース溶液とグルコース溶液の濃度が 0.1 mol/L であるとします。したがって、この場合、両方の溶液の蒸気圧は同じであると結論付けることができます。
ただし、イオン溶液の場合は、イオン化やイオン解離が起こることも考慮する必要があります。たとえば、濃度が 0.1 mol/L の塩化ナトリウム (NaCl) 溶液の蒸気圧は、前述の蒸気圧の 2 倍になります。これは、NaCl の分子ごとに 2 つのイオン (Na +と Cl – ) が放出されるためです。

蒸気圧の低下は、圧力と温度の関係を示すグラフで表すことができます。以下の一般的な例では、同じ温度「t」では、溶液の蒸気圧が溶媒の蒸気圧よりも低いことがわかります。

この現象の定量的側面は、ラウールの法則によって与えられます。


