アミンは、アンモニア (NH 3 ) から誘導される化合物です。有機基で置換された水素ごとに、アミンの種類 (第一級、第二級、第三級) が得られます。これらは塩基性の化合物であり、強い生臭さを放ちます。融点、沸点、密度などの化学的特性の多くは、窒素に結合した炭素鎖のサイズと種類によって異なります。
この官能基の命名は、「アミン」という用語が接尾辞として存在するため、間違いがありません。アミンはアミノ酸として私たちの体内に存在します。 そして これらは染料や医薬品の製造に使用されます。
アミン構造
アミン分子は三角錐のような構造をしています。化学ではこれを錐体構造と呼びます。窒素は「ピラミッドの頂点」にあり、(sp3) タイプの結合を介して有機ラジカルに結合するか、ピラミッドの底部の頂点にある非置換水素に水素結合によって結合します。
アミンの分類
アミンはアンモニア (NH 3 ) から誘導されます。したがって、アンモニアの水素がラジカル、炭化水素のグループ (文字「R」で表される) によって置き換えられます。アミンの分類は、置換された水素の数に従って行われます。
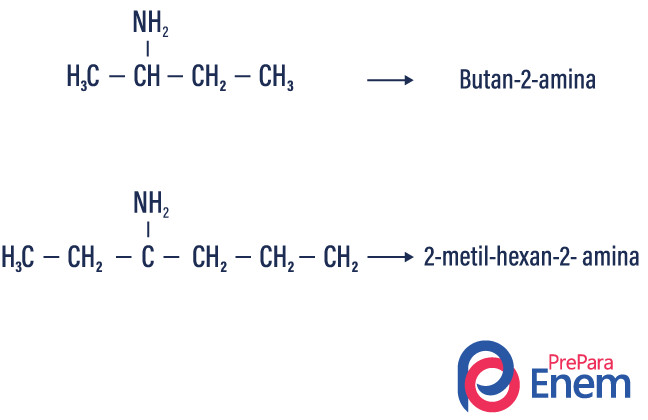
第一級アミン→ 有機ラジカルによる水素の置換 (R-NH 2 )。
第二級アミン→ 2 つの水素が 2 つの有機ラジカル (R 1 R 2 NH) で置換されます。
第三級アミン→ 窒素に結合した 3 つの水素を有機ラジカル (R 1 R 2 R 3 N) で置換します。
アミンの性質
溶解度:炭素数 5 までの分子は水とアルコールに可溶ですが、炭素数5 を超えるアミン分子は水に不溶です。
密度:開鎖有機ラジカルを持つアミンの密度は 1 g/m3 未満で、芳香族化合物を形成するアミンの密度は 1 g/m3 を超えます。
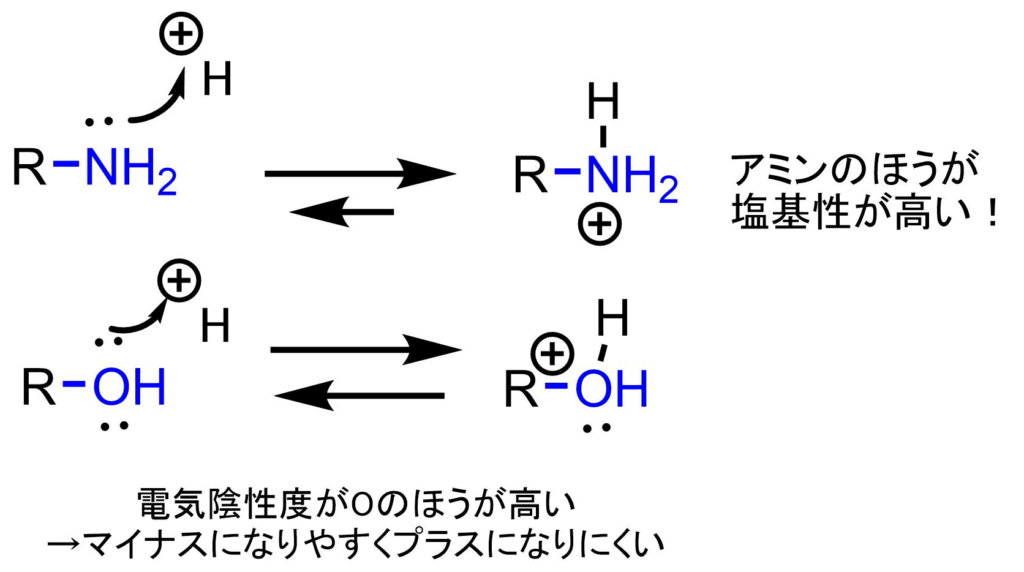
塩基性:アミンは不対電子対により塩基性の性質を持ち、分子はこの電子対を供与して H +イオンを受け取ります。芳香族アミンは、自由電子対が分子内に存在する芳香環と共鳴するため、弱い塩基になる傾向があります。
毒性:芳香族アミンは健康に有害な有毒化合物です。
アミンの特徴
物理的状態:常温常圧条件下では、分子内に炭素数 1 ~ 3 のアミンは気体です。炭素数が 3 ~ 12 の場合、それらは液体です。分子内に 12 個を超える炭素を持つアミンは固体です。
臭気:メチルアミンやエチルアミンなどの小さな有機ラジカルを持つアミンはアンモニアの特有の臭気を持ちますが、より大きな置換基を持つ他のアミンは強い生臭さを持ちます。
色:ほとんどが無色です。

アミン命名法
国際純粋応用化学連合 (Iupac) によると、鉱山官能基の命名法は次のようになります。
第一級アミンの命名法
|
置換基の名前 + 窒素に直接結合した炭素の位置 + アミンという用語 |
→ 部首の命名法
接頭語 (炭素数を示す) + 中置語 (結合の種類を示す)
|
プレフィックス |
中置語 |
|
1カーボン:メット 炭素数6: 16進数 |
1 つの単結合: – 1 つの二重結合: – en 三重結合 1 個: – ino 2つの二重結合: –ジエン |
→アミンの位置:窒素に直接結合している炭素を見つけるには、アミンに近い側から始めて鎖内の炭素を数える必要があります。位置が炭素上にある場合、それを命名法で明示する必要はありません。
例:
CH 3 -NH 2 → メタンアミン
CH 3 -CH 2 -NH 2 → エタンアミン
CH 3 -CH 2 -NH 2 –> エタンアミン
第二級アミンおよび第三級アミンの命名法
N + 小さいラジカル (接頭辞 +yl) + 大きいラジカル (結合の種類を示す接尾辞付き) + アミン
命名法の前にある文字 N は、アミン官能基の特徴である炭素鎖に結合した窒素を指します。
例:
CH3-NH2-CH2-CH2 → N-メチルエタンアミン
CH3 – NH2-CH2-CH2-CH3 → N-エチル-プロパンアミン
こちらもご覧ください:ニトロ化合物の命名法 – その方法?
アミン反応
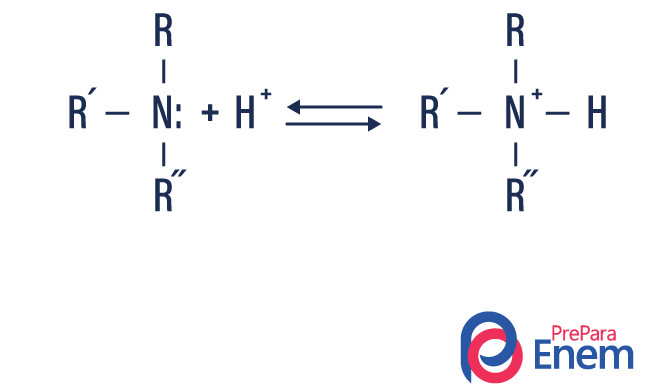
酸塩基反応
アミンには一対の不対電子があり、これが分子に基本的な性質を与えます。酸塩基反応では、アミンは H +イオンを受け取り、プロトン化された分子になります。
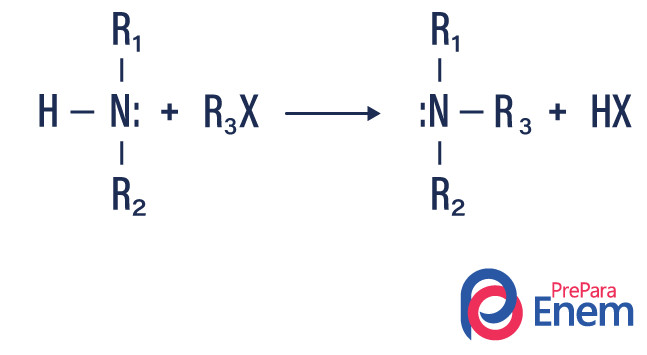
アミンのアルキル化
このタイプの反応では、第一級または第二級アミンの窒素が有機ハロゲン化物に移動し、アルキル置換アミンと酸が生成されます。
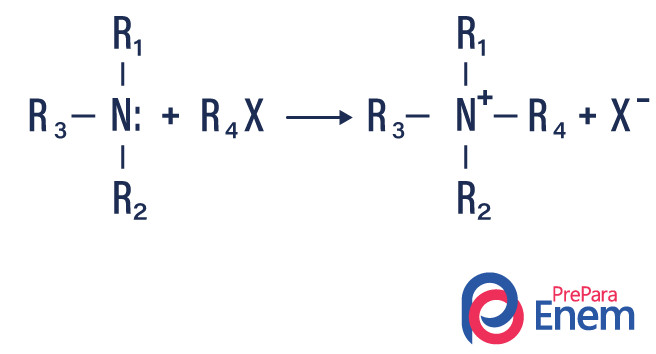
反応が三級アミンと行われる場合、反応生成物はプロトン化された四級アミンとハロゲンアニオンになります。
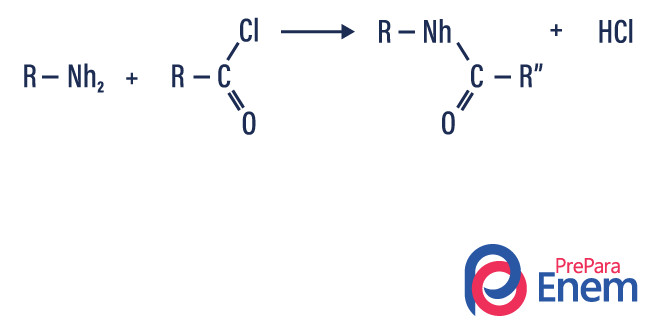
アミンのアシル化:第一級アミンまたは第二級アミンの間で起こり、場合によっては塩化アシル (RCOCl) とともに起こり、アミドと酸を形成します。
また、カルボン酸無水物 (RCO) 2 O でも起こり、アミドとカルボン酸が形成されます。
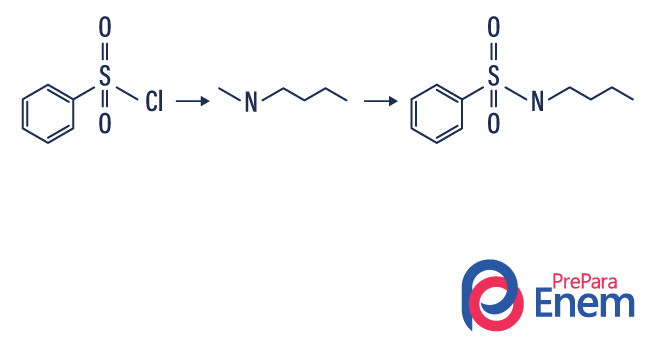
スルホンアミド反応
スルホンアミド反応は、一級アミンおよび二級アミンの検出に使用されるヒンスベルグ試験で起こる反応です。この場合、塩化スルホニル (C 6 H 4 ClO 2 S) がアミドと反応して、スルホンアミドが形成されます。
日常生活におけるアミンの使用
これらは、菓子に使用されるアニリンなど、食品に適用される人工着色料の製造に使用されます。
これらは有機化合物の合成や石鹸や化粧品の製造に使用されます。
それらは有機物の分解プロセスの一部です。私たちが感じる強くて不快な臭いは、カダベリン (C 5 H 14 N) など、プロセス中に存在するアミン基分子から生じます。
第一級アミンは、鉱物産業で金属に利益をもたらしたり、金属を精製したりするために使用されます。アミンは浮選剤として使用され、ミネラルを不要な残留物から分離します。