1884 年、スウェーデンの化学者スヴァンテ アレニウスは、化学溶液を使用していくつかのテストを実施しました。彼はそれらに電流を流し、この電流が溶液に伝わるかどうかを観察しました。溶液が電解質である場合、つまり電気を通す場合、システムに接続されているランプが点灯します。ランプが点灯しない場合は、溶液は電解質ではありません。
この科学者は、溶液に電流が流れるのは、溶液にイオンがあるためであると結論付けました。イオンは電荷を持った原子または原子のグループであり、バッテリーなどの発電機からの電荷を運ぶことができる化学種です。
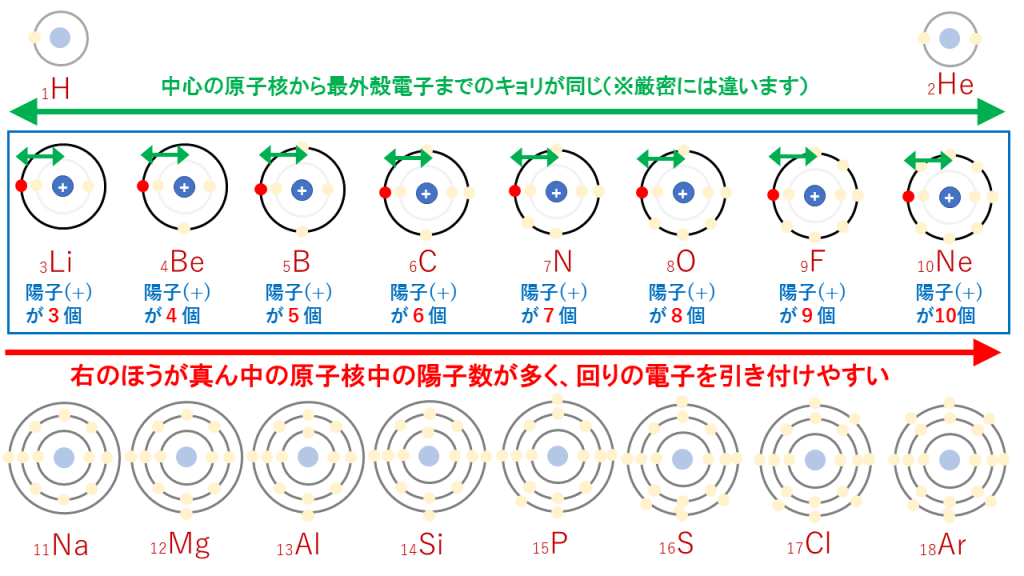
溶液中でイオンが形成される仕組みの 1 つは、水の中に分子物質を入れ、これらの化合物が反応するときに起こります。
たとえば、塩酸ガスは分子物質です。つまり、水素原子と塩素原子 (HC) の間で電子対を共有することによって形成された分子で構成されています。
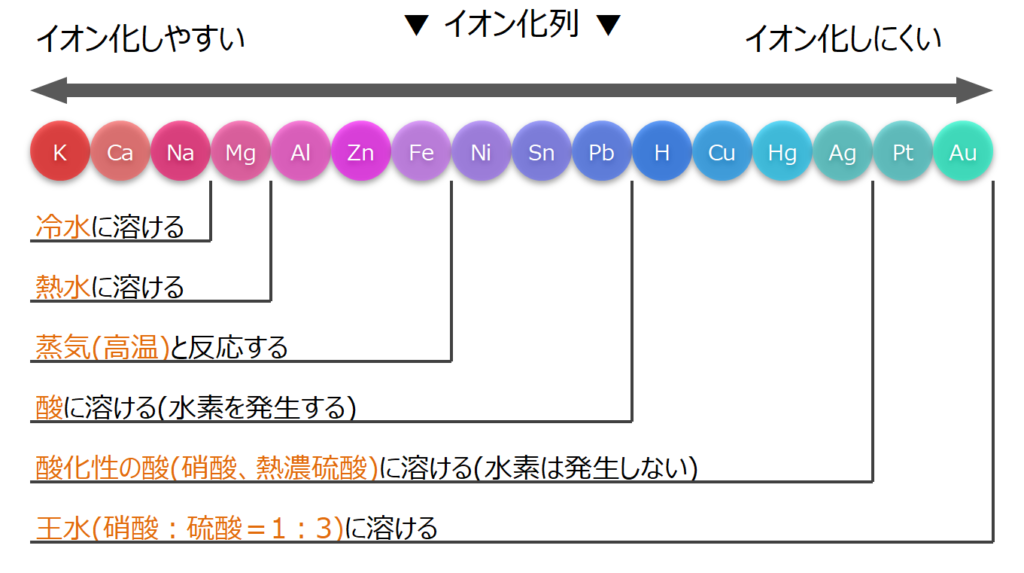
塩素原子は水素原子よりも電気陰性度が高く、共有結合から電子対を自身に向かって引き寄せ、極性分子を作成します。塩酸ガスを水に加えると、その中の水素陽イオン (H + ) が HC? 分子の負の部分 (塩素) をより強く引き付けます。一方、水のヒドロキシルアニオン (OH – ) は、HC 分子のプラスの部分 (水素) を引き付けます。
その結果、塩酸ガス分子が分解され、H + (aq)と C? イオンが生成されます。 – (aq) 。

このイオン化は次のように表すことができます。
一般に、上記の方程式で行われたように、反応物としての水は省略されます。しかし、最も正しいことは、それを反応物として式に書き込むことであり、生成されるカチオンはヒドロニウム (H 3 O + ) です。
HC? (g) + H 2 O (?) → H 3 O + (aq) + C? – (aq)
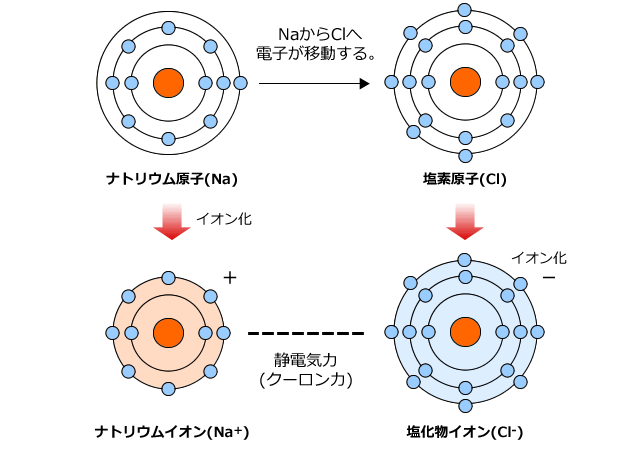
したがって、イオン化現象は、水が反応物質として作用し、以前には存在しなかったイオンを生成するときに起こる化学反応です。
このテーマに関するビデオレッスンをぜひご覧ください。



