オクテット則によれば、原子が安定性を獲得するには、価電子殻 (原子核の最も外側の殻) に 8 つの電子が必要ですが、K 殻のみを持つ原子の場合は 2 つの電子だけが必要です。つまり、希ガス構成です。
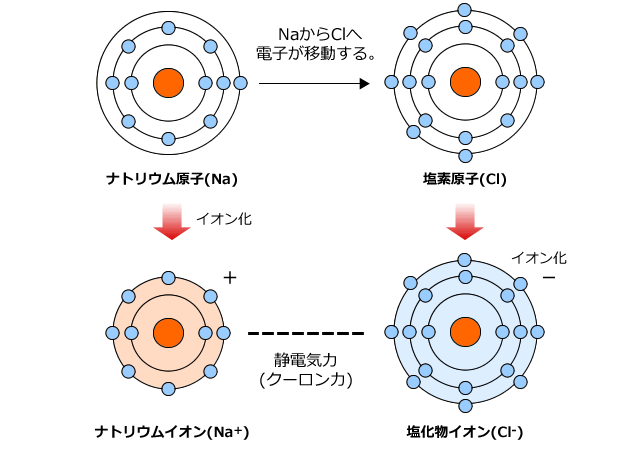
したがって、ナトリウム (Na) と塩素 (Cl) の原子が結合して塩化ナトリウム (NaCl)、つまり食塩を形成することを考えてみましょう。中性状態では、ナトリウム原子の価数は 1 個の電子です。シェル。したがって、最後の殻に 8 個の電子を持ち、安定するためには、この電子を失う必要があります。塩素原子の価殻には 7 つの電子があり、安定するには 1 つの電子を受け取る必要があります。したがって、ナトリウム原子は塩素原子に電子を与えます。したがって、正イオン (ナトリウム陽イオン (Na + )) と陰イオン (塩化物陰イオン (Cl – )) があり、両方とも完全なオクテットを持ちます。

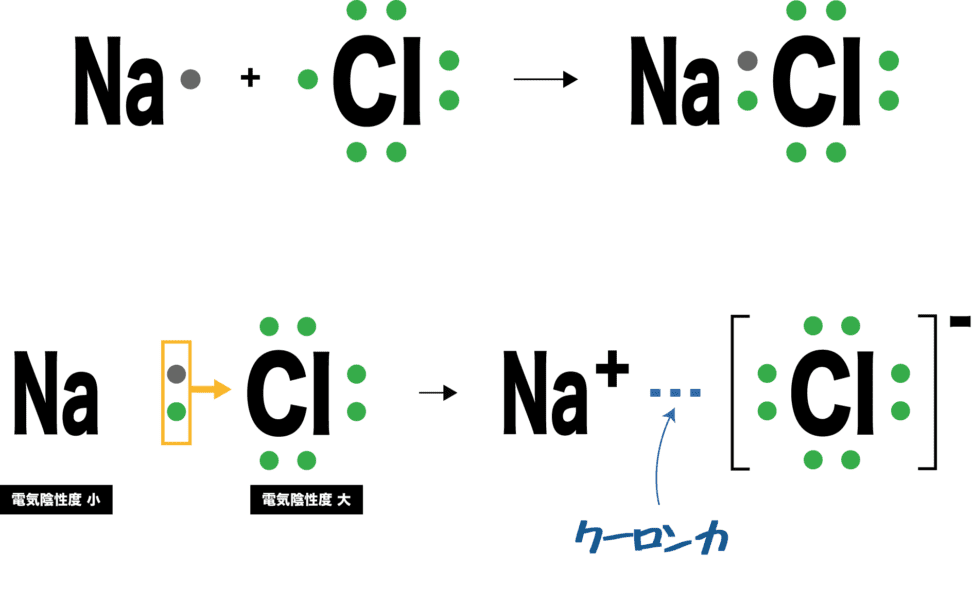
この場合、イオン結合が生じたと言います。したがって、

イオン結合は、電子の決定的な移動が起こる唯一の結合です。
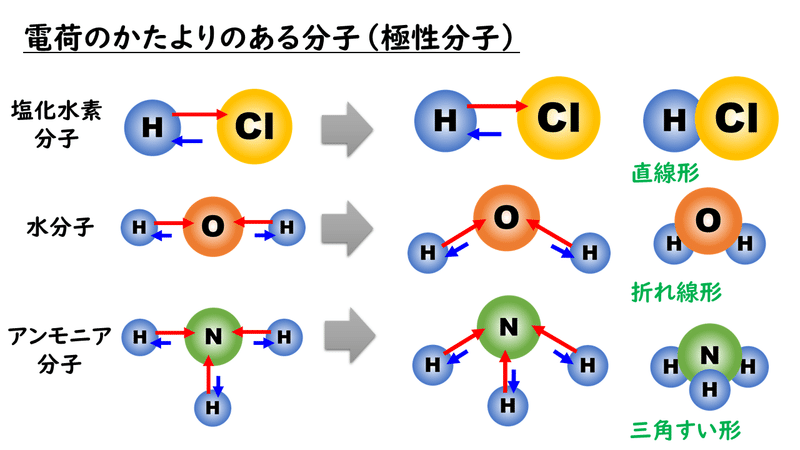
したがって、このタイプの結合は、反対の傾向を持つ原子間で発生します。つまり、一方は電子を受け取る傾向があり (ほとんどの場合、これらは族 15、16、17 の非金属であり、水素も含まれます)、もう一方は電子を供与する傾向があります (ほとんどの場合)。多くの場合、これらは族 1、2、および 3 の金属です)。
このテーマに関するビデオレッスンをぜひご覧ください。

