シリコン (Si) は原子番号 14 の化学元素で、炭素と同じ族である VI A 族の第 3 周期または周期表の第 16 族に属します。このため、ダイヤモンド(炭素の天然の同素体の一つ)に似た構造を持ち、化学反応も炭素と似ています。
ケイ素は、1824 年にスウェーデンの化学者ヨンス ヤコブ ベルゼリウスによって四フッ化ケイ素をカリウムと加熱することによって発見されました。

ベルゼリウスはシリコンを最初に調製した
ケイ素は、地球の地殻内で酸素に次いで 2 番目に豊富な元素 (27.7%) です。それは事実上すべての岩、砂、粘土、土壌に含まれています。
シリコンは自然界では孤立して存在することはなく、酸素と結合してシリカ (SiO 2 – 二酸化ケイ素) を形成することもあります。また、他の元素と結合して、主に石英 – SiO 2 、アスベスト – H 4 Mg 3 Si 2 O 9 、ゼオライト – Na 2 (Al 2 Si 3 O 10 )、H 2 O およびマイカ – K 2 Al 2 (Al) を形成します。 2Si3O10 )・H2O 。
アスベストについて少しお話しますと、土壌中には 30 種類以上の天然の繊維状ケイ酸塩が存在しており、これらは「アスベスト」としてよく知られています。このうち商業的関心のあるものは 6 つだけです。アスベスト岩石の 2 つの主なグループは次のとおりです。 (1) 蛇紋岩、地球上のすべての地質学的徴候の 95% 以上に相当する白色アスベストで、鉱物クリソタイル (Mg 3 Si 2 O 5 (OH) 4 ) で構成されています。 ; (2)角閃石: 褐色、青色、およびその他のアスベストであり、世界中で採掘されるすべてのアスベストの 5% 未満に相当し、鉱物トレモライト (Ca 2 Mg 5 Si 8 O 22 (OH) 2 ) で構成されています。 )およびアモサイト((Fe、Mg、Ca)OSiO 2・n H 2 O)。
アスベストは、タイル、タンク、水槽の製造、さまざまな建設製品、機械や設備の断熱に広く使用されています。しかし、アスベストのこの使用は多くの論争を引き起こしています。なぜなら、アスベストの繊維から出る粉塵を吸い込むと、「石肺」として広く知られる石綿肺に加えて、珪肺として知られる肺疾患やその他の健康上の問題を引き起こすからです。
白色アスベスト繊維およびそれから作られたタイル
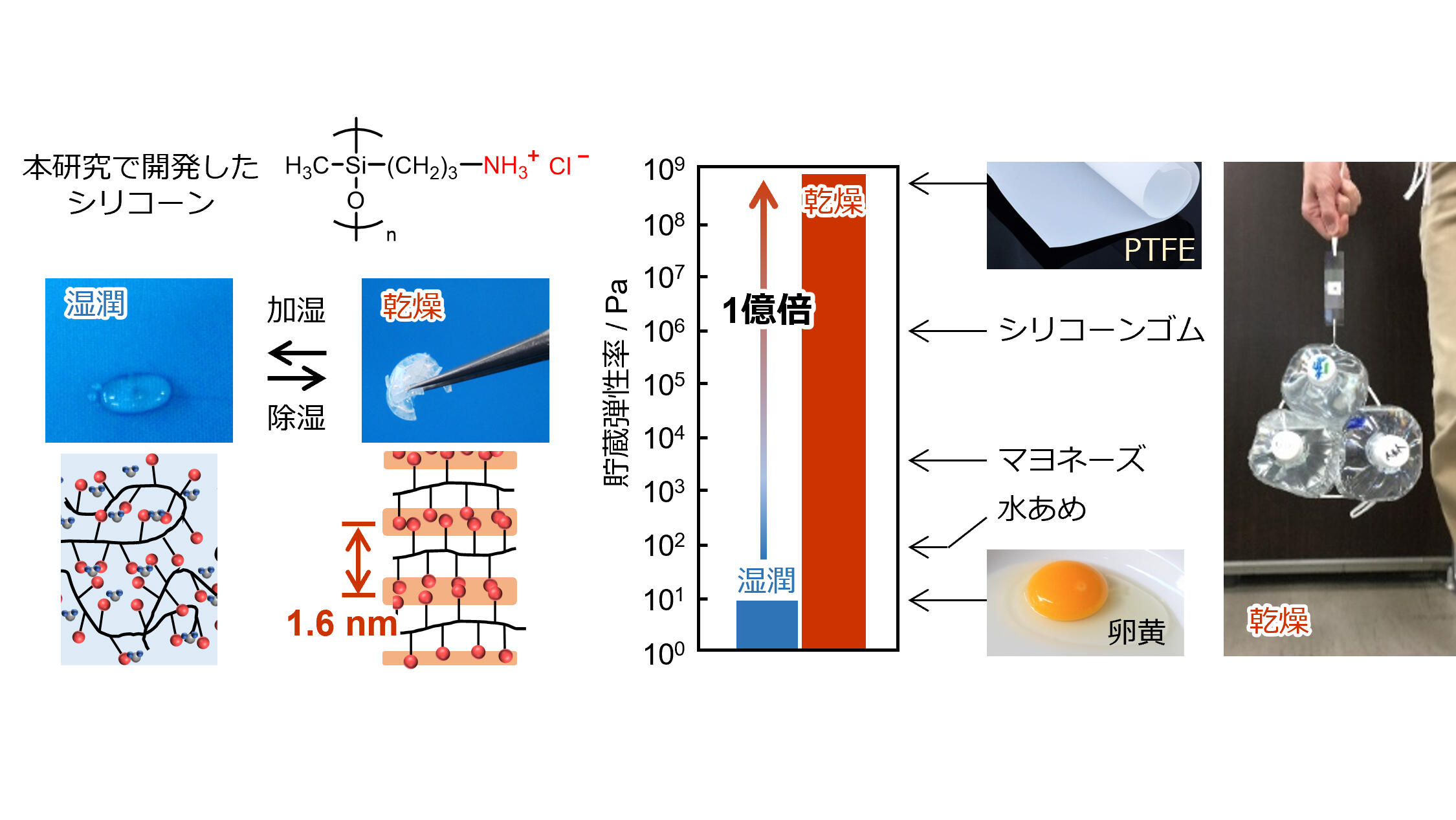
シリコンも炭素によって形成されるものと同様の縮合ポリマーを形成します。最もよく使用されるシリコン ポリマーの 1 つはシリコーンで、主にジクロジメチル シランまたはジクロロジフェニル シランの重合によって形成されます。以下に、一般的なシリコーンポリマー分子を形成する基本構造を示します (R は任意の有機ラジカルを表します)。
R R R R
│ │ │ │
… ─ ─ シ ─ ─ ─ シ ─ ─ ─ シ ─ ─ ─ シ ─ ─ …
│ │ │ │
R R R R
シリコーンはさまざまな用途に使用できますが、特に次のような用途に使用できます: おもちゃ、哺乳瓶の乳首、水泳用キャップ、車磨き剤、高抵抗ゴム、外科用器具用プラスチック、シール用シリコーン接着剤、形成外科のインプラントに使用されるプロテーゼ、とりわけ。
シール用接着剤および人工乳房におけるシリコーンの応用
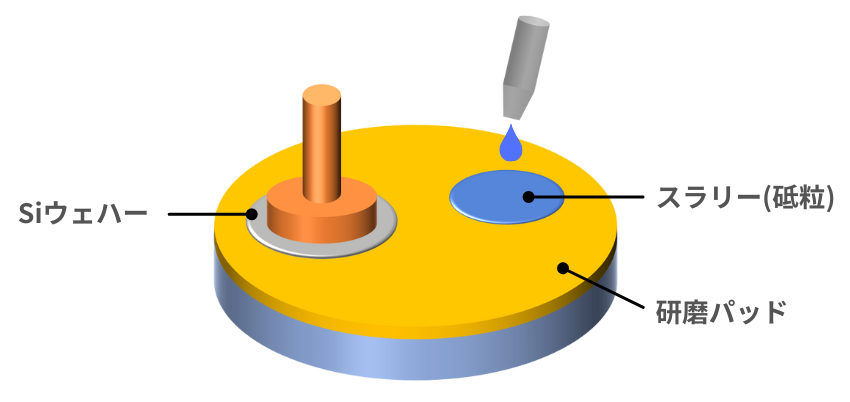
しかし、シリコンの最もよく知られた用途は、回路部品や電子チップに使用される半導体です。
シリコンは硬い固体で、色は濃い灰色で、金属光沢があり、ほとんどの電子回路の製造に広く使用されています。

.jpg)

