原子や分子などの微小な物体の数を数えるには、モルがよく使われます。
オブジェクトの 1 モル = 6.023 x 10 23オブジェクト

形態学的観点から見ると、mol という単語は、12、10、100 などの単語と同じカテゴリに属します。したがって、同じように次のように書くことができます。
リンゴ 1 ダース = リンゴ 12 個
リンゴ 2 ダース = リンゴ 20 個
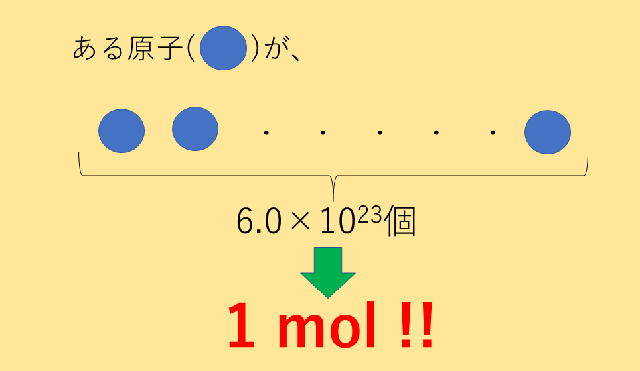
次のように書くことができます:
リンゴ 1 モル = 6.023 x 10 23リンゴ
リンゴ 2 モル = 12.046 x 10 23リンゴ
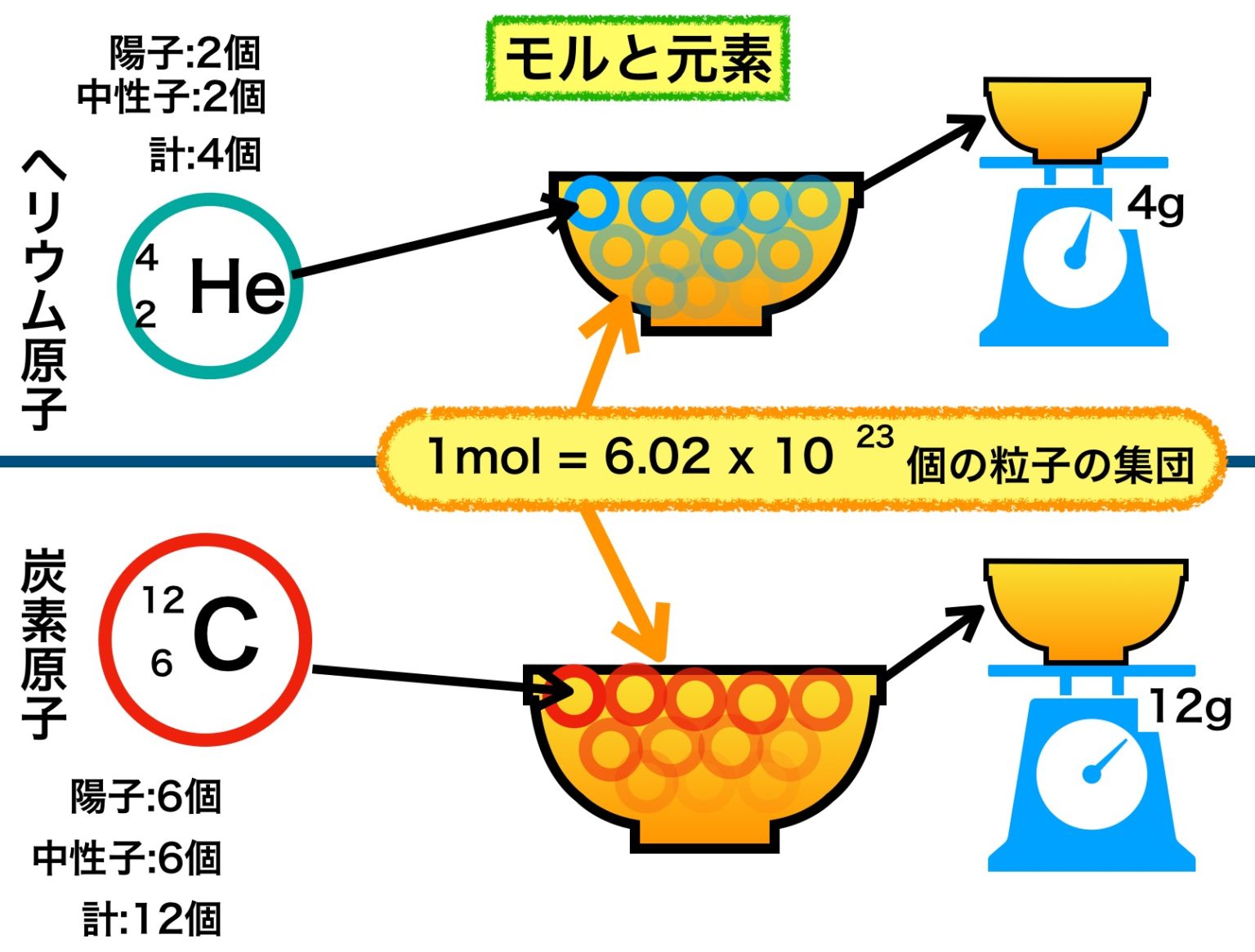
6.023 x 10 23という数字はアボガドロ数として知られており、通常は NA で表されます。
NA = 6.023 x 10 23粒子/モル = 6.023 x 10 23モル-1
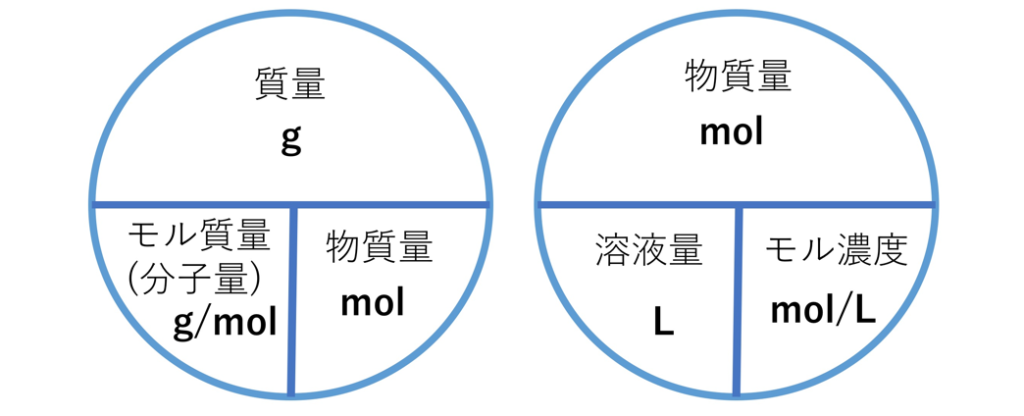
モル質量
元素のモル質量 (M) は、その元素の原子 1 モルの質量です。元素のモル質量は、原子質量を取得し、u 単位をグラム/モル単位に置き換えることによって取得できます。たとえば、原子量が約 27 μ のアルミニウムのようなものです。したがって、アルミニウムのモル質量は次のようになります。

M = 27 グラム/モル = 27 g/モル
物質のモル質量は、その物質の分子 1 モルの質量です。物質のモル質量は、分子量を取得し、単位 u をモルあたりのグラムに置き換えることによって取得できます。 n モルの原子を含む元素または物質のサンプルを考えてみましょう。元素のモル質量とサンプルの質量 (グラム単位) を M とすると、次のようになります。

m = n。 M または n = m/M
この主題に関連するビデオ レッスンをぜひご覧ください。
