日常生活において、私たちが卵やバナナなどの特定の製品を購入するとき、これは通常 12 個の「セット」または「ポーション」を使用して行われます。ダースは製品の 12 個に相当します。多くの場合、このタイプの購入が必要になります。たとえば、紙 1 連には 500 ユニットが含まれ、レンガ 1,000 個には 1,000 ユニットが含まれ、鉛筆やすりには 144 ユニットが含まれます。
化学では、原子、分子、式、イオン、電子の定量的な側面を扱うときに、同様の推論が発生します。これらは非常に小さいため、秤で個々の質量を測定することは不可能です。たとえば、水素原子の原子質量は 1 u にほぼ等しいことがわかっていますが、この値は非常に小さいため扱うことができません。

化学者は「計量」できる物質の量を必要としたため、質量を測定できる物質の一部または集合を扱うようになりました。さらに、この「部分」は、元素の原子量の値に比例して一定である必要があります。
そこで、1826 年にドイツの化学者ヴィルヘルム オストワルド (1853-1932) がモルの概念を導入しました。
?
モルは単位の名前であると同時に、物質の量の単位の記号でもあります。名前は単数形でも複数形でも発音できますが、単位は単数形でのみ言及されます。例: 「80 g のカルシウムには何モル(複数名)がありますか?」答え: 40 g には 2 mol (単数形) のカルシウムが含まれています。 」
1 ダースには 12 個の単位があるのと同様に、製品に関係なく、次のとおりです。
これはアボガドロ定数の値であり、現在いくつかの実験方法によって確認されています。
しかし、1モルの物質の質量はいくらでしょうか?これはモル質量で示されます。
モル質量は、元素の原子質量値の間に一定の比率を確立します。たとえば、酸素の原子量は 16 u であるため、酸素のモル質量は 16 g/mol です。
分子や式についても同様です。説明のために、酸素の場合を続けてみましょう。酸素ガス (O 2 ) の原子質量は 32 u (2.16 u) です。したがって、このガスのモル質量は 32 g/mol に等しくなります。
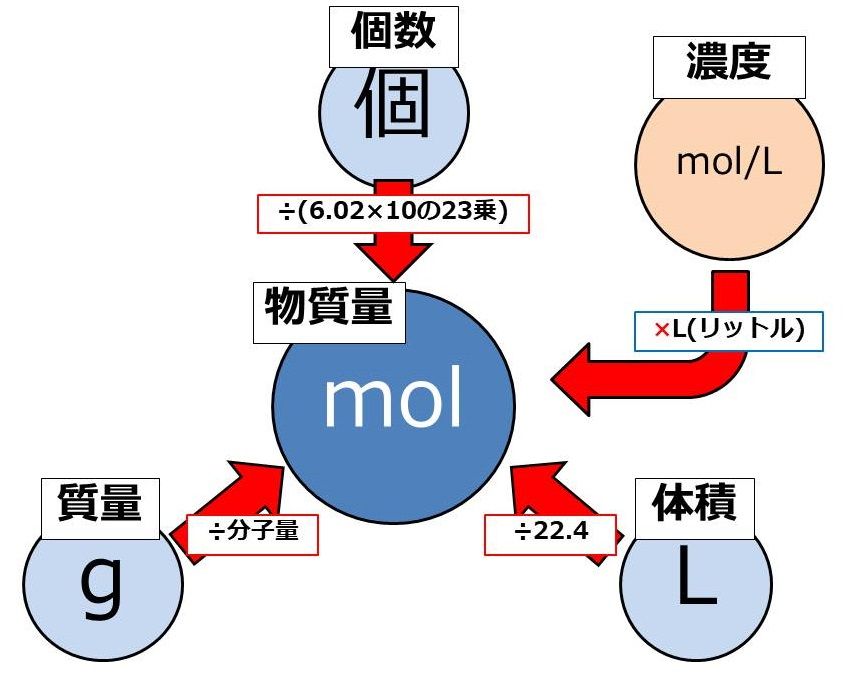
物質の量 (n)、つまり、化学元素または物質の特定の質量中に何モルが存在するかを決定するには、単純に 3 の法則または次の数式を使用します。
どこ:
n = 物質の量(モル単位)。
m = 与えられた質量 (グラム単位);
M = モル質量 (g/mol)
このようにして、サンプルを構成する化学物質の数 (たとえば、原子の数) を決定することもできます。
例:
88 g の二酸化炭素 (CO 2 ) サンプルに関して、次のことを決定します。
a) このサンプルには分子が何個ありますか?
b) モル数を決定します。
データ: 原子質量: C = 12 u、O = 16 u。
解決:
a) まず、二酸化炭素のモル質量を決定する必要があります。

M(CO 2 ) = 12 + 2 。 16 = 44 g/mol
1 mol の CO 2は 44 g であることがわかっているので、次の 3 つの規則を使用できます。
44 グラム —— 6.022 。 10 23分子
88g——x
x = 1.2。 10 24分子
88gでは1.2になります。 10 24分子の二酸化炭素 (CO 2 )。
b) 3 の法則または公式を使用できます。両方の方法を参照してください:
1 番目の方法: 3 つの規則 2 番目の方法: 数式
1 モル ——- 44 g n = m
n ———— 88g M
n = 88 n = 88
44 44
n = 2 n = 2
88 g グラムは、2 モルの二酸化炭素 (CO 2 ) を含む質量です。
この機会に、この主題に関連するビデオクラスをチェックしてください。




