化学者は、目で見て触れられる定量的側面、つまり質量(グラム)や体積(リットル)などの巨視的な量を扱いますが、研究では構成する原子や分子に何が起こるかが関係しているため、微視的な量も扱います。物質を説明し、巨視的な現象を説明します。
しかし、どうやって原子の質量を測定できるのでしょうか?原子の質量測定基準は何ですか?

明らかに、化学者にとって原子、イオン、分子の重さを秤で量ることは非現実的です。
この問題を解決するために、マクロの世界とミクロの世界を繋ぐ架け橋のような役割を果たすモグラの概念が登場しました。だからこそ、それは化学において非常に重要なのです。
この大きさが何を意味するかを理解するには、たとえば、ジュエリーの製造に使用される非常に小さな物体であるビーズを梱包する作業をしていると考えてください。各パッケージには 1,000 個のビーズが含まれている必要があるとします。このカウントをより簡単かつ効率的にするにはどうすればよいでしょうか?
ビーズを一つ一つ数えることは大変な作業ですので、扱いやすい量で基準を設けるのが適切でしょう。たとえば、秤で 10 個のビーズの質量を測定し、1,000 個のビーズの重量を調べることができます。 1,000 個のビーズが 90 グラムに相当するとします。90 グラムが参照標準になります。これに基づいて、質量中にビーズがいくつあるかを知ることができるからです。
この場合、大きな単位は質量によって数えます。例の場合、使用量は「ビーズの量」です。化学種の数の場合、つまり原子、分子、イオン、電子、式の量の場合、使用される量は物質量と呼ばれるようになり、文字nと単位で表されます。使用されるのはほくろです。
モルに関連する質量参照標準は、12 グラムの炭素 12 です。
炭素-12 ( 12 C) は、自然界で炭素元素の最も豊富な同位体 (98.94%) であり、6 つの陽子、6 つの中性子 (質量数 (A) は 12)、および 6 つの電子を含んでいます。自然界に低い割合で存在する他の炭素同位体は、炭素 13 と炭素 14 です。
12 g の12 C の質量は、正確に 12 u に等しい原子量を持っています。これにより、任意の原子の 1 モルの量が、グラム単位で表される原子質量の値に対応することが保証されます。たとえば、水素の原子質量はほぼ 1 u に等しく、これは12C原子の質量が水素原子の 12 倍であることを意味します。また、H のモル質量は 1 g となります。
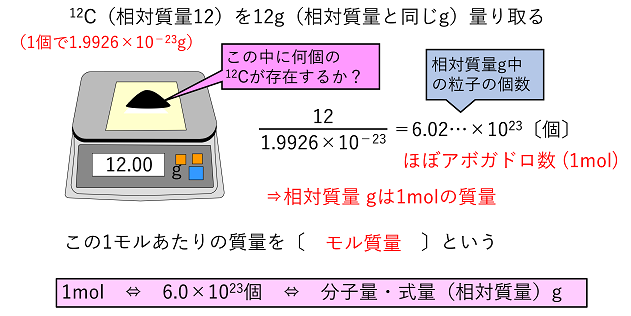
物質の場合、1モルの質量は分子量(原子量の合計)をグラム単位で表した値になります。
たとえば、すでに述べたように、H の原子量は 1.0 u、O の原子量は 16.0 u です。したがって、水の分子量は次のようになります。
H 2 O – (2. 1.0) + (1. 16.0) = 18.0 g/mol
したがって、 1モルの水には18グラムが含まれることがわかります。
炭素 12 は、1957 年に IUPAC (国際純粋応用化学連合) によって標準として確立され、豊富で安定しているため選ばれました。
しかし、これまではモルと質量を関連付けてきましたが、どのようにして化学種の特定の質量が持つ粒子の単位を数えることができるのでしょうか?たとえば、1 モルの水 (または 18 グラムの水) には何個の分子が含まれますか?
ここで、ほくろとアボガドロ数の関係が登場します。化学者はモルを使用して、特定のモル質量内に存在する実体 (原子、分子、イオン、式、または電子) の数を決定します。モルという言葉は 6.022 という数字を表します。 10 23 、これはアボガドロ定数の値です。
イタリアの化学者ロレンツォ・ロマーノ・アメデオ・カルロ・アボガドロ (1776-1856) は、原子質量と数値的に等しいグラム単位の質量を持つ元素のサンプルには常に同じ数の原子があるという考えを思いついた最初の科学者でした。彼自身はこの数字が何であるかを決定できませんでしたが、20 世紀を通じてこの数字を発見するために実験が行われ、最終的にそれが決定されたのは6.022 でした。 10 23 –、彼らはこの科学者に敬意を表してそれをアボガドロ定数と呼びました。
ロレンツォ ロマーノ アメデオ カルロ アボガドロ (1776-1856)

モル、アボガドロ数、原子質量の関係は非常に重要です。モル、粒子数、グラムの 3 つのうちの 1 つがわかれば、他の 2 つを決定できるからです。
たとえば、1モルの水には何個の分子が含まれていますか?
アボガドロ数に関連して、6,022 あることがわかっています。 1 モルの水には 10 23個の H 2 O 分子があり、18 g の水には 6.022 個の H 2 O 分子があるとも言えます。 10 23水の分子。
さらに 2 つの例を参照してください。
例 1: 1.5 mol の Fe 原子中に存在する質量はいくらですか?
鉄のモル質量は 55.85 g/mol なので、次のようになります。
1 mol ——- Fe 55.85 g
1.5モル—–x
x = 55.85。 1.5
x = 83.775 gの鉄
1.5 mol の Fe 原子に存在する質量は約 83.775 グラムです。
例 2: 80 g のメタン (CH 4 ) サンプル中にはどれくらいの物質が存在しますか?
- メタンの分子量の計算:
CH 4 = (1.12.0) + (4.1.0) = 16.0 g/mol

1モル —– 16.0g
× ———– 80
x = 80/16
x = 5 モル


.jpg)

