分子物質は、安定するために電子を受け取る必要がある元素の原子が結合して形成され、電子対を共有する化学結合 (共有結合) を形成します。
これは、ドイツの化学者ヴァルター コッセル (1888-1956) によって 1916 年に初めて発表された電子原子価理論と呼ばれるオクテット ルールに基づいて行われます。その後、アメリカの化学者ギルバート・ルイス (1875-1946)とアーヴィング・ラングミュア (1881-1957) によって独自に改良されました。

この理論は、自然界で原子が安定に孤立している唯一の元素は希ガス (族 18 または VIII A) であるという事実に基づいています。これらの元素はすべて、最後の電子殻 (価電子殻) に 8 個の電子、または 2 個の電子 (ヘリウムの場合は最初の殻 (K) のみ) を持ちます。
したがって、希ガスの電子配置を得るために、異なる元素の原子が化学結合を形成し、このようにして安定になることが確立されました。
その後、ギルバート N. ルイスは、分子内で確立されたこれらの結合を表現する方法を提案し、これはルイスの電子式として知られるようになりました。
この式は、関係する元素と原子の数だけでなく、各原子の価電子殻電子と各原子が共有する電子対の数も示すため、重要です。

価電子殻内の電子は点または x で表され、化学元素の記号の周囲に配置されます。共有電子は並べて配置されます。
この式がどのように記述されるかをいくつか例を挙げてみましょう。
- 水素ガスの分子式はH 2です。水素はその価電子殻に電子を 1 つだけ持っているため、周期表の IA 族に属します。したがって、各水素原子はその周りに「小さなボール」で表されます。 ? H.
オクテット則によれば、K 殻しか持たないため、価電子殻に 2 つの電子を持ち、安定を保つためには、さらに 1 つ電子を受け取る必要があります。このように、これら 2 つの水素原子は一対の電子を共有しているため、どちらも安定しており、その電子式は次のとおりです。
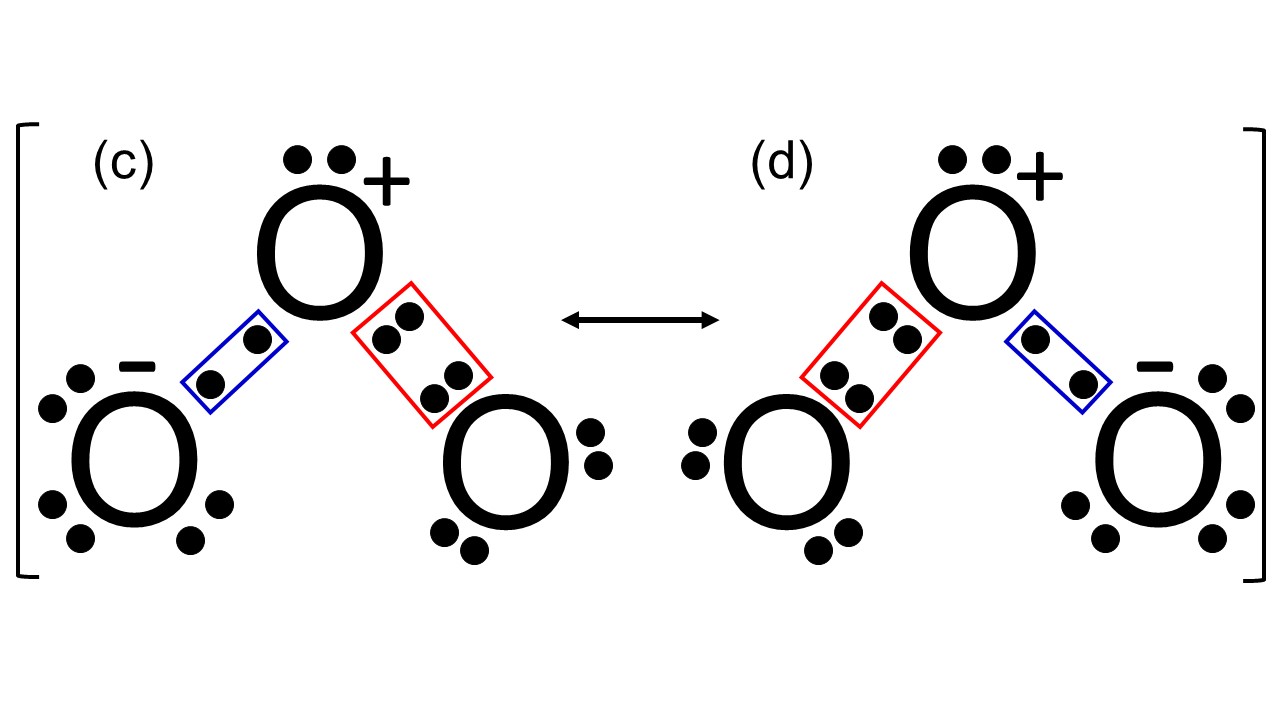
- 同じ理由に従って、すべて単体である酸素ガス ( O 2 )、窒素ガス ( N 2 )、塩素 ( C? 2 ) の分子式を書いてみましょう。
- 次に、複合物質の例をいくつか見てみましょう。
関連するビデオレッスン:

.jpg)

