一般気体方程式による計算は、気体の新しい状態、つまり、圧力、体積、温度などの新しい変数を、これらの変数のうち 2 つの変更に基づいて決定する必要がある場合に実行されます。
たとえば、ガスの体積がその温度とともに変化する場合、以下で説明する一般的なガス方程式を使用して、ガスが受ける新しい圧力を決定することができます。

P 1 .V 1 = P 2 .V 2
T1T2
この方程式では次のようになります。
T 1 = 瞬間 1 の温度。
T 2 = 瞬間 2 の温度。
P 1 = 瞬間 1 の圧力。
P 2 = 瞬間 2 の圧力。
V 1 = 瞬間 1 の音量。
V 2 = 瞬間 2 の音量。
一般的な気体方程式を使用して計算を実行する場合、変数の圧力、体積、温度はそれぞれ同じ測定単位を持つ必要があります。温度は必須の測定単位を持つ唯一の変数であり、ケルビンで与えられます。
以下に、一般的なガス方程式を使用した計算例をいくつか示します。
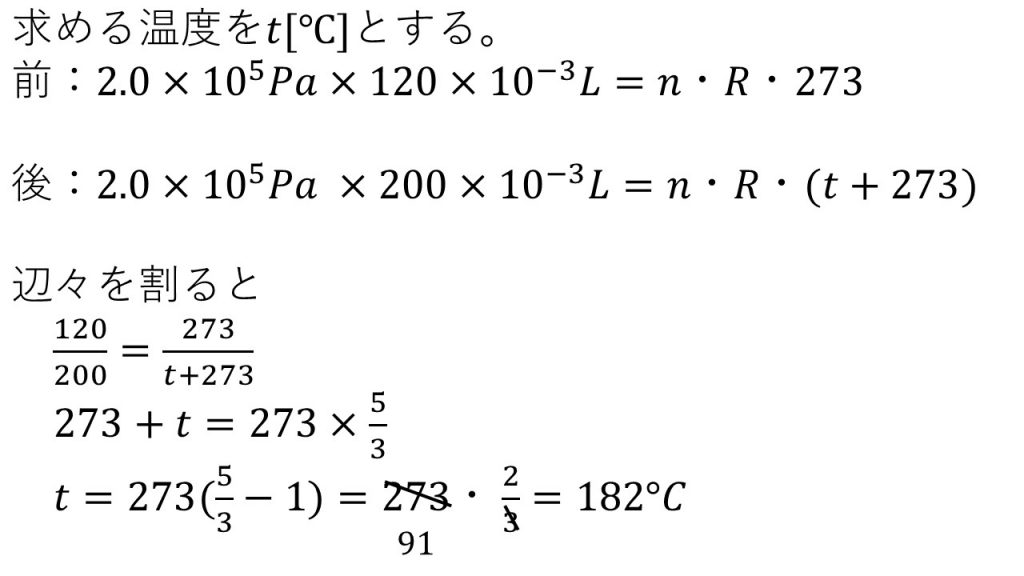
第1実施例−(UFJF−MG) 化学実験室(圧力=600mmHg、温度=300K)において、金属マグネシウムと塩酸との反応が行われ、30mLの水素ガスが生成された。圧力を 800 mmHg に増加し、システムを 400 K の温度に加熱すると、生成される水素の体積は次のようになります。
a) 30 mL。
b) 120mL;
d) 40mL;

e) 20 mL。
演習によって提供されたデータは次のとおりです。
容量 1= 30 mL
2巻 = ?
圧力 1= 600 mmHg
圧力 2 = 800 mmHg
温度 1 = 300 K
温度 2 = 400 K
P 1 .V 1 = P 2 .V 2
T1T2
600.30 = 800.V2
300 400
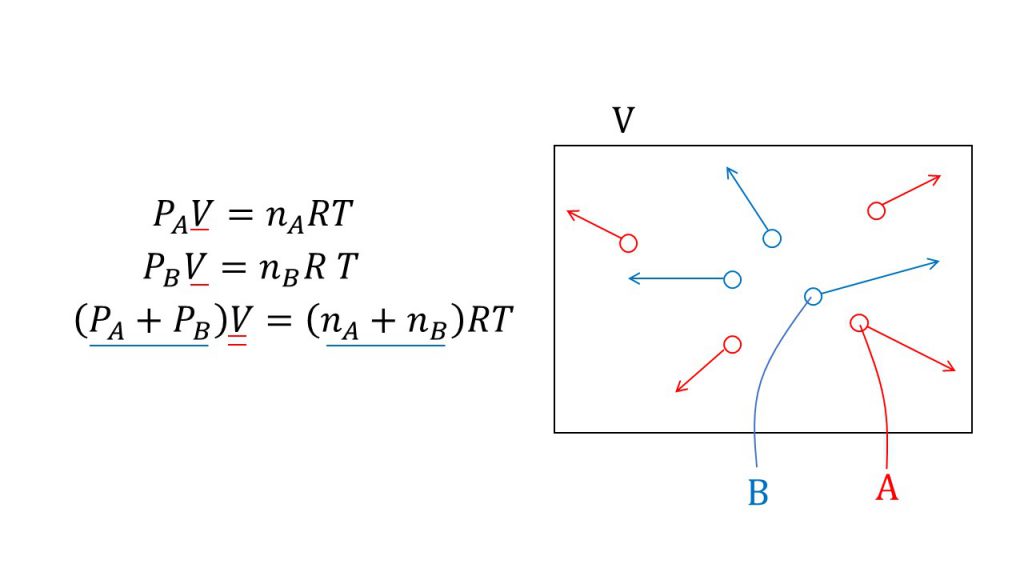
300,800V 2 = 600,30,400
240000V2 = 7200000
V2 = 7200000
240000
V2 = 30 mL

2 番目の例– (UnB-DF) ある質量の水素は、-73 ℃ 、5 気圧で 100 cm 3の体積を占めます。同じ質量の水素が 760 mmHg で 1 L の体積を占めるのに必要な温度を℃で計算します。
演習によって提供されたデータは次のとおりです。
体積 1= 100 cm 3または 0.1 L
容量2 = 1L
圧力1=5気圧
圧力 2 = 760 mmHg または 1 atm (もう一方は atm 単位なので)
温度 1 = – 73 o C または 200 K (温度はケルビンで処理する必要があるため)
温度2 = ?
演習で要求される温度を決定するには、一般的な気体方程式で提供されるデータを使用するだけです。
P 1 .V 1 = P 2 .V 2
T1T2

5.0.1 = 1.1
200T2
0.5.T2 = 200.1.1
T2 = 200
0.5
T2 = 400K

最後に、ケルビン単位で得られた値を °C に変換する必要があります。これを行うには、273 で見つかった結果を単純に減算します。
T 2 = 400-273
T2 = 127 ℃
