金属、特に鉄鋼の腐食により、社会は毎年、多大な経済的および環境的損害を被っています。研究によると、米国だけでも、腐食による損失を補うための年間コストが 800 億ドルに上ります。
腐食とは、主に酸素と水などの自然の物質による金属の酸化です。パイプ、建設構造物、建物、橋、高架橋、産業施設、機械などの金属物の耐用年数が大幅に短縮され、これらの金属をより多く生産する必要が生じるため、経済的損失が生じます。
また、重要な機器の腐食は事故や汚染につながる可能性があるため、この現象は人の命を危険にさらします。
さらに、鉄鋼の製造プロセスには鉱石の探査と、製鉄炉内の酸化鉄を還元するための多大なエネルギー消費が含まれるため、環境に悪影響を及ぼします。
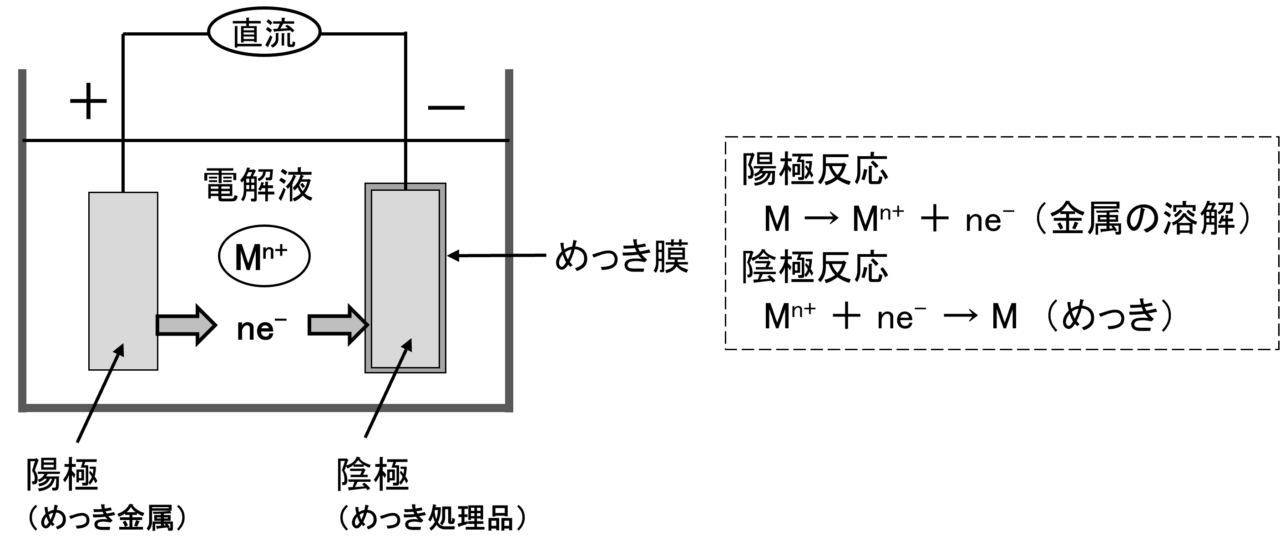
したがって、これらの損失を最小限に抑えるために、金属を保護して腐食を防ぐ取り組みが行われています。鋼の場合、使用される技術の 1 つは亜鉛メッキです。このプロセスでは、鋼が亜鉛でコーティングされ、陰極防食が行われます。このコーティングは 2 つの方法で行うことができます。下の図に示すように、溶融亜鉛に浸漬する方法と、金属を電気メッキする方法です。この最後のプロセスについては、 「ガルバノ形成術」のテキストで詳しく説明されています。この文書では、電気分解プロセスを通じて、陰極上に配置された金属を、陽極上または水溶液中に配置できる別のより貴な金属でコーティングできることが示されています。したがって、このプロセスが金属部品のコーティングに亜鉛を使用して行われる場合、電気めっきは亜鉛めっきとなります。
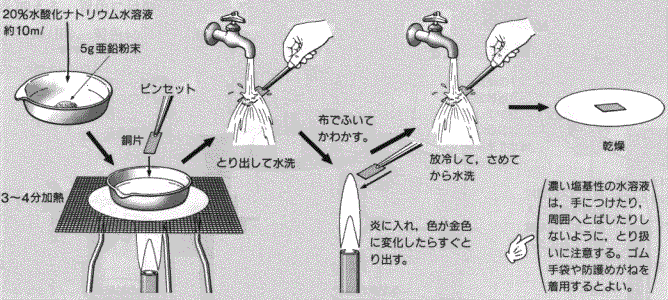
亜鉛めっきの仕組みを理解するために、まず鋼が錆びる原因を見てみましょう。
鋼は、主に鉄で構成される金属合金です(鋼の組成 = Fe(約 98.5%)、C(0.5 ~ 1.7%)、Si、S、O(微量))。鉄は酸素よりも還元電位が低いため、酸化を受けます。
Fe (s) → Fe 2+ + 2e –

条件に応じていくつかの還元反応が発生しますが、錆の形成につながる主な反応は水と酸素の還元反応です。
O 2 + 2 H 2 O + 4 e – → 4 OH –
すでに述べたように、酸素は鉄よりも還元電位が大きいため、酸素が陰極となり、鉄が陽極になります。
陽極: 2 Fe (s) → 2Fe 2+ + 4e –
カソード: O 2 + 2 H 2 O + 4e – → 4 OH – ____
全体反応: 2 Fe + O 2 + 2 H 2 O → 2 Fe (OH) 2
続いて、酸素の存在により、水酸化鉄 (II)、Fe (OH) 2が酸化されて、水酸化鉄 (III)、Fe (OH) 3になります。
4 Fe (OH) 2 + O 2 + 2 H 2 O → 4 Fe (OH) 3
この水酸化物は水分を失い、赤茶色の酸化鉄(III)一水和物、つまり錆びに変化する可能性があります。
2 Fe (OH) 3 → Fe 2 O 3 。 H2O + 2H2O

金属表面は空気中の酸素と接触するため、錆が落ちやすくなり、腐食が促進されます。
したがって、亜鉛めっきの場合、鋼をコーティングする金属亜鉛は鉄よりも優れた還元剤です。これは、その還元電位が -0.76 V であるのに対し、鉄の還元電位は -04 V に等しいためです。亜鉛の還元電位は低いため、酸化電位は高く、酸化するのは鉄ではなく亜鉛です。
このように、亜鉛は鉄の代わりに酸化するため、犠牲金属として機能し、金属構造を無傷に保ちます。
さらに、亜鉛の腐食は鉄よりも遅く、腐食すると Zn(OH) 2の皮膜が形成されますが、この皮膜は錆とは異なり、金属の表面から簡単には剥がれません。実質的に水に溶けません。

しかし、物体に傷がつき、アイロンが空気に触れたままになったらどうなるでしょうか?鉄は酸化されますが、亜鉛も酸化され、酸化の際に生じたFe 2+イオンが金属鉄(Fe)に還元されるため、心配ありません。さらに、露出した鉄の上にZn(OH) 2膜が堆積し、再び保護されます。


