私たちは日常生活の中で、室温では固体状態の物質、液体状態の物質、気体状態の物質があることに気づきます。ある物理状態から別の物理状態に変化するのは、粒子間の相互作用力です。
たとえば、固体状態の粒子は互いに非常に接近しており、動きの自由度がほとんどないため、分子間の引力または分子間力が非常に大きくなります。

そして、この力が大きくなればなるほど、それを破壊して材料の物理的状態を変化させるために必要なエネルギーも大きくなります。
同じ物理的状態にある物質間であっても、異なる分子間力が存在することが注目されています。一例として、アセトン 3 滴と水 3 滴を別々のスプーンに注ぎ、何が起こるかを観察するとします。アセトンは水よりもはるかに早く蒸発することがわかります。これは、アセトンの分子間力が弱いことを意味します。
オランダの物理学者ヨハネス・ファン・デル・ワールスは、1873 年にこれらの力の存在を研究し、提案しました。そのため、それらはファン・デル・ワールス力と呼ばれるようになりました。非極性分子間に存在する分子間力のみが別の科学者、フリッツ・ロンドンによって説明されました。
3 つの分子間力は次のとおりです。
1. 誘起双極子誘起双極子力 (ファンデルワールス力、結合、またはロンドン分散力とも呼ばれます):
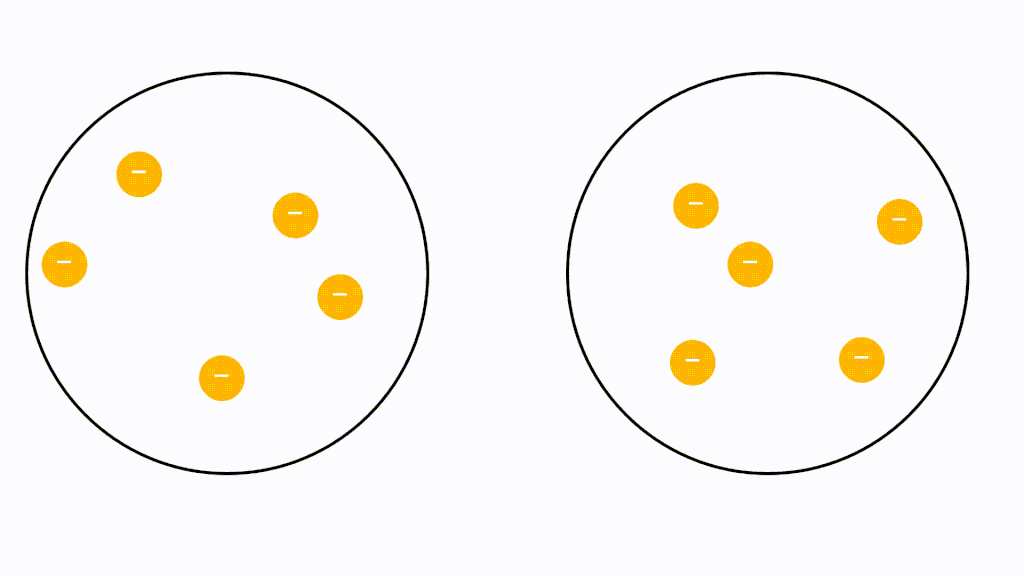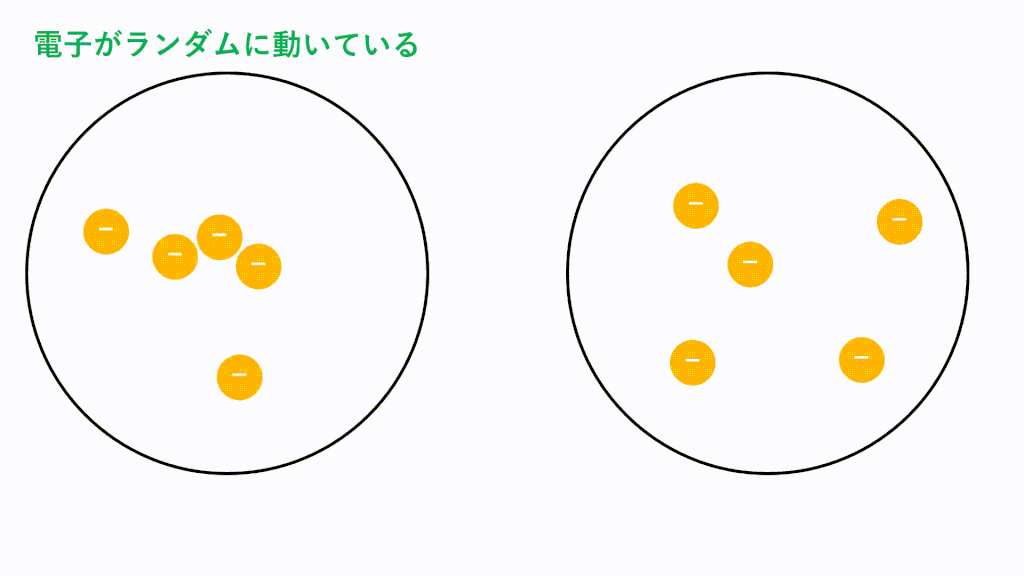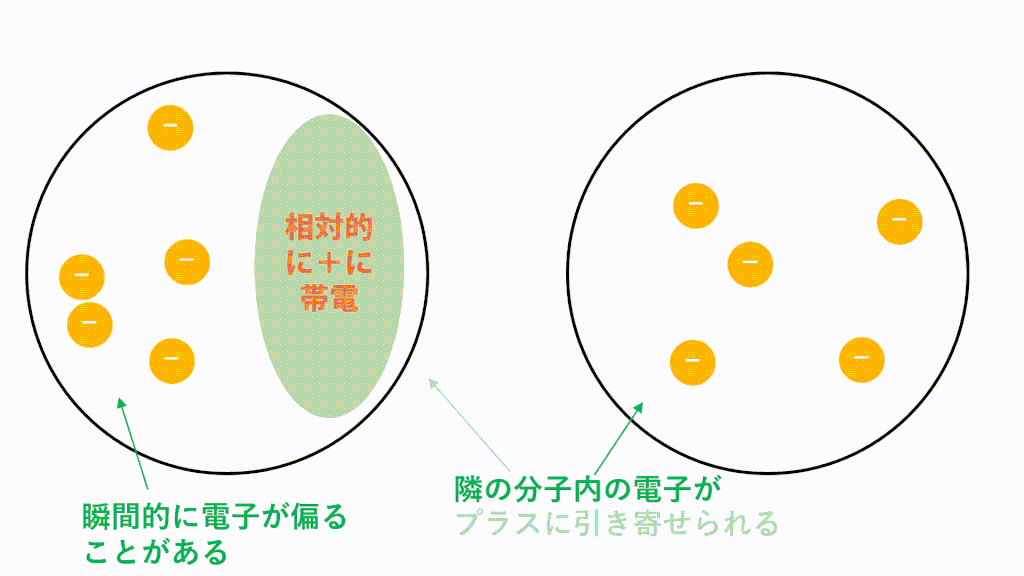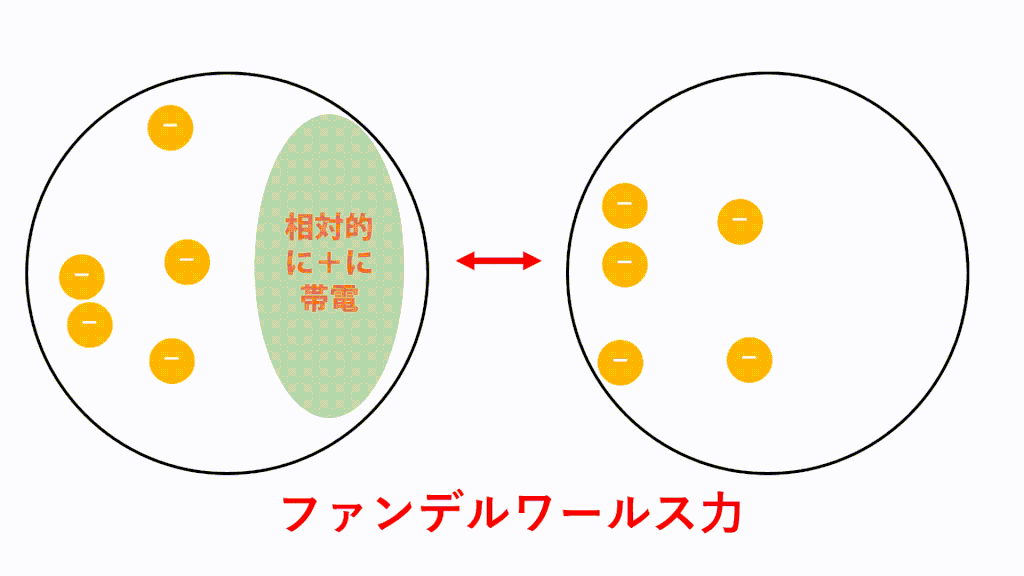
それは非極性分子で起こります。一定の瞬間に、一定の運動をしている非極性分子の電子は、一方の側にもう一方の側よりも多くの電子を持ち始め、その結果、瞬間的に分極されます。このようにして、電気誘導を通じて、隣接する分子を分極させます。つまり、誘導双極子を作成します。以下の非極性ヨウ素分子 (I2) の例を参照してください。
これは電子の動きだけでなく、分子の衝突によっても起こります。これはすべての分子間結合の中で最も弱い結合です。
2. 永久双極子-永久双極子または双極子-双極子力:
これは、一方の端がプラスでもう一方の端がマイナスである極性分子で発生し、下に示すように永久電気双極子を作成します。HCl 分子の場合、プラスの部分が隣接する分子のマイナスの部分を引き付けるなど、の上。 :

。
3. 水素結合:
これは、分子内の水素が他の小さくて強い電気陰性原子、主にフッ素、酸素、窒素と結合するときに発生します。例としては水があります。ある分子の水素 (部分的にプラスに帯電) は、隣接する別の分子の酸素 (部分的にマイナスに帯電) に引き寄せられます。

これはすべての分子間力の中で最も強いものです。このようにして、以下が得られます。
| インタラクション強度の昇順: |
| 誘起双極子 – 誘起双極子<双極子間双極子<水素結合 |
このテーマに関するビデオレッスンをぜひご覧ください。



