イオン結合:電子の移動によりイオン間に生じる結合です。これは、マイナスイオン (アニオン) とプラスイオン (カチオン) のイオン間の静電引力の存在によって形成されます。
イオン性化合物の最も一般的な例は、食卓塩である塩化ナトリウム (NaCl) です。ナトリウム原子 (Na) は安定ではありません (原子価殻に自由電子が 1 つあります)。安定性は、電子を 1 つ失った場合にのみ達成され、Na+ カチオンが生じます。塩素原子 (Cl) も Na と同じ理由で不安定であり、電子を獲得して Cl- イオンを生成する場合にのみ安定に達します。イオンがすでに形成されており、電子的に安定している場合は、静電相互作用、つまり以下の方程式で表すことができるイオン結合が存在します。

Na ++ Cl – → NaCl
金属結合:金属の原子構造は結晶であり、電子に囲まれた金属カチオンで構成されています。金属に存在する結晶格子は次の図で表すことができます。
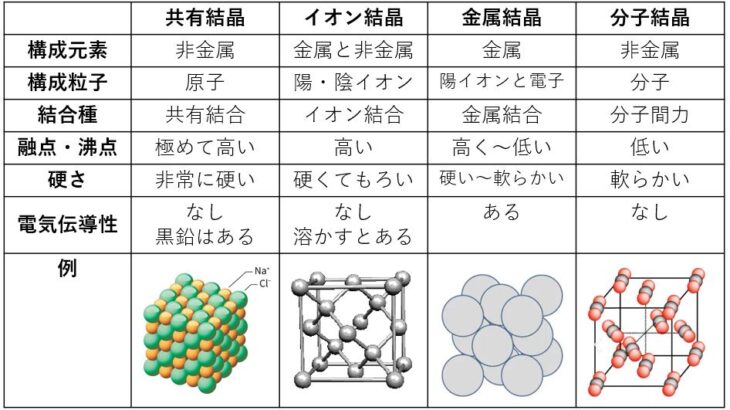
金属の結晶格子は、電子に囲まれた固定陽イオンのグループによって形成されます。電子は非局在化されており、どの原子核にも引き寄せられません。
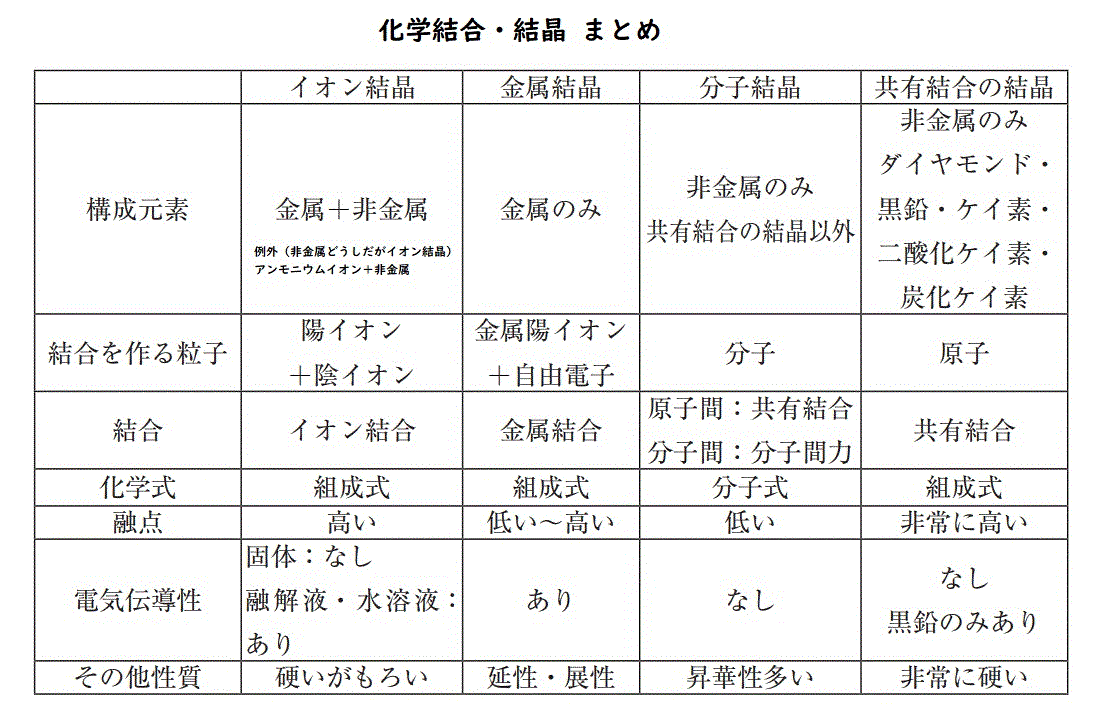
共有結合:この結合では、電子の共有により原子が結合され、円で示される電子ペアが作成されます。
2 つの塩素 (Cl) 原子の分子共有結合

形成された各電子対は同時に両方の原子に属します。電子の獲得も喪失もなく、共有するだけなので、分子は電気的に中性の構造です。
関連するビデオレッスン:


