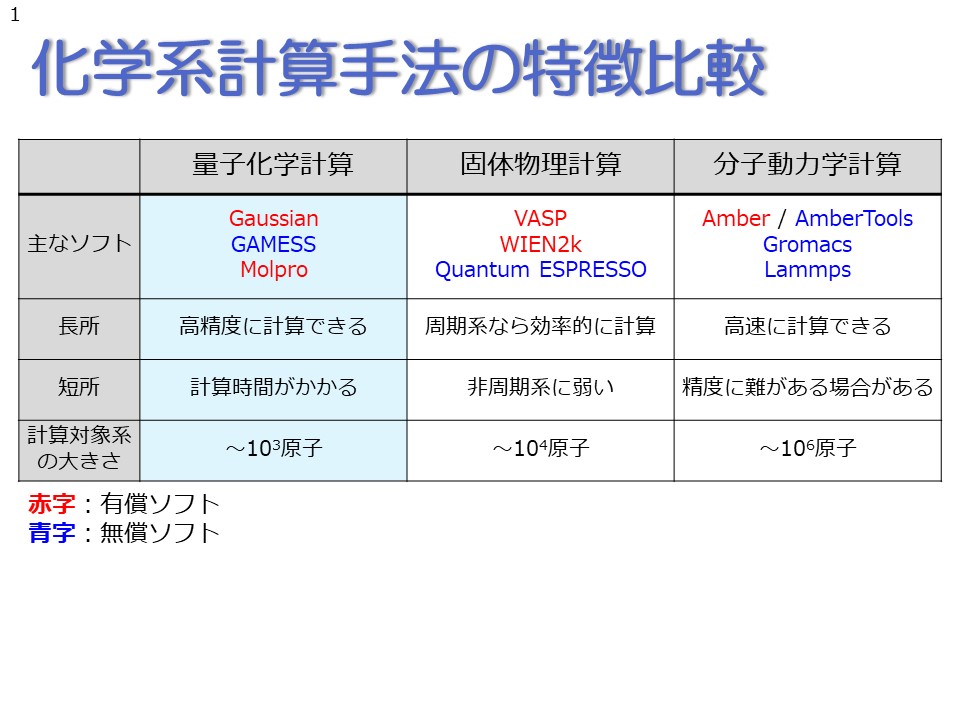
化学元素は、同じ原子番号 (Z)を持つ原子、つまり原子核内の同じ数の陽子によって形成されるグループです。特定の元素の原子が基底状態にあるとき、その原子は中性であるため、陽子 (正の電荷をもつ粒子) と電子 (負の電荷をもつ粒子) の数は等しくなります。
原子番号 = 陽子 = 電子
Z = P = e –

原子核内に存在する陽子と中性子の数の合計は質量数と呼ばれ、文字Aで表されます。
A = P + NまたはA = Z + N
したがって、化学元素は通常、記号の上部に質量数、下部に原子番号を配置して表されます。
Z A X またはZ X A
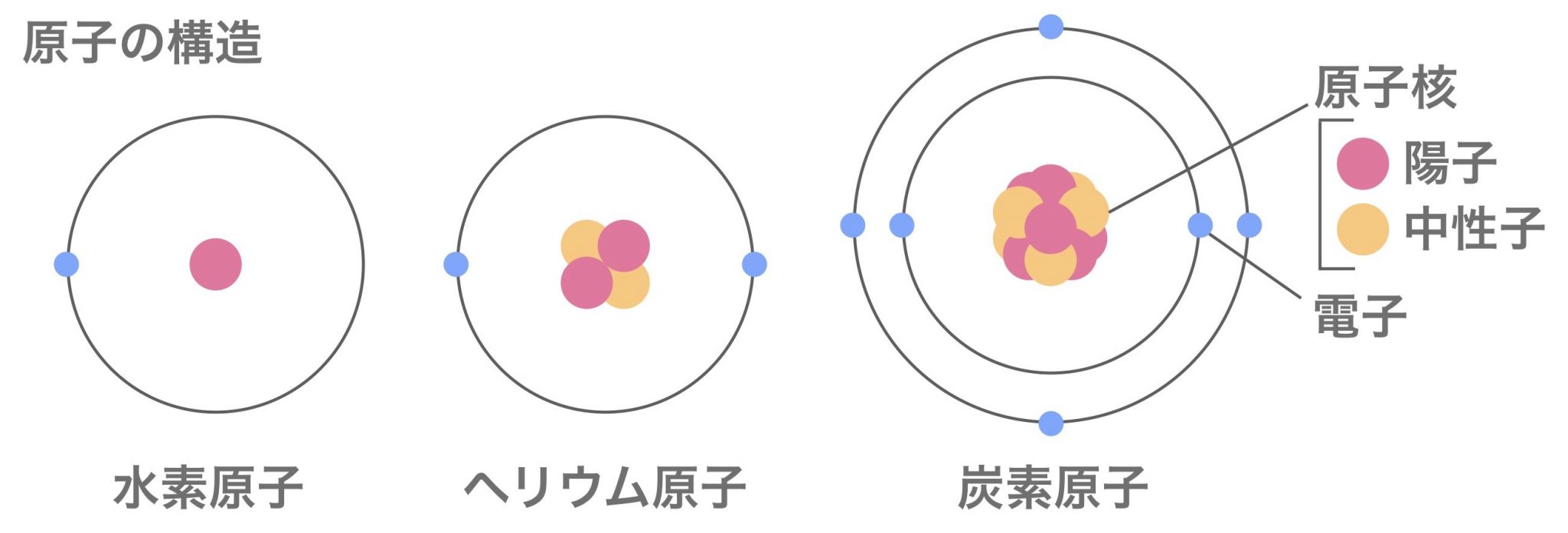
例: 21 45 Sc
この表現は、スカンジウム (Sc) が Z = 21 または 21 個の陽子と 21 個の電子に等しい原子番号を持っていることを示しています。さらに、その質量数は A = 45 であり、以下の計算に示すように、24 個の中性子があると結論付けられます。
A = P + N
N = A – P
N = 45 – 21
N = 24
元素の原子が電子を失ったり電子を獲得した場合、それはイオンになり、その電荷は上部の右側にZ A X電荷として表される必要があります。原子が電子を失っている場合、その原子は正の電荷を持ち、カチオンになります。逆に電子を受け取るとマイナスの電荷を持ち、陰イオンになります。
イオンが関係する場合の原子粒子の計算方法の例を参照してください。
「イオン11 23 Na 1+が持つ陽子、中性子、電子の数を書きなさい。」
解決:
見ただけで、次のことがすでにわかります。
A = 23
Z = 11
Z = P なので、陽子は 11 個あります。中性子の数を調べるには、次の計算を行います。
A = P + N
N = A – P
N = 23 – 11
N = 12
次に、原子がイオンになるときに変化する唯一の粒子である電子を発見する必要があります。この場合、カチオンの電荷は +1 であり、電子が 1 つ失われたことを意味します。基底状態では、11 個の電子 (これは陽子の数と同じです) を持っていましたが、電子が 1 つ失われたため、このイオンは10 個の電子を持っています。
このテーマに関するビデオレッスンをぜひご覧ください。
