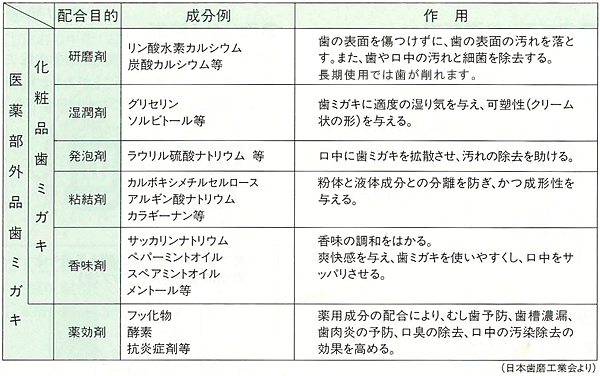
歯磨き粉は歯の健康を維持するために不可欠な製品であり、虫歯と闘うだけでなく、歯石や細菌性プラークと闘い、さらには歯を白くするのにも役立ちます。
しかし、これらすべての機能を可能にする歯磨き粉に含まれる物質は何でしょうか?
まず、歯の化学的性質について詳しく見てみましょう。歯のエナメル質の主成分はヒドロキシアパタイトで、分子式Ca 5 OH(PO 4 ) 3(s)の塩です。この塩は硬く、水にほとんど溶けませんが、酸によって攻撃される可能性があります。
水性媒体中にあるヒドロキシアパタイトは、唾液により、以下の化学式に従ってイオンと平衡状態になります。ハイドロキシアパタイトの溶解は脱灰と呼ばれます。そしてその逆のプロセスである石化。
私たちの口の中に酸が存在すると、H +イオンが生成され、これがヒドロキシル (OH – ) と反応し、上記の反応の平衡状態が直接反応にシフトします。これは、脱灰が促進され、ハイドロキシアパタイトがより多く消費され、歯のエナメル質が弱くなることを意味します。
酸の存在は主に 2 つの方法で発生します。1 つ目は、酸性の食べ物や飲み物 (ソフトドリンクなど) の摂取によるものです。環境が酸性になる別の方法は次のとおりです。私たちの唾液にはタンパク質が含まれており、歯の上に目に見えない層を形成します。この層には細菌が蓄積しており、これを細菌プラークまたはバイオフィルムと呼びます。私たちが糖分やタンパク質を食べると、細菌もそれらを食べて代謝し、歯を攻撃する酸を放出し、エナメル質を溶かして虫歯を引き起こします。
このヒドロキシアパタイトの脱灰プロセスに対抗するために、歯磨き粉のパッケージにはフッ化物 (F) が含まれていると記載されることがよくあります。しかし実際には、この用語は正しくありません。なぜなら、すべての歯磨き粉には、モノフルオロリン酸ナトリウム (Na 4 (PO 4 )F) やフッ化ナトリウム (NaF) などの塩として含まれるフッ化物イオン (F 1 – ) が含まれているからです。

フッ化物の存在は重要です。フッ化物にはヒドロキシアパタイト内のヒドロキシルイオン(OH – )を置き換えて化合物フルオロアパタイトを形成する特性があるためです。フッ素アパタイトは水にさらに溶けにくく、歯のエナメル質を酸による攻撃に対してより耐性のあるものにします。解離時に形成される:
酸性環境は虫歯の形成を促進するため、一部の歯磨き粉には、重炭酸ナトリウムや水酸化マグネシウムなど、口の酸性度を下げる特定の塩基も含まれています。
したがって、正しく歯磨きするときにデンタルフロスと歯磨き粉を使用すると、形成される細菌性歯垢が除去され、歯垢が除去されなかった場合に生じる歯上の無機塩の沈着である歯石が防止されます。歯石は歯みがきだけでは除去できない硬い構造になっているため、歯科医院での治療が必要になります。
マーケティングで強調されている虫歯予防作用は、フッ化物イオンの存在によるものです。抗歯石作用は、過酸化物またはピロリン酸の存在によって達成されます。そして、これまで見てきたように、歯垢には細菌が含まれているため、抗歯垢作用のある歯磨き粉には抗菌物質が含まれています。ホワイトニング作用は過酸化水素の存在によるものです。
歯磨き粉のもう一つの興味深い点は、それが作る泡であるため、シャンプー、合成洗剤、石鹸、石鹸などの泡を生成する他の製品と同様に、洗剤とみなされます。この泡は、その組成物中にラウリル硫酸ナトリウムが存在することによって生じます。その式を以下に図示します。

H3C ─ CH 2 ─ CH 2 ─ CH 2 ─ CH 2 ─ CH 2 ─ CH 2 ─ CH 2 ─ CH 2 ─ CH 2 ─ CH 2 ─ CH 2 ─ OSO – 3 Na +


