「水のイオンバランス」のテキストに示されているように、その分子は自己イオン化を起こし、ヒドロニウム (H 3 O + (aq) ) およびヒドロキシル (OH – (aq) ) イオンを生成します。
H 2 O (l) + H 2 O (l) ↔ H 3 O + (aq) + OH – (aq)

水の電気分解は、これらのイオンが電極で放電するときに発生します。ただし、この自動イオン化では、電流を流し、継続的に放電するのに十分な量のイオンが生成されません。
したがって、水の電気分解を実行できるようにするには、水に可溶で、ヒドロニウム ( H 3 O + (aq) ) やヒドロキシル ( OH – ( aq) )イオン。これは、金属の反応性(電気陽性)が高いほど、電子を供与する傾向が大きくなり、電子を受け取る傾向が低くなるためです。したがって、反応性の低い金属カチオンが最初に放電します。
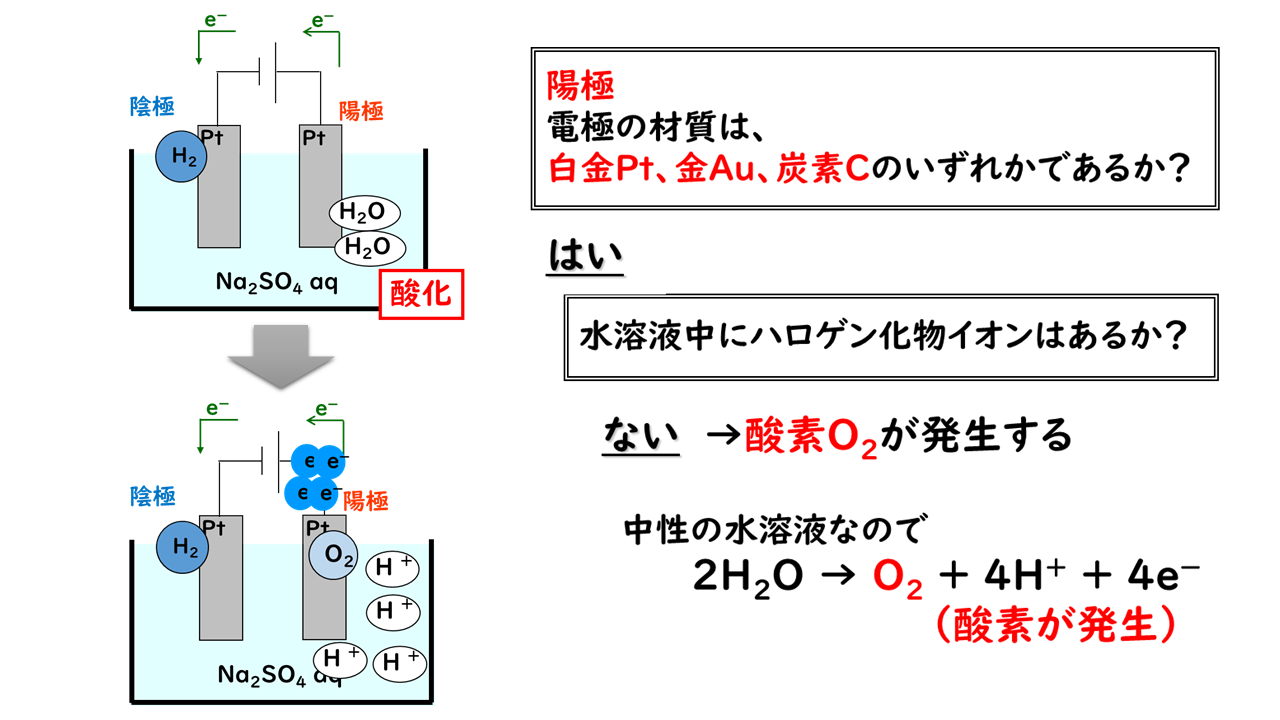
アニオンに関しては、アニオンを形成する元素の電気陰性度が高いほど、電子を引き付ける傾向が大きくなり、電子を供与する傾向は低くなります。したがって、電気陰性度の低い非金属陰イオンが最初に放電します。
使用できる電解質の例としては、硫酸 (H 2 SO 4 )、水酸化ナトリウム (NaOH)、および硝酸カリウム (KNO 3 ) があります。

これらの物質が水からのイオンの放出を可能にすることは、 「水性媒体中の電気分解」の本文で、陽イオンと陰イオンの放出の容易さの降順を示す 2 つの表が提供されているためです。
最初の表によると、ヒドロニウム カチオン (H 3 O + (aq) ) を、それぞれ水酸化ナトリウム (NaOH) および硝酸カリウム (KNO 3 ) によって供給される Na +および K +カチオンと比較すると、次のことがわかります。これらのカチオンはヒドロニウムよりも反応性が高いため、電極で最初に放電されます。

陰イオンを分析すると、SO 4 2-陰イオン (硫酸によって供給される) と NO 3 – (硝酸カリウムによって供給される) 陰イオンが水中のヒドロキシルよりも反応性が高く、最初に放出されることがわかります。
硝酸カリウム塩が水に溶解してイオンを生成する電気分解の例を見てみましょう。

塩の解離: 1 KNO 3 → 1 K + + 1 NO 3 –
水の自動イオン化: 8 H 2 O → 4 H 3 O + + 4 OH –

前述したように、K + はH 3 O +よりも反応性が高くなります。これは放電しやすく、前者は OH –よりも反応性が高いため、放電しやすくなります。
したがって、水中の H 3 O + は負極 (カソード) で還元され、水素ガスH 2が生成されます。水の OH –アニオンは、正極 (アノード) で酸化を受け、酸素ガスO 2を生成します。

カソード半反応: 4 H 3 O + + 4 e – → H 2 O + H 2
アノード半反応: 4 OH – → 2 H 2 O + 1 O 2 + 4 e –
このプロセス全体を合計すると、次のような全体的な方程式が得られます。

塩の解離: 1 KNO 3 → 1 K + + 1 NO 3 –
水のイオン化: 8 H 2 O → 4 H 3 O + + 4 OH –
カソード半反応: 4 H 3 O + + 4 e – → 4 H 2 O + 2 H 2
アノード半反応: 4 OH – → 2 H 2 O + 1 O 2 + 4 e –
全体的な方程式: 2 H 2 O → 2 H 2 + 1 O 2
塩は反応に関与せず、そのイオンは同じ初期濃度で水中に遊離したままであるため、全体的な方程式に塩を記述しませんでした。それは、電流を流し、水の電気分解を促進することのみを目的として機能しました。
