電気分解は、液体状態、溶融状態、または水性媒体中の物質に電流を流すことによって、電気エネルギーを化学エネルギーに変換するプロセスです。このプロセスでは、使用される電極は不活性または活性の場合があります。
最も一般的に使用される不活性電極はグラファイトと白金であり、これらは酸化還元反応には関与せず、電子のみを伝導します。

非不活性電極または活性電極の場合、酸化と還元が起こり、化学反応に関与します。
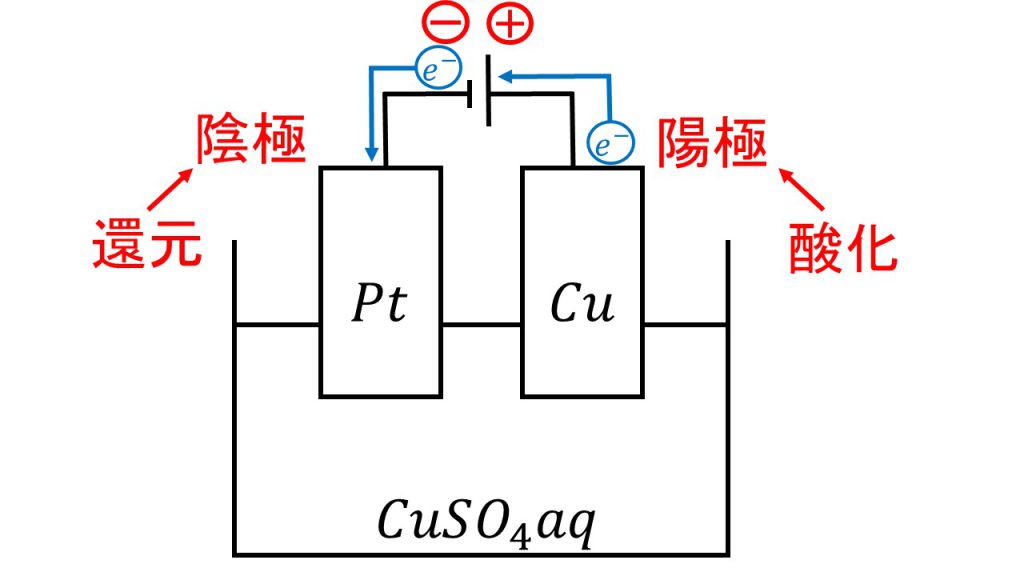
活性電極の使用の最も重要な例は、銅の電解精製です。冶金用銅は通常、非純粋なカルコサイト (Cu 2 S) 鉱石から得られます。しかし、特に電線に使用するには、電気分解による高純度(99.9%)が必要です。
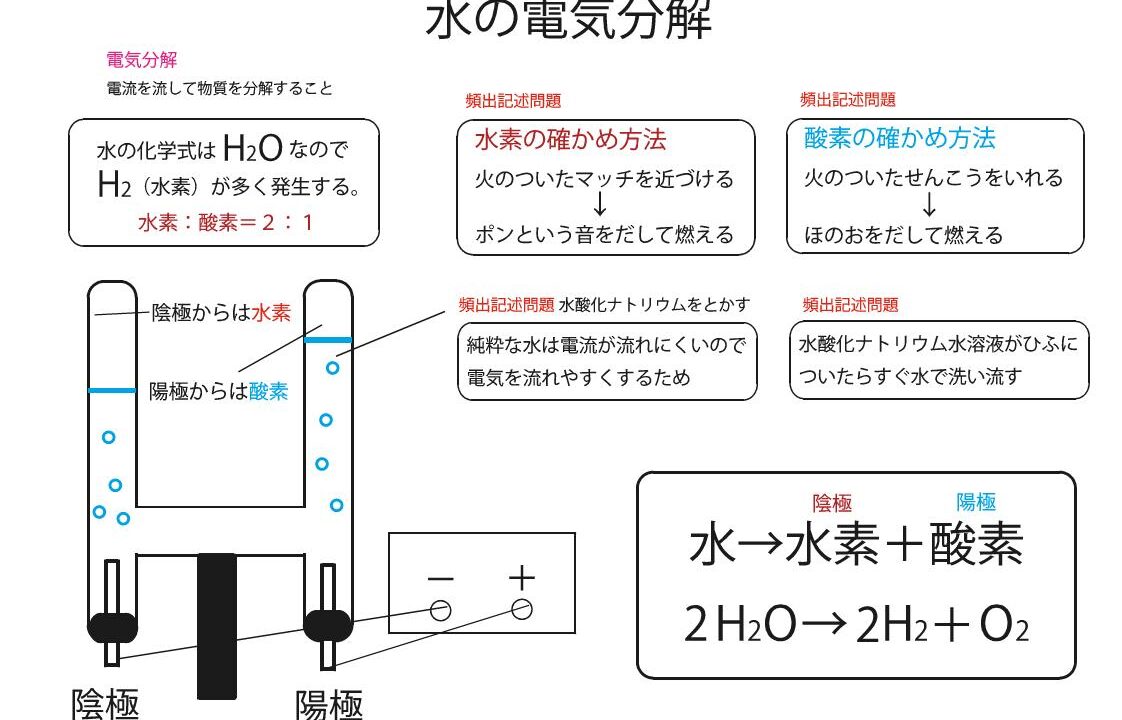
これは、純度の高い銅板を陰極 (電解負極) に置き、不純な銅板を浄化したい陽極 (陽極) に配置します。両方とも硫酸銅 (CuSO 4 ) の溶液に浸されます。
次に、アノードの酸化が発生し、各銅原子が 2 つの電子を失い、Cu 2+イオンが環境中に放出されます。アノードによって放出された Cu 2+イオンと溶液中に存在する Cu 2+イオンの両方がアノードに引き寄せられ (カソードはマイナスで反対の電荷が互いに引き合うため)、還元はカソードで起こり、この電極上に堆積します。 。
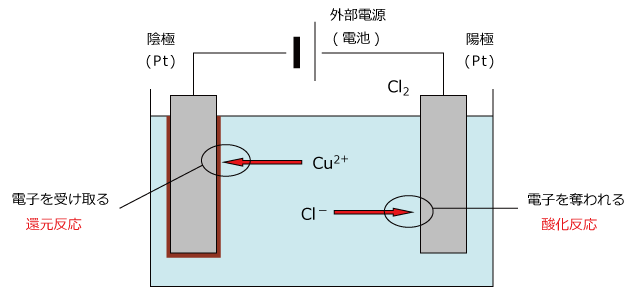

各電極での半反応は次のとおりです。

アノード半反応: Cu 0 (s) → Cu 2+ (aq) + 2e-
カソード半反応: Cu 2+ (aq) + 2e- → Cu 0 (s)
世界的な反応: ゼロ
実際には化学変化は起こらず、アノードからカソードへの銅の輸送のみが発生したため、全体的な反応の結果はゼロに等しくなります。このようにして、負極 (カソード) で精製された銅が得られます。

