化学元素はそれぞれ、同じ原子番号を持つ 1 つ以上の原子、つまり原子核内の同じ数の陽子によって形成されます。たとえば、元素の水素は原子番号 1 の原子で構成され、酸素は原子番号 8 の原子で構成されます。
しかし、これらの元素(同じまたは異なる)が結合してイオン分子またはクラスター(イオンは電荷を持った原子または原子のグループ)を形成し、純粋な物質を形成することがあります。
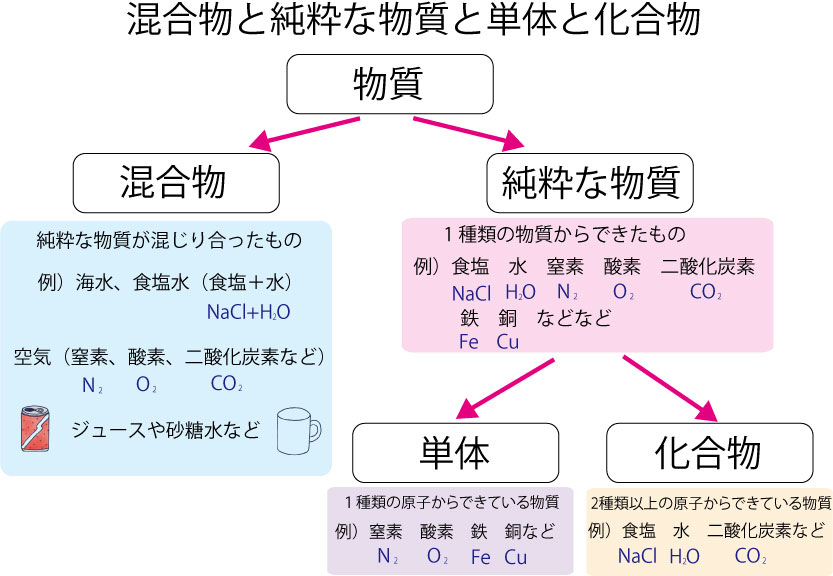
たとえば、酸素原子に 2 つの水素原子が結合すると、水の化学物質である分子式 H 2 O で表される分子が形成されます。純粋な物質の別の例は、食塩の主成分である塩化ナトリウム (NaC?) です。水の場合のように分子によって形成されるのではなく、電気的に結合した非常に多くの正イオン (Na + ) と負イオン (C? – ) のクラスターによって形成されます。
純粋な物質は次のように定義できます。
?
たとえば、蒸留水は、等しい H 2 O 分子のみで構成されていることに加えて、一定の特性を備えているため、純粋な物質です。海面 (1 気圧下) では、融点は 0 ℃、沸点は 100 ℃、密度は 4 ℃で 1.0 g/mL です。これらの特性は、サンプルの量に関係なく、純水では常に同じです。
純物質には、単体と複合物質の 2 種類があります。
たとえば、酸素ガスは O 2分子、つまり酸素元素の原子のみによって形成されます。以下の単体物質の他の例を参照してください。
一例は、水素と酸素という 2 種類の元素の原子で形成されている前述の水そのものです。以下に、化合物とも呼ばれる複合物質の例をさらに示します。
しかし、自然界に見られる物質の大部分は、純粋な単純物質や複合物質ではなく、物質の混合物です。たとえば、ミネラルウォーターは水 (H 2 O) だけで構成されているのではなく、パッケージラベルに記載されているように、いくつかの溶解ミネラルが含まれています。海水も主に塩化ナトリウムを中心としたさまざまな塩の混合物ですが、ミネラルウォーター、川水、水道水などとは組成が異なります。いずれの場合も、混合物が存在します。
混合物は次のように定義できます。
混合物には均一なものと不均一なものがあります。詳細については、以下のテキストをお読みください。
このテーマに関するビデオレッスンをぜひご覧ください。






