数学では、分数は (1 つ以上の整数の) 全体の一部を表すものであると学びました。たとえば、ピザが 5 つに分割されている場合、あなたがそのうちの 3 つを食べ、あなたの友人が残りの 2 つを食べた場合、これは、あなたがピザの 3/5 を食べ、友人がその 2/5 を食べたことを意味します。 。これらの分数の合計はピザ全体に相当します。
3 + 2 = 5 = 1
5 5 5

物質量における分率 (モル分率とも呼ばれます) の形での化学溶液の濃度の場合、この量は物質の量 (モル数) 間の関係に対応するため、同様の推論が続きます。溶液全体中の物質の量に関連した溶質または溶媒。
したがって、次のようになります。
溶質のモル分率 =溶質(または溶媒)中の物質の量
溶液中の物質の量
∕\
x 1 = n 1またはx 2 = n 2
ん、ん
ここで、「x」は物質量の分数を表す記号、「n」はモル数を表す記号です。化学溶液の濃度のすべての計算では、従来、溶質を表すインデックス「1」、溶媒を表すインデックス「2」を使用し、溶液全体を表すインデックスは使用しませんでした。

溶液全体に含まれる物質の量 (n) の値は、溶質と溶媒に含まれる物質の量を加算することで求められます。
n = n 1 + n 2
したがって、上記のモル分率の式は次のように置き換えることができます。
x 1 = ___n 1___またはx 2 = ___n 2___
n 1 + n 2 n 1 + n 2
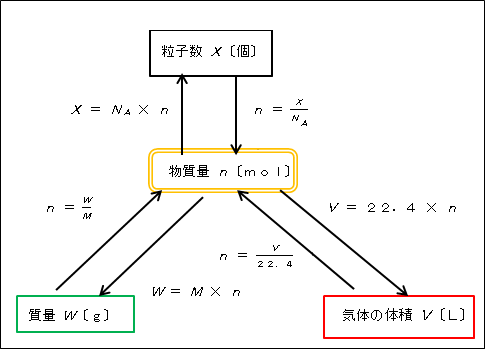
また、一般にモル数は示されず、使用された溶質と溶媒の質量がグラム単位で示されることにも注意してください。以下の式に示すように、これらの質量を通じて物質の量を知ることができます。
n = m (グラム単位の質量)
M (モル質量)
例を考えてみましょう。
38gの塩化カルシウムを36gの水に溶解することによって溶液を調製した。この溶液中の溶質のモル分率は何ですか?
解決:
データ:
× 1 = ? (それが私たちが知りたいことです)
n1 =?
n 2 = ?
n = ?
m1 =38g
平方メートル= 36g
* まず、溶質と溶媒 (n 1と n 2 ) 中の物質の量をそれぞれの質量から調べる必要があります。

* 溶質のモル数: * 溶媒のモル数:
n 1 = m 1 n 2 = m 2
M1M2
n 1 = 38 g n 2 = 36 g
M1M2
塩化カルシウム (CaCl 2 ) と水 (H 2 O) のモル質量は、周期表の各元素の原子質量の値を参照し、次の計算によって計算できます。
Ca Cl 2 H 2 O
M1 = 1。 40.1 + 2。 35.5 = 111.1 g/mol M 2 = 2。 1 + 1 。 16 = 18 g/mol
式に代入すると次のようになります。
* 溶質のモル数: * 溶媒のモル数:
n 1 = 38 g n 2 = 36 g
111.1 g/mol 18 g/mol
n 1 = 0.34 モルn 2 = 2 モル
n = n 1 + n 2
n = 0.34 + 2
n = 2.34 モル
これで、これらの値をモル分率の式に代入して、この溶液中の溶質のモル分率を見つけることができます。
x 1 = n 1
n
× 1 = 0.34 モル
2.34モル
× 1 = 0.14
質問にはありませんでしたが、溶媒のモル分率を知りたい場合は、それを式にも適用するだけです。
X2 = n2
n
× 2 = 2.0 モル
2.34モル
x2 = 0.86
この例を通じて、次の 2 つの重要な点がわかります。
- モル分率 (x) には単位がありません。
- 溶液のすべての成分のモル分率の合計は常に 1 に等しくなります: x 1 + x 2 = 1。
これがどれほど真実であるかは次のとおりです: 0.14 + 0.86 = 1。
すべての参加者が液体または気体である混合物についても同じ計算を行うことができます。
