2 つの原子が共有結合 (電子対を共有すること) で結合すると、より安定性が高まります。これは、この結合を形成する際に、一重、二重、三重のいずれであってもエネルギーを環境に放出することを意味します。したがって、化学結合の形成は発熱プロセスであり、エンタルピー変化は負になります (ΔH < 0)。
逆もまた真です。つまり、共有結合を切断するには、原子にエネルギーを供給する必要があります。原子はより不安定な孤立状態に戻るため、結合の切断にはエネルギーの吸収が伴います。これは、正のエンタルピー変化 (ΔH > 0) を伴う吸熱プロセスです。

共有結合の形成時に放出されるエネルギーは、実際には測定できません。しかし、絆を解く際にエネルギーは吸収されます。この吸収されたエネルギーは結合エネルギーと呼ばれます。
したがって、次のように定義できます。
たとえば、1 モルの水素ガス (2 つの水素原子の間) の単結合を切断すると、437 kJ が吸収されます。

H 2(g) → 2 H (g) ΔH = +435 kJ
次の例に示すように、二重結合および三重結合の結合エネルギーも決定できます。
- 二重結合切断: O 2(g) → 2 O (g) ΔH = +497.8 kJ
O = O (g) → 2 O (g) ΔH = +497.8 kJ
- 三重結合切断: N 2(g) → 2 N (g) ΔH = +943.8 kJ
N≡N (g) → 2 N (g) ∆H = +943.8 kJ
二重結合または三重結合のエネルギーは単結合のエネルギーの倍数ではないことに注意することが重要です。これらの値は、それぞれ 1 モルの二重結合と 1 モルの三重結合を切断するのに必要なエネルギーに対応します。

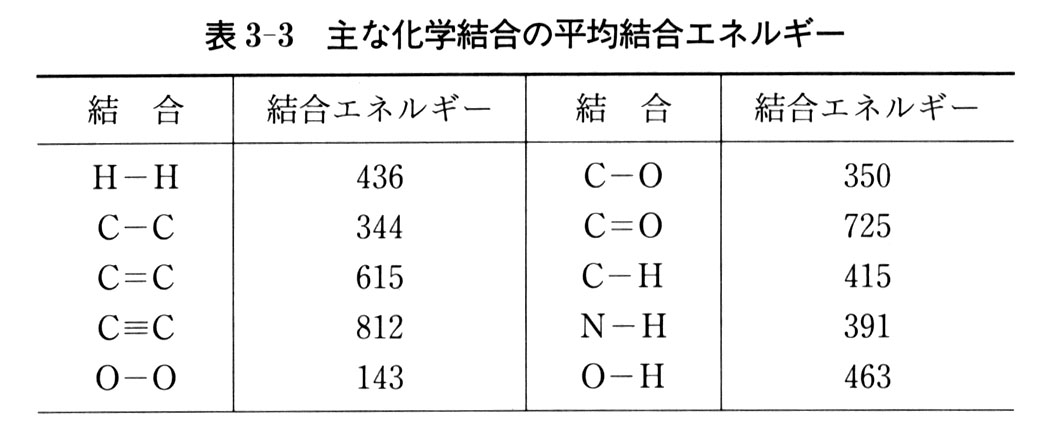
以下に、いくつかの結合エネルギーの測定値を示します。
結合エネルギーが高いほど、原子間の結合は強くなります。
これらの値はすべて、結合を切断するためにすべてのエネルギーが使用されるため、気体状態での反応で得られます。別のケースでは、このエネルギーの一部は物理的状態を変化させるために使用される可能性があります。
複合物質にも同じ原理が当てはまります。たとえば、1 モルの水の結合が切れると、927 kJ が吸収されます。
H 2 O (g) → O 2 (g) + 2 H (g) ΔH = +927 kJ
1モルの水には2つのO─H結合があります。上の結合エネルギーの表を見ると、この結合の各切断は 463.5 kJ に等しいことがわかります。したがって、水の総結合エネルギーは、すべての結合エネルギーの合計になります。
2 (O─H) = 2 mol. 463.5 kJ/モル = 927 kJ
別の例はメタン (CH 4 ) です。
CH 4(g) → C (g) + 4H (g) ΔH = +1653.6 kJ
この場合、C─H 結合が 4 回連続して切断されました。実際には、これらの破断ごとに異なる値が見つかり、合計すると 1653.6 kJ になります。したがって、CH 結合を切断する結合エネルギーは平均値で、約 413.4 kJ に等しくなります。
結合エネルギーの値を通じて、反応のエンタルピーの変化を決定することができます。その方法については、「 結合エネルギーによる反応エンタルピー」のテキストを読んでください。



.jpg)