セルとバッテリーは、化学エネルギーを電気エネルギーに変換できる装置であり、これにより特定の電気装置が動作します。
これらのデバイスの違いは、セルには 2 つの電極と電解質があるのに対し、バッテリーは直列に接続された複数のセルで構成されていることです。
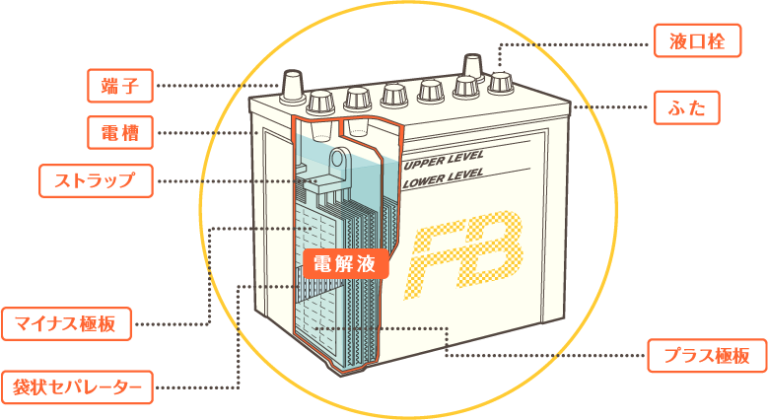
日常生活で最もよく知られ、最も一般的なバッテリーの 1 つは、自動車で使用される鉛バッテリーまたは蓄電池です。通常、このバッテリーは 12 V で、それぞれ 2 V の 6 つのセルのセットで構成されます。
アノードまたはマイナス極は鉛 (Pb) 電極であり、酸化して電子を失います。カソード、正極は酸化鉛 IV (PbO 2 ) です。 Pb プレートはマイナス コネクタに接続され、PbO 2でコーティングされたリード プレートはプラス コネクタに接続されます。これらを厚紙またはプラスチックで隔てて交互に置き、濃度約 30%、密度 1.28 g/cm 3の硫酸 (H 2 SO 4 ) 溶液にすべて浸漬します。
これらの電池で起こる各電極での半反応と全体の反応は次のとおりです。
アノード半反応: Pb +HSO 4 1- + H 2 O ↔ PbSO 4 + H 3 O 1+ + 2e –
カソード半反応: PbO 2 + HSO 4 1- + 3H 3 O 1+ + 2e – ↔ PbSO 4 + 5 H 2 O_______

全体の反応: Pb + PbO 2 + 2 HSO 4 1- + 2 H 3 O 1+ ↔ 2 PbSO 4 +4 H 2 O
以下は、動作しなくなった開いたバッテリーの画像です。バッテリーの隣に、前から後ろに、正極板、セパレーター、負極板が表示されます。
時間の経過とともに硫酸が消費されるため、溶液の密度が減少することに注意してください。したがって、バッテリーが放電しているかどうかを観察する 1 つの方法は、比重計を使用して硫酸溶液の密度を測定することです。密度が 1.2 g/cm 3に等しい場合、実際には帯電していません。
セルとバッテリーを区別するもう 1 つの要素は、最初のセルは充電可能ではなく、反応が終了すると役に立たなくなることです。ただし、バッテリーは充電可能です。
鉛バッテリーで起こる反応は可逆的ですが、自発的ではないことに注意してください。したがって、反応の方向を逆転させ、バッテリーを再充電して硫酸の大部分を再生したい場合は、極を反転する電位差を加えて、直流電流を通じてシステムにエネルギーを供給する必要があります。これは通常、自動車のダイナモまたはオルタネーターによって行われます。

このタイプのバッテリーには、保管、輸送、電解液のメンテナンス、取り扱いなどの点でいくつかの欠点があります。ただし、鉛/酸バッテリーは電圧が最も高く、低コストで電気エネルギーを生成し、厳しい充放電に対する耐性が非常に高いため、これらの欠点は克服されます。



