酸化還元反応は、電子の喪失と獲得が同時に起こることを特徴としています。たとえば、塩酸の入った容器にマグネシウムリボンを置いたときに起こる反応を考えてみましょう。マグネシウムは水素元素よりも反応性の高い金属であるため、次の反応に従って酸カチオンである H +を置き換えます。
Mg (秒) + 2 HCl (水溶液) → MgCl 2 (水溶液) + H 2(g)
または
Mg 0 (s) + 2 H + (aq) → Mg 2+ (aq) + H 2 0 (g)

それぞれの化学種に何が起こったのか見てみましょう。
- 金属マグネシウム(Mg (s) )は電子を2つ失って、つまり酸化してMg 2+ (aq)になりました。また、Nox (酸化数) が0から+2に増加していることも確認してください。
Mg 0 (s) → Mg 2+ (aq) + 2e –

本文の冒頭で述べたように、あらゆる酸化還元反応において、一方の化学種は電子を失い、他方の化学種は電子を獲得するため、マグネシウムが失った電子は別の原子によって獲得されます。このように、マグネシウムは別の元素の還元を引き起こすため、マグネシウムは物質または還元剤と見なされます。
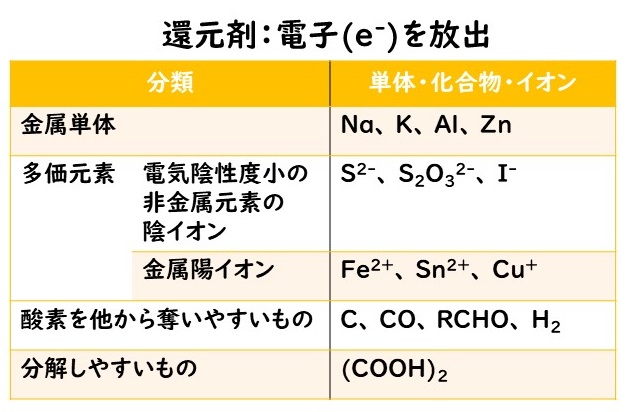
これに基づいて、還元剤は次の特性によって説明されると言えます。

- 酸の水溶液中に存在する水素カチオン (H + ) は、金属マグネシウムが失った電子を受け取り、水素ガス (H 2 ) に変わりました。水素は減少し、マグネシウムとは異なり、その Nox は+1から0に減少しました。
2H + (aq) + 2e – → H 2 0 (g)

これは、還元された種が他の種を酸化させることを意味します。このため、それは酸化物質または酸化剤と呼ばれ、その識別特性は次のとおりです。
したがって、この反応については次のようになります。

.jpg)
.jpg)
