スチール釘 (主に鉄で構成される金属合金) を硫酸銅 (CuSO 4(aq) ) の水溶液に浸すことを想像してください。時間が経つと、主に青色だった溶液が無色になり、爪上に赤みがかった金属の沈着物が形成されることに気づきます。
何がこうした変化を引き起こしたのでしょうか?
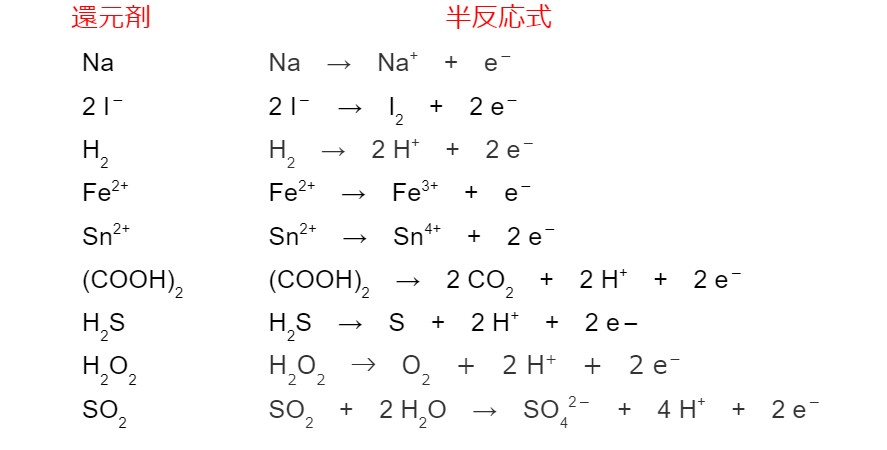
以下のこの反応の方程式に見られるように、電子移動が発生しました。
金属亜鉛 (Zn (s) ) は 2 つの電子を失い、Zn 2+ (aq)カチオンに変化し、水溶液中に残ります。鉄が酸化した、つまり電子が失われ、酸化数(Nox)が増加した(電子がマイナスの電荷を持っているため)と言います。
Fe (s) → Fe 2+ (aq) + 2e –
同時に、水溶液中に存在する銅カチオン(Cu 2+ (aq) )は、鉄から伝達されたこれら2つの電子を受け取り、金属銅(Cu (s) )になります。 Cu 2+ (水性)カチオンは溶液の青色の原因でした。したがって、それらが消費されると、溶液は無色になります。形成された銅金属は爪の上に堆積し、前述の赤みを帯びた層を形成します。
銅カチオンが電子を獲得し、Nox が減少したため、銅カチオンが減少したと言います。
Cu 2+ (aq) → Cu (s)
これは酸化還元反応の一例です。
このタイプのすべての反応は、反応する物質の原子、イオン、または分子間の電子の移動によって特徴付けられます。これは、酸化と還元が同時に起こること、つまり、それぞれ電子の喪失と獲得が起こることを意味します。 1 つの原子、イオン、分子によって失われた電子は、すぐに他の原子、イオン、分子によって受け取られます。
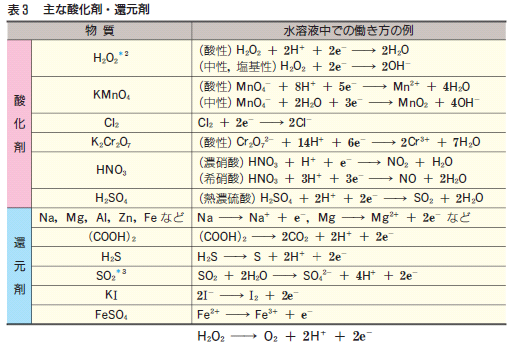
適切にバランスがとれた酸化還元反応では、ある反応物によって失われる電子の数は、別の反応物によって獲得される電子の数と正確に等しくなります。したがって、酸化を受ける化学種は還元剤とも呼ばれます。これは、反応で他の化学種の還元が起こるのは電子の喪失によるものであるためです。そして、還元を受けた化学種は、相手の酸化を引き起こすため、酸化剤と呼ばれます。
酸化還元反応は、酸化還元反応やレドックス反応とも呼ばれることがあります。

これまでの説明に基づいて、すべての酸化還元反応には次の要素が含まれると言えます。
この主題に関連するビデオ レッスンをぜひご覧ください。



