金属との単純な交換反応は、反応物が必然的に、金属カチオン-Y +またはヒドロニウム-H +を有する複合物質-YXと、単一の金属物質[W (s) ]である化学プロセスです。
単純な交換反応の反応物は化合物と単体であるため、この種の化学反応で生成される生成物も必然的に新しい複合物質と新しい単体になります。
金属との単純交換反応の原理は、以下に提案する一般式に従って、金属単体 (W (s) ) が複合物質 (YX (aq) ) のカチオンに生じる位置または変位の交換です。
W (s) + YX (aq) → WX (aq) + Y (s)
ただし、このタイプの反応は、反応物として使用される金属が、化合物物質に存在するカチオンよりも反応性が高い (非貴金属である) 場合にのみ発生します。
注:単体の金属が貴金属(水素よりも電気陽性率が低い非反応性)の場合、金属との単純な交換反応は起こりません。
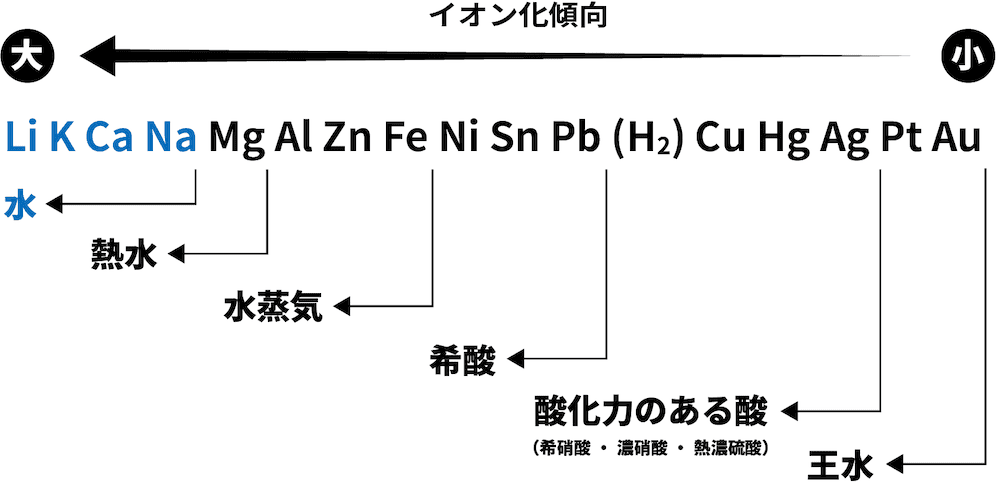
次のスキームは、金属元素に関する反応性 (電気陽性) の降順を示しています。
Li > Rb > K > Cs > Ba > Sr > Ca > Na > Mg > Al > Zn > Cr > Fe > Cd > Co > Ni > Sn > Pb > H > C > Ag > Pd > Hg > Pt > Au

例 1:金属銅 [Cu (s) ] と硫酸 (H 2 SO 4 ) との単純な交換反応。
Cu (s) + H 2 SO 4(aq) →
上で提案された金属の反応性の順序によると、銅は貴元素、つまり水素よりも反応性が低いため、反応は起こりません。
Cu (s) + H 2 SO 4(aq) → 発生しない
2 番目の例:アルミニウム [Al (s) ] とヨウ化クロム III (CrI 3 ) の間の単純な交換反応。
Al (s) + CrI 3(aq) →

反応性の順序によれば、アルミニウムはクロムよりも反応性の高い元素です。このような:
アルミニウムはクロムを置き換えます。
その結果、金属クロムが放出されます。
アルミニウム金属カチオン(IIIA族由来のAl +3 )と塩(I -1 )のヨウ化物アニオンの結合による複合物質ヨウ化アルミニウム(AlI 3 )の形成。
次のバランスの取れた方程式は、このプロセスを表します。
2 Al (s) + 2 CrI 3(aq) → 2 AlI 3(aq) + 3 I 2(aq)

例 3:金属カリウム [K (s) ] と塩酸 (HCl) との単純な交換反応。
K (s) + HCl (aq) →
上記で提案された反応性の順序によれば、カリウムは塩酸中に存在する水素よりも反応性の高い元素です。その方法:
カリウムは水素を置き換えます。
結果として水素分子(水素原子が結合して H 2分子を形成するもの)が放出されます。
カリウム金属カチオン (K +1 、ファミリー IA 由来) と塩の塩化物アニオン (Cl -1 ) の結合による複合物質塩化カリウム (KCl) の形成。

次のバランスの取れた方程式は、このプロセスを表します。
2 K (秒) + 2 HCl (水溶液) → 2 KCl (水溶液) + H 2(g)
第 4 例:スズ [Sn (s) ] と炭酸マグネシウム (MgCO 3 ) との単純な交換反応。
Sn (s) + MgCO 3(aq) →
金属に対して提案されている反応性の順序に従えば、スズはマグネシウムよりも反応性が低い元素であるため、反応は起こりません。
Sn (s) + MgCO 3(aq) → 発生しない
このテーマに関するビデオレッスンをぜひご覧ください。
