酸化還元反応とは、「酸化還元」の文中にあるように、電子の喪失と獲得が同時に起こる反応です。電子を失った原子またはイオンは酸化を受け、電子を獲得した原子またはイオンは還元を受けます。
たとえば、銅 II カチオンを含む硫酸銅の溶液に亜鉛板を置くと、亜鉛が酸化して銅に電子を供与し、以下が減少します。
Zn 0 (s) → Zn 2+ (aq) + 2 電子
Cu 2+ (aq) + 2 電子 → Cu 0 (s)
Zn 0 (s) + Cu 2+ (aq) → Zn 2+ (aq) + Cu 0 (s)
この場合、銅と亜鉛という 2 つの金属がありますが、亜鉛は電子を供与する傾向が大きいため、酸化が起こります。金属の反応性については次の定義があるため、銅よりも反応性が高いと言えます。
これは、以下に示すように、銅が酸化して亜鉛に電子を供与するという逆の反応を実行したい場合、これは自然媒体では不可能であることを意味します。

Cu 0 (s) + Zn 2+ (aq) →自発反応は起こらない
反応性の低い金属原子から反応性の高い金属のカチオンへの電子の移動は自発的ではないため、この反応はシステムにエネルギーを供給した場合にのみ発生します。
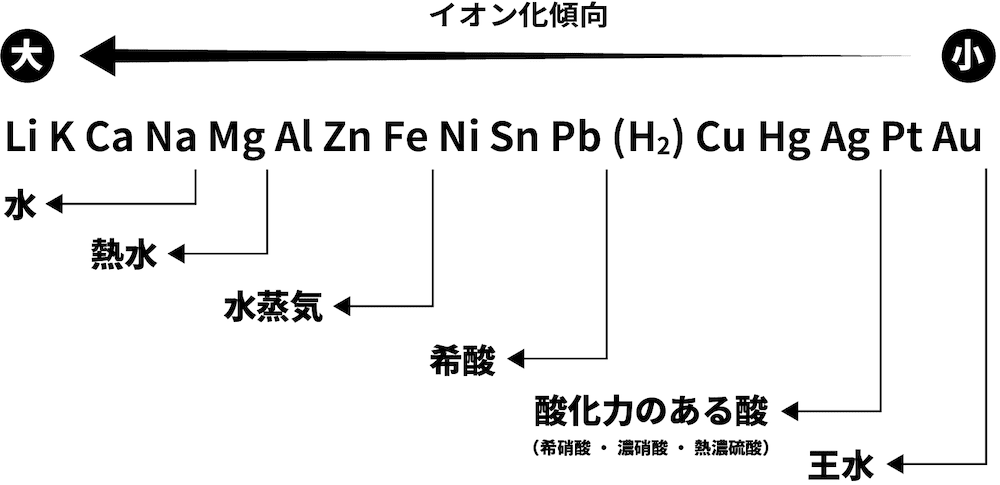
化学者は、さまざまな金属を比較することで、どの金属が電子を放出する傾向が最も大きいか、最も小さいかを判断することができました。これに伴い、反応性キューまたは 電解電圧の行。これは以下に与えられます。

金属ではないにもかかわらず、水素はこの反応性ラインに現れることに注意してください。これは、水素が特定の物質(酸など)に存在すると、ヒドロニウムカチオン(H 3 O 1+ )を形成できるためです。このカチオンは電子を受け取ることができ、次の反応に従って水素ガスと水を生成します。
2 H 3 O 1+ (aq) + 2e – → H 2(g) + 2 H 2 O (l)
水素より反応性の低い金属は貴金属と呼ばれます。
反応性の高い金属は、反応性の低い金属のカチオンを置き換えます。反応性キューで、Zn が Cu よりも前に表示されること、つまり Zn の方が反応性が高いため、銅のカチオンを置換するのは Zn であることにもう一度注意してください。

したがって、この反応性キューを参照することで、特定の酸化還元反応が起こるかどうかを予測することができます。
たとえば、銅 (Cu)、アルミニウム (Al)、および亜鉛 (Zn) のサンプルを塩酸 (HCl) の中に入れた次の実験を参照してください。反応性キューを見ると、Al と Zn は水素よりも反応性が高いため、これらの反応が発生し、亜鉛の反応性が高いため、酸化がアルミニウムよりも早く起こることがわかります。 Cu は水素よりも反応性が低くなります (反応性スケールでは水素のすぐ下にあることがわかります)。これは、水素カチオンを置換しないため、この反応は起こらないことを意味します。
また、金 (Au) はすべての金属の中で最も反応性が低いことにも注意してください。これが貴重な理由の 1 つであり、孤立した酸の攻撃に耐性があり、塩酸 3 部と硝酸 1 部の混合物である王水によってのみ攻撃されるためです。



