冶金学では、鉱石から金属を得るために電気分解技術 (液体化合物を分解するために電気を通す) を使用することはよく知られています。
ただし、電気分解は多くの非金属を得るためにも使用されます。その中には、周期表の第 17 族 (または VII A) に属する元素であるハロゲンも含まれます。

それらの中で、商業的に最も重要なものは塩素であり、周囲条件下で緑がかった黄色のガス (Cl 2 ) を形成し、高密度で毒性が高く、反応性が高く、水に溶けにくく、水素と爆発的に反応します。 有機および無機化合物の製造、紙の製造(セルロースの漂白を目的)、上下水の処理に使用されます。 「液体塩素」は水に溶けた塩素で、「固体塩素」は実際には次亜塩素酸カルシウム塩(Ca(ClO) 2 )と次亜塩素酸ナトリウム塩(NaClO)です。
塩素ガスを得る最も一般的な方法の 1 つは、塩化ナトリウムの火成電気分解によるものです。つまり、食塩を溶かし、液体状態のこの塩に電流を流すと、塩素ガスだけでなく金属も生成します。ナトリウム。

この場合に起こる全体的な反応は次のようになります。
陰極:Na + (ℓ) + e- →Na (s)
陽極: 2Cl – (ℓ) → 2e – + 1Cl 2 (g)____________
全体的な反応: Na + (ℓ) + 2Cl – (ℓ) → Na (s) + 1Cl 2 (g)
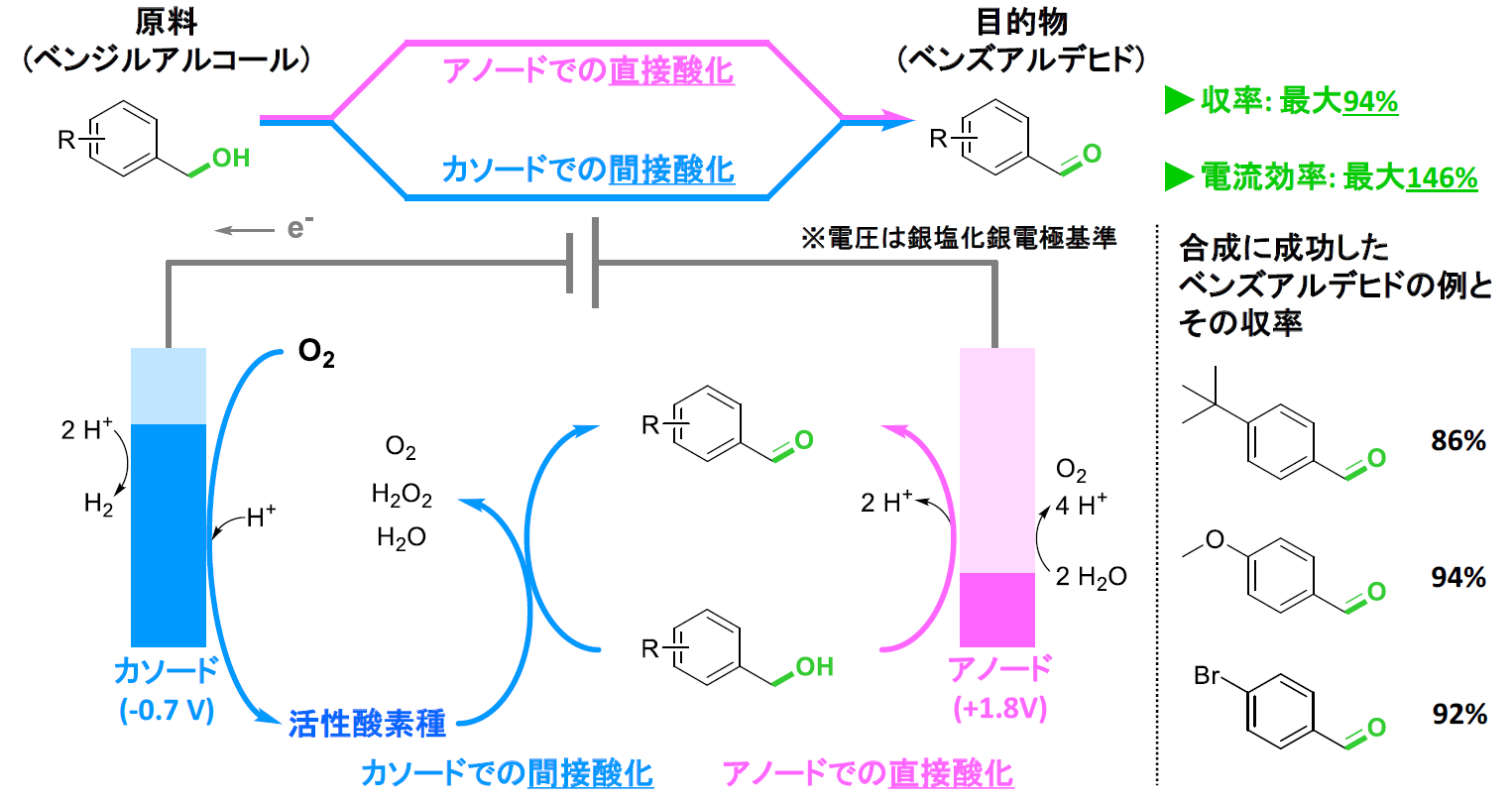
塩化マグネシウム (MgCl 2 ) の電気分解も塩素ガスを得る手段です。

フッ素、あるいはフッ素ガス (F 2 ) は電気分解によっても得ることができますが、現在は溶融フッ化カリウム (KF) の存在下で液体フッ化水素酸 (HF) から得られます。
この電気分解の半反応と全体反応は次のとおりです。
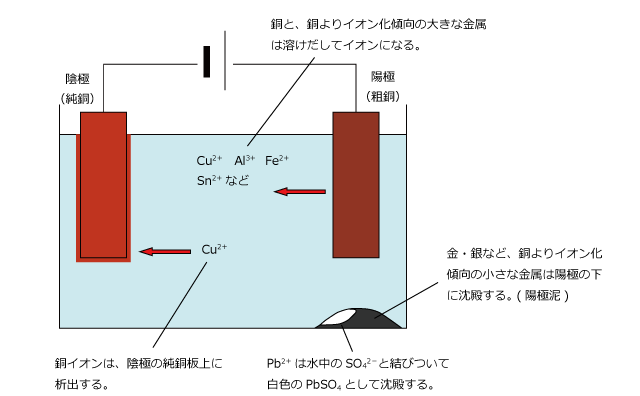
カソード:2H ++ 2e- →H2 (g)
アノード: 2F – → 2e – + F 2(g) ____________
全体の反応: 2 HF (ℓ) → H 2(g) + F 2(g)
塩素、臭素、ヨウ素は、以下に示すような酸化還元反応によっても得られます。
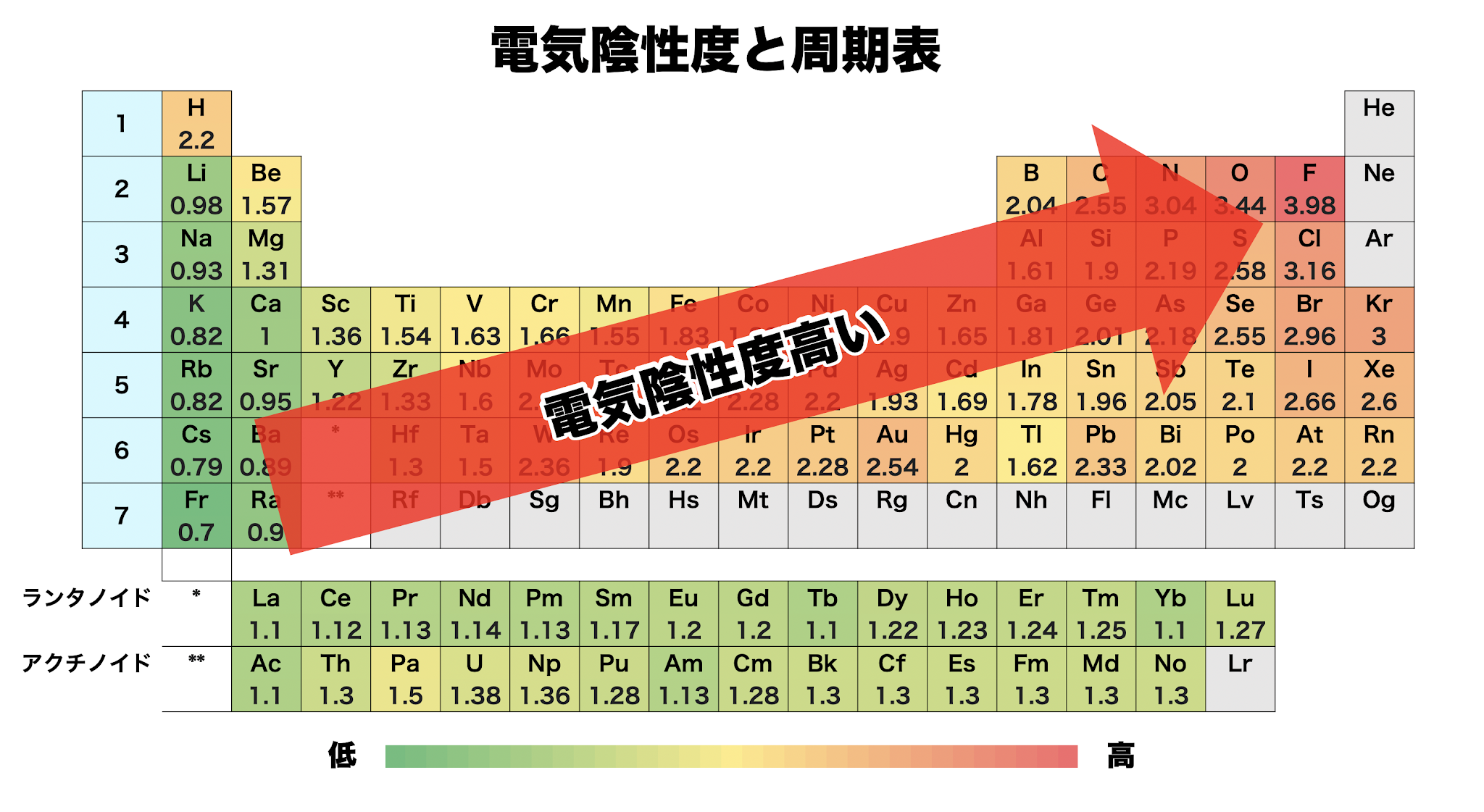
臭素の取得: Cl 2(g) + 2 NaBr (aq) → 2 NaCl (aq) + 2 Br 2(g)
ヨウ素の取得: Cl 2(g) + 2 NaI (aq) → 2 NaCl (aq) + 2 I 2(g)
塩素ガスは還元電位が高いため、上記の反応で使用されます。
*画像編集クレジット:
出典: Science Made Alive: 化学/元素 – ハロゲン/ ウィキメディア・コモンズ
著者: W. オーレン

