顕熱と潜熱は、物質が熱変化を受けるために物質に追加または除去する必要がある熱量を表す物理量です。以下の定義を参照してください。
顕熱とは、物質の単位質量あたりの温度が1度変化するのに必要な熱量のことです。この名前は、材料が凝集したままの状態で、受け取った熱によって温度が変化するだけの場合にのみ付けられます。

このタイプの状況の例としては、火の近くに置かれると加熱しますが、固体状態を保つ金属片が挙げられます。
顕熱(顕比熱とも呼ばれる) は文字 c で表され、材料の種類とその凝集状態によって異なります。例えば:
液体の水の場合、c = 1 cal/g となります。 ℃。これは、水の温度を1℃上げるには水1gに対して石灰1個を供給する必要がある、または温度を1℃下げるには石灰1個を除去する必要があることを意味します。
しかし、固体の水の場合、この量はすでに c = 0.5 cal/g.℃ です。
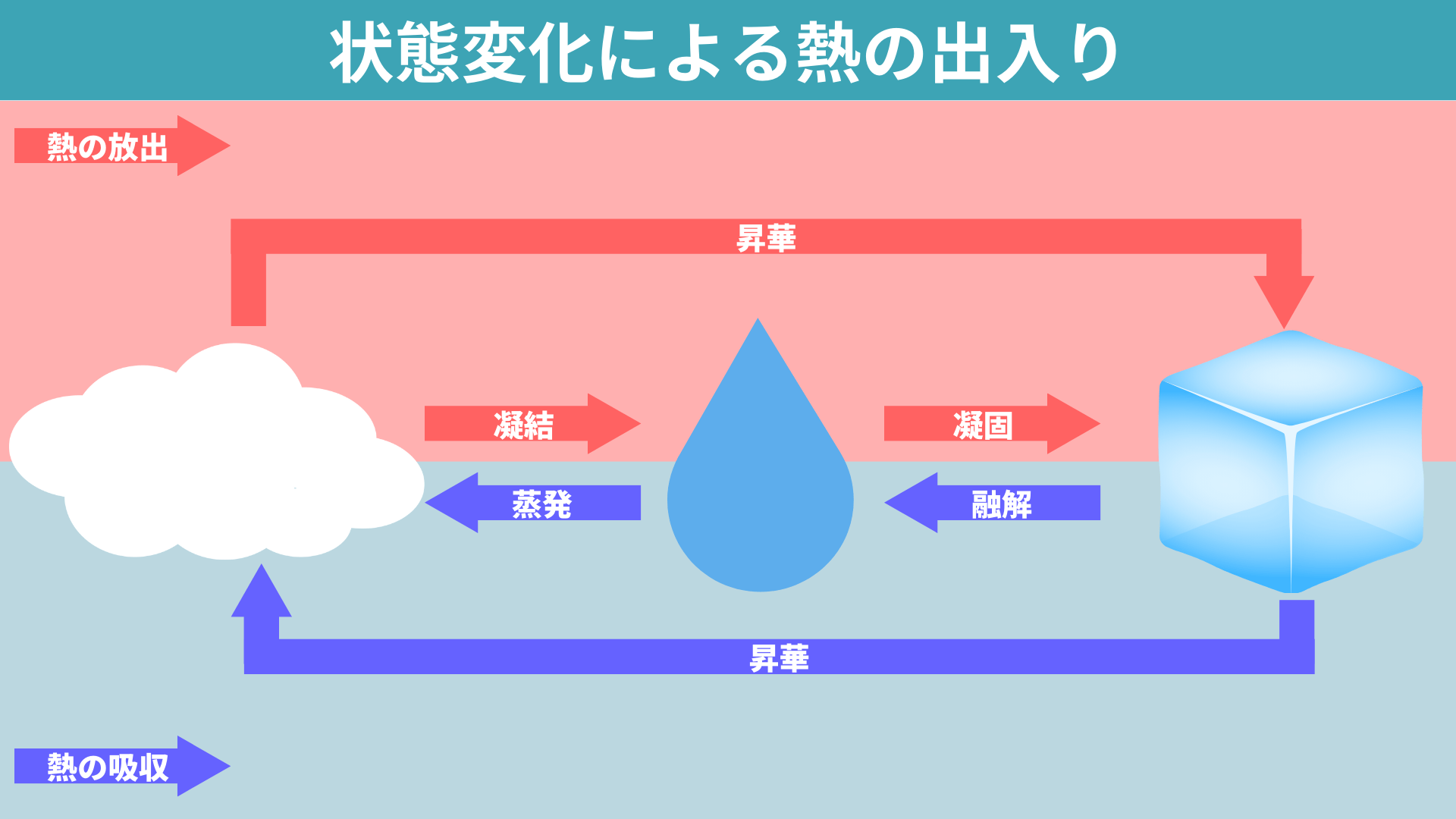
材料の顕熱の計算に使用される方程式は次のとおりです。
Q = m。 w 。 Δθ
いる:
Q – 熱量。

m – 物質の質量。
c – 物質の比熱;
Δθ — 温度変化。
顕熱の定義は、熱容量の概念にも関連しています。熱容量は、温度が 1℃変化するために物体の総質量が受け取るか失う必要がある熱量に相当します。

熱容量は次の式で求められます。
C = メートル。 w
いる:
C – 熱容量。

m – 物体の質量。
c – 比熱。
文字 L で表される潜熱は、物体に供給または除去されたときに、その温度は変化しないが、その凝集状態に変化を引き起こす熱量です。これは、凝集状態を変化させるために物体に供給または除去する必要がある単位質量当たりの熱量を示します。
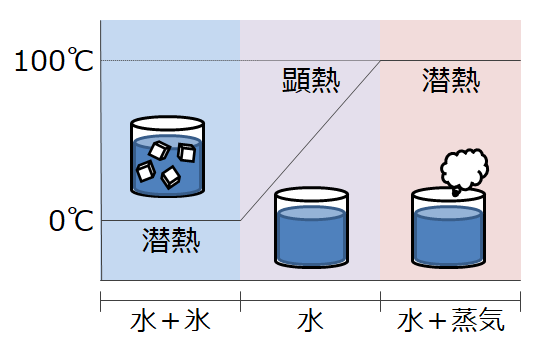
私たちはこの現象を氷の融解で観察し、同じ温度で固体状態と液体状態の水を見ることができます。物質に供給された熱は、温度の上昇ではなく、完全に相変化に戻ります。
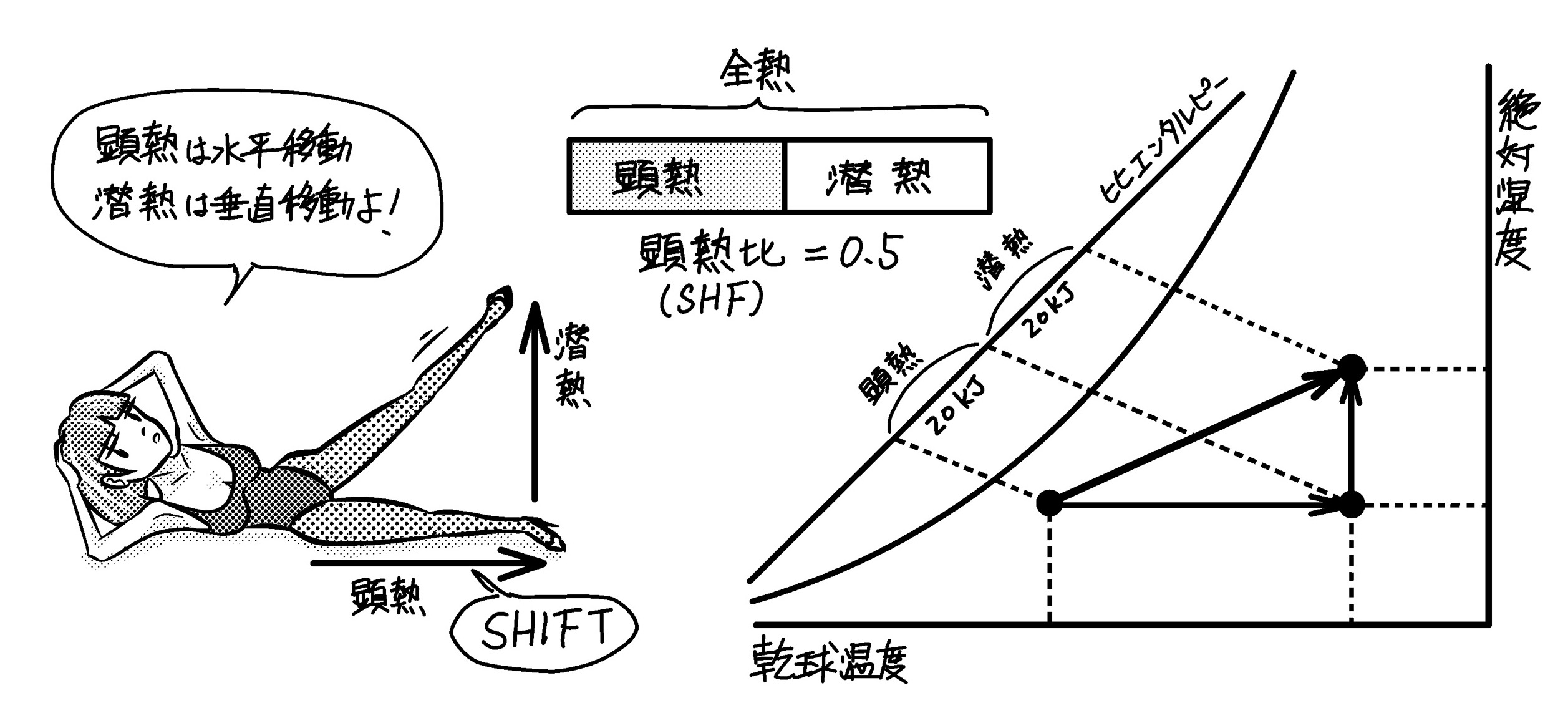
潜熱は次の式で計算されます。
Q = m。 L
したがって:
Q – 熱量。
m – 物質の質量。
L – 潜熱。
物質が熱を受けてその状態が変化する場合、つまり溶融や蒸発が起こる場合、L の値は正になります。しかし、物質が熱を失うと、L は負になり、これが凝固と液化で起こります。
この主題に関連するビデオ レッスンをぜひご覧ください。
