アルカンは炭素原子間に単結合しかない炭化水素であるため、飽和化合物と呼ばれます。それらは直鎖、分枝鎖、および環状鎖で存在することができ、後者の場合、それらはシクロアルカンとして知られます。その一般式は次のとおりです: C n H 2n+2 。
一般に、アルカンは非反応性で非極性の性質を持ち、その融点と沸点の特性は炭素鎖の長さに比例して変化します。石油と天然ガスはアルカンの主な入手源であり、特に燃料として多くの用途があります。
アルカンの概要
これらは炭化水素、つまり炭素原子と水素原子のみで形成されます。
これらは飽和炭化水素です。つまり、炭素原子間には単結合しかありません。その一般式は次のとおりです: C n H 2n+2 。
それらの鎖は、直鎖、分枝鎖、または環状にすることができます。
これらは最も単純な炭化水素であり、非極性の性質を持ち、あまり反応性がありません。
炭素鎖が長ければ長いほど、融点と沸点は高くなります。
その主な原産地は石油と天然ガスです。
天然ガスは主にメタン (CH 4 ) で構成されています。
石油は、アルカン含有量が高い炭化水素の複雑な混合物です。
石油の分別蒸留により、炭素鎖のサイズに応じてさまざまなアルカンが分離されます。
石油に基づいて、燃料を含むいくつかの商業用製品が得られます。
燃料に加えて、アルカンは化学産業で幅広い用途に使用されています。
アルカンとは何ですか?
アルカンはパラフィンとも呼ばれ、炭化水素の部類に属し、炭素原子間に単結合のみを持つ飽和化合物です。これらは炭化水素であるため、完全に炭素原子と水素原子で構成されており、他の官能基はありません。
アルカンは最も単純な炭化水素種です。下の画像は、メタンと呼ばれる 1 つの炭素原子で構成されるアルカンと、エタンと呼ばれる 2 つの炭素原子で構成されるアルカンを示しています。

アルカンは炭素鎖の構成に応じて 3 つのグループに分類できます。以下のグループを参照してください。
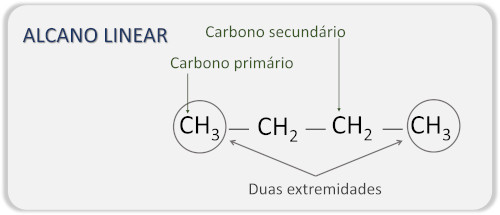
→ 直鎖アルカン
直鎖アルカンの主な特徴は、分岐がないことです。直鎖アルカンは、一次炭素 (1 つの炭素原子のみに結合) と二次炭素 (他の 2 つの炭素原子に結合) のみで形成されます。つまり、鎖の末端は 2 つだけです。 。これらは脂肪族アルカンまたは非環式アルカンとしても知られています。
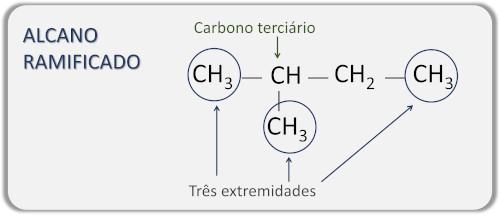
→ 分岐鎖アルカン
分岐鎖アルカンは、3 つ以上の末端を持ち、少なくとも 1 つの第三級炭素 (他の 3 つの炭素原子に結合) または第四級炭素 (他の 4 つの炭素原子に結合) を持ち、その中に分岐が位置する分子です。
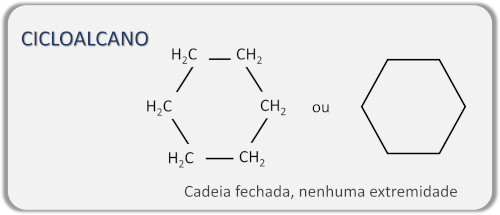
→ 環状鎖状アルカン(シクロアルカン)
シクロアルカンまたは環状アルカンは、単純な結合のみで結合された炭素原子の環を形成するという点で他のものとは異なります。これらの構造は閉鎖アルカンとも呼ばれます。
アルカンの特徴と性質
アルカンは最も単純な炭化水素です。通常は無色無臭で、密度は水よりも低いです。
アルカンを他の炭化水素と区別する特徴は、反応性が低いことです。これは、不飽和が存在しないことでアルカン分子が化学的に安定していることで説明されます。
アルカンでは、各炭素原子は 4 つの単純な結合、つまりシグマ (σ) 結合を確立します。シグマ結合は、化学結合の確立中に各原子の原子軌道間でより大きな相互作用が発生するため、パイ (π) 結合よりも安定で強力です。
有機化学では、二重結合と三重結合に存在するπ結合(それぞれアルケンとアルキンに見られます)により、これらの分子はアルカンに比べて反応性が高くなります。これは、アルカンが化学反応をまったく起こさないという意味ではありません。実際には、このタイプの炭化水素が反応するには、熱または放射線による追加のエネルギーの入力が必要です。
アルカンは反応性が低いため、研究室で興味深い用途が得られます。たとえば、さまざまな化学反応において溶媒として機能し、研究中のシステムへの影響を最小限に抑えることができます。
アルカンには他にもいくつかの用途がありますが、そのうちの 1 つである燃料としての使用は注目に値します。たとえば、ガソリンは、異なるモル質量のアルカンの混合物です。燃料としてのアルカンの効率は、炭素-炭素結合および炭素-水素結合に閉じ込められた高いエネルギーによるもので、このエネルギーは燃焼などの酸化反応で容易に放出されます。
アルカンは非極性 (または非極性) 物質であるため、水などの極性溶媒とは混和しません。一方、ベンゼンやトルエンなどの他の非極性物質とは完全に混和します。
海上で石油が流出した場合、極性が異なるため、この物質は水と混合しません。石油はアルカンの混合物で形成されており、非極性の性質を持っているため、極性物質である水と混合することができません。

最大 4 個の炭素原子で形成されるアルカンは、ガス状で引火性の高い物質です。この例としては、メタン、エタン、プロパン、ブタンなどがあります。
ペンタンからオクタデカン(それぞれ炭素数 5 と 18 の炭化水素)まで、アルカンは液体です。ペンタンの沸点は比較的低く、約 36 °C です。より長いアルカンは、分子量の増加により、融点が徐々に上昇します。
炭素数が 18 を超える炭素鎖は、ワックス状で密度の高い物質を形成する傾向があります。たとえば、キャンドルのワックスは、20 ~ 25 個の炭素原子を持つ鎖で構成されています。
以下のグラフは、炭素数 16 までの一連のアルカンについて、炭素鎖のサイズが大きくなるにつれて、融解温度 (青) と沸点 (赤) が上昇する傾向を示しています。グラフには示されていませんが、チェーンが長くなるほど傾向は続きます。

アルカン式
アルカンの一般式は C n H 2n+2で、 nは炭素数です。これを考慮すると、存在し得る最も単純なアルカンはメタンであり、炭素原子が 1 つあるため、水素原子が 4 つあります。

アルカンの一般式を使用すると、炭素数に基づいて分子内に存在する水素の量を予測することができます。たとえば、 n = 2 の場合、水素の数は 6 で、アルカンの分子式は C 2 H 6です。

n = 3 の場合、水素の数は 8 で、アルカンの分子式は C 3 H 8です。

n = 8 の場合、水素の数は18で、アルカンの分子式はC8H18です。

重要:環状アルカン (シクロアルカン) を扱う場合、一般式は C n H 2nになります。
アルカンの命名法は何ですか?
アルカンの命名法は、炭化水素の命名法に関してIupac (国際純粋応用化学連合) によって定義された規則に従う必要があります。
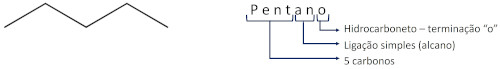
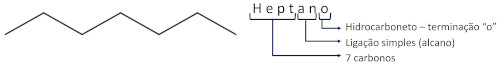
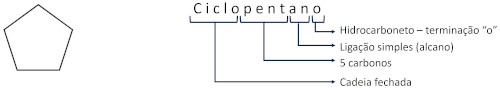
分子の名前は、主鎖の炭素数に対応する接頭辞で始まります。次に、不飽和の有無を示す中置記号があります。アルカン、飽和分子の場合、接尾辞は-an-となり、接尾辞-oで終わり、炭化水素であることを示します。

以下の表は、炭化水素分子の主鎖の炭素数に応じて使用する必要がある接頭辞を示しています。
|
炭素数 |
プレフィックス |
|
1 |
会った- |
|
2 |
え~ |
|
3 |
プロップ- |
|
4 |
しかし- |
|
5 |
ペント- |
|
6 |
ヘックス- |
|
7 |
ヘプト- |
|
8 |
10月~ |
|
9 |
非 |
|
10 |
12月~ |
いくつかの例を見てみましょう。
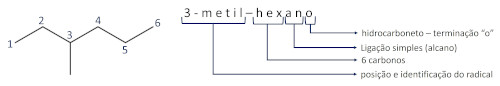
分岐アルカンでは、分岐の位置は、分岐が位置する主鎖の炭素数に従って特定する必要があります。分岐の識別はアルカンの名前の前に来ます。
見て:
アルカンの異性化
異性体は、同じ分子式を持ちますが、結合の周りの分子の回転による単純な配置を除いて、空間内の原子の配置が異なる分子です。
構造異性では、原子が異なる順序で配置されており、このタイプの異性の中にさまざまなタイプが存在します。アルカンの場合、鎖異性が最も関係しており、炭素鎖に分岐が存在する可能性があるために発生します。

アルカンの可能な異性体の数は、炭素鎖の原子の数に応じて増加します。見て:
|
名前 |
分子式 |
考えられる異性体の数 |
|
メタン |
CH4 |
1 |
|
エタン |
C2H6 |
2 |
|
プロパン |
C3H8 |
1 |
|
ブタン |
C4H10 |
2 |
|
ペンタン |
C5H12 |
3 |
|
ヘキサン |
C6H14 |
5 |
|
ヘプタン |
C7H16 |
9 |
|
オクタン |
C8H18 |
18 |
|
ノナノ |
C9H20 |
35 |
|
ディーン |
C10H22 |
75 |
アルカンの入手源
アルカンは、石油と天然ガスという 2 つの主な供給源から得られます。どちらも特定の地層で発生します。
石油は炭化水素の複雑な混合物であり、アルカンを多く含んでいます。天然ガスは短鎖炭化水素の混合物であり、多量のメタンとエタンを含み、程度は低いですがプロパンとブタンを含みます。
石油と天然ガスは、不浸透性の岩層の下にある多孔質の岩石に含まれています。これらの物質は、古代の海の底に堆積し、堆積物の層に覆われた動植物の死骸に由来する有機物に由来します。低酸素、高温、高圧の環境により、有機物は数百万年かけてゆっくりと現在の形に変換されました。

天然ガスと石油は、車両や機械のエネルギー源として使用されます。生成プロセスが遅いため、これら 2 つの燃料は短期間で再度準備することができないため、再生不可能なエネルギー源とみなされます。
存在する最も単純な炭化水素であるメタン (CH 4 ) は、動物や有機物の分解によって生成されるガスであるバイオガスに含まれています。メタンは、有機物の分解プロセスによりこれらの場所で自然に生成されるため、埋め立てガスまたは沼地ガスとしても知られています。これらの資源から得られるメタンは、再生可能なエネルギー源と考えられています。
天然ガスは、配管システムを通して排出することにより、多孔質の岩石中に見られるポケットから容易に得られます。石油を形成する炭化水素の混合後、製油所の特定の装置を使用して実行される物理的分離プロセスである分別蒸留によってアルカンが分離されます。
接触改質や分解などの化学プロセスも、分別蒸留によって石油から分離された高分子量画分からアルカンを得るために使用されます。

アルカンは何に使用されますか?
アルカンはほとんどの燃料および潤滑油の主成分であり、化学産業で広く使用されています。
天然ガスの主成分であるメタンとエタンは、暖房および調理システムに使用されます。天然ガスは燃料としても使用され、車両用天然ガス (CNG) として知られています。
石油の分別蒸留により、さまざまな沸点に従って分離された炭化水素のさまざまな留分が得られます。この特性は、炭素鎖のさまざまなサイズを反映しています。沸点が高いほど、鎖を構成する炭素の量が多くなります。
以下の表は、アルカンの範囲、その特性、主な用途に関する情報をまとめたものです。
|
炭素鎖の延長 |
主な特性と用途 |
|
炭素数3~4 |
プロパンとブタンは低圧で液化するため、エアロゾル、ガスバーナー、ライターの噴射剤として使用されます。 |
|
炭素数5~8 |
液体で揮発性の高いアルカン。これらは、非極性溶媒として、また内燃機関の燃料として使用されます。オクタン( C8H18 ) はガソリンの主成分の 1 つです。 |
|
炭素数9~16 |
|
|
炭素数17~35 |
高粘度の液体または固体のアルカン。これらは潤滑油の組成物や防食剤(疎水性のため)として使用されます。固体アルカンはワックスやパラフィン(キャンドル)として使用されます。 |
|
炭素数が35以上 |
道路(アスファルト)の舗装に使用されるアルカン。これらは工業的用途がほとんどないため、一般に分解プロセスを受けて、より低いモル質量のアルカンに変換されます。 |