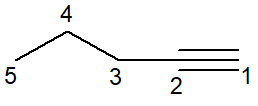炭化水素は、その組成中に炭素と水素のみを含むため、最も単純な有機化合物です。しかし、それらは主に石油から得られるため、最も重要であり、日常生活で使用されています。したがって、それらは燃料 (天然ガス、ガソリン、ディーゼルなど)、樹脂、およびプラスチックの大部分で構成されています。
炭化水素は、その炭素鎖に従って、開いたもの(アルカン、アルケン、アルキン、およびアルカジエン)、閉じたもの(シクロアルカンおよびシクロアルケン)、または芳香族に分類できます。その一般的な分子式は C x H yで、x と y は整数を表します。

炭化水素の種類
前述したように、炭化水素は炭素鎖の種類に応じて分類されます。
開鎖炭化水素には次のようなものがあります。
アルカジエン: 炭素間に 2 つの二重結合があります。
閉鎖炭化水素には次のものがあります。
芳香族鎖状炭化水素、つまり少なくとも 1 つの芳香環 (または核) を持つ炭化水素もあります。
炭化水素の性質
炭化水素のすべての物理化学的特性の中で、最も重要なのは、炭化水素が非極性化合物であることです。炭化水素は非極性であるため、極性溶媒である水には溶けません。類似性の法則によれば、極性化合物が他の極性化合物にのみ可溶であるのと同様に、非極性化合物は他の非極性化合物にのみ可溶であることを覚えておく必要があります。

また、炭化水素は非極性であるため、ファンデルワールス力(またはロンドン力、または誘起双極子相互作用 – 誘起双極子)と呼ばれる非極性分子間の相互作用力として、同様の分子量の極性化合物と比較した場合、融点と沸点が低くなります。は、双極子間相互作用と呼ばれる極性分子間の相互作用力よりも弱いです。
しかし、炭化水素の中では、鎖が長くなるにつれて双極子による誘起双極子相互作用がより強まるため、融点と沸点が上昇することは明らかです。

炭化水素分子間の相互作用も密度に影響を与えます。これらの相互作用はそれほど強くないため、分子間の間隔が広くなる傾向があり、このため炭化水素の密度は水よりも低くなり、その値は 1.0 g/cm3 です。
反応性に関しては、炭化水素は付加、酸化、還元、置換などのさまざまな種類の反応を受ける可能性があります。ただし、炭素数が 6 個を超えるアルカン、芳香族化合物、およびシクロアルカンは最も安定した炭化水素であるため、他の炭化水素よりも反応性が低くなります。
この安定性を説明するには、アルカンには最も強い σ (シグマ) タイプの結合のみがあることを考慮する必要があります。芳香族化合物は共鳴効果によって常に安定化しており、構造内の電子の反発が減少します。少なくとも 6 つの炭素を含むシクロアルカンは、炭素間の結合角が 109° 28′ になることがあり、電子間の反発を最小限に抑えて安定性を保証します。このような角度を達成するために、炭素は異なる平面にあり、分子を歪めます。
炭化水素の命名法
すべての有機化合物は、国際純粋応用化学連合 (Iupac) によって確立された正式な命名法に従います。 Iupac は、すべての炭化水素には接尾辞 –o が必要であると決定しています。
炭化水素に名前を付けるには、次のことを行う必要があります。
主鎖を特定する。
不飽和(存在する場合)の位置を決定します。
分岐がある場合は、分岐の位置を決定します。
その後、名前は一般に次の構造になります。
アルファベット順の枝の位置と名前 + 主鎖の名前
メインチェーンの名前は常に 3 つの部分に分かれています。
接頭辞: 炭素原子の数を示します。
infix : 鎖に単結合のみ (-an-) があるか、二重結合 (-en-) または三重結合 (-in-) が存在するかを識別します。
接尾辞: 有機関数を識別します。前述したように、炭化水素の場合は常に –o です。
接頭辞に関しては、炭素数 4 までは次のとおりであることを覚えておく価値があります。
満たされた – 1 つの炭素の場合。
et- 2 つの炭素の場合。
prop- 3 つの炭素の場合。
ただし、炭素数 4 の場合。
炭素数が 5 つ以上の場合は、ギリシャ語に由来する接頭辞 (pent-、hex-、hept-、oct-…) を使用する必要があります。
ブランチには、炭素鎖と同じ接頭辞に加えて、接尾辞 –il または –ila が付けられます (中置辞は必要ありません)。
アルカン
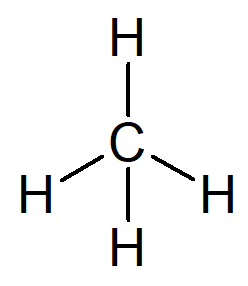
存在する最も単純な炭化水素はメタンと呼ばれるアルカンで、分子式CH4を持ち、天然ガスの主成分です。
その名前は次の理由に基づいて作成できます。
炭素を 1 つだけ持つ有機構造を表す接頭辞が満たされます –。
炭素間に単結合のみを持つ有機構造を表す接辞は、 -an- です。
すべての炭化水素の接尾辞は–oです。
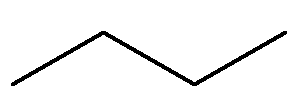
非常に重要なもう 1 つのアルカンは、液化石油ガス(LPG) に存在する式 C 4 H 10のブタンです。
ブタンという名前を理解するには:
4 つの炭素を持つ有機構造を表す接頭辞はbut です。
炭素間に単結合のみを持つ有機構造を表す接辞は、 -an- です。
すべての炭化水素の接尾辞は–oです。
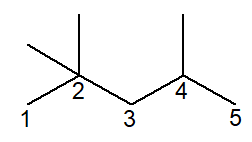
アルカンが分岐している場合、すべての分岐に番号と名前を付ける必要があります。以下の例は、ガソリンの主成分である2,2,4-トリメチルペンタンです。主鎖は、Iupac の推奨に従って識別され、番号が付けられます。主鎖は、構造内で続く最も長い鎖であり、最後の 1 つの炭素から始まり、間にジャンプはありません。枝は常に可能な限り少ない位置に配置する必要がありますが、決して端に配置しないでください。
その名前は次のように正当化されます。
Iupac は、たとえ繰り返しがある場合でも、各ブランチにポジションが存在する必要があると判断します。 「メチル」と呼ばれる炭素の 3 つの分岐が確認されたことがわかります。主鎖の 2 位に 2 つのメチルラジカルがあり、4 位にもう 1 つあります。接頭辞tri – を使用します。 命名法では、そのような分岐が構造内で 3 回繰り返されることを示します。
主鎖には 5 つの炭素があるため、接尾辞pent- 、接尾辞-an- 、および炭化水素接尾辞-o が付加され、ペンタンになります。
続きを読む: 炭素数 10 を超えるアルカンの命名法
アルケン、アルキン、アルカジエン
アルケン、アルキン、アルカジエンなどの開鎖不飽和炭化水素には、アルカンと同じ命名規則がありますが、詳細が 1 つあります。それは、中置記号の不飽和を識別する必要があることです。
分岐と同様に、不飽和は鎖内のさまざまな位置に発生する可能性があるため、構造の正式名でその位置を特定する必要があります。
もう 1 つの重要な点は、不飽和が常に主鎖に存在する必要があるということです。
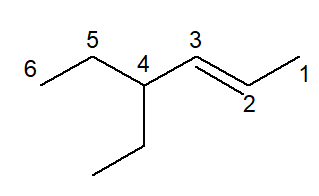
4-エチルヘキサ-2-エンに対応する次の例を参照してください。
鎖に分岐と不飽和が存在する場合、一般的な IUPAC 規則によれば、不飽和が分岐よりも優先されるため、最も小さい番号の位置を持たなければなりません。したがって、主鎖には右から左に番号が付けられました。
この番号付けでは、炭素 2 個の分岐 (名前はエチル) は炭素番号 4 にありました。
二重結合は炭素2と炭素3の間にありますが、正式名称では不飽和の開始炭素の位置のみが記載されています。
4-エチルヘキサ-2-エンという名前は次のように理解されます: 4 はエチル分岐の位置、 hex は主鎖の接頭辞、二重結合の位置を含む中置2-en 、および接尾辞としての-o炭化水素のこと。
2 番目の例では、次のようなケースがあります。 ペント-1-イン、アルキン。
三重結合を形成する炭素はspハイブリダイゼーションを起こしているため、直線状の形状をしています。したがって、一部の著者はこの特性を説明するために線形公式を採用しています。
三重結合は鎖の先端にあるため、主鎖のカウントが開始されます。
この構造には、接頭辞pent- 、三重結合の位置を含む中置辞1-in 、および炭化水素接尾辞として-o が付けられます。
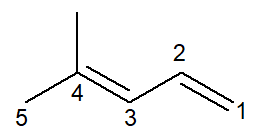
ここではアルカジエンの場合を考えます: 4-メチル-ペンタ-1,3-ジエン
命名法は実質的に同じですが、いくつかの変更が加えられています。読みやすくするために、接頭辞がペントからペンタに変更されています。
二重結合が 2 つあるため、両方に中置記号で番号を付ける必要があります。炭素番号 1 から始まるものと炭素番号 3 から始まるものの両方です。接頭辞di-は、名前に二重結合が 2 つあることを示すためにも使用されます。 。
したがって、分岐である4-methylで始まり、接頭辞penta- 、2 つの二重結合の位置を含む中置1,3-dien 、および炭化水素接尾辞–oが続きます。
シクロアルカンおよびシクロアルケン
シクロアルカンとシクロアルケンはどちらも、それぞれの開鎖炭化水素、アルカン、アルケンと同じ命名規則を持っています。
唯一の違いは、次の例に示すように、メイン チェーンの名前が接頭辞ciclo-で始まる必要があることです。
上記の構造は炭素数 4 のシクロアルカンであるため、シクロブタンとして知られています。
炭素数が 4 つで閉じているため、接頭辞cyclobut- が付きます。
中置辞–an–は、炭素間のすべての結合が単純であることを示します。
接尾辞-oは、炭化水素であることを示します。
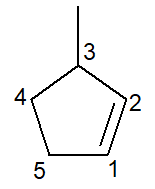
以下に3-メチル-シクロペンテンの構造を示します。
シクロアルケンの場合、常に1 番の炭素が二重結合を開始します。
前述したように、ブランチは可能な限り最小の番号を受け取る必要があるため、番号付けは反時計回りに続きます。
3-メチル。炭素番号 3 にメチル分岐があるためです。シクロペント-、炭素数 5 のシクロアルケンであるため。二重結合の存在を示す中置–en- (この場合、冗長であるため数字 1 は必要ありません) に炭化水素の接尾辞–oを加えます。
芳香族
芳香族炭化水素には、ベンゼンやナフタレンなどの独自の名前があり、以下に示します。
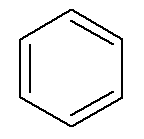
→ベンゼン
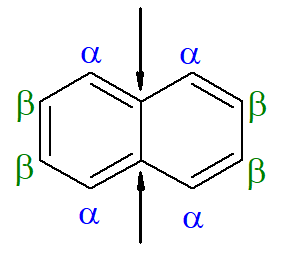
→ナフタレン
この場合、それら自身の名前はそれぞれのメインチェーンの名前でもあります。ベンゼンには一般にシクロアルカンやシクロアルケンと同じ命名規則と番号付け規則がありますが、ベンゼンに 2 つの分岐がある場合、これらの分岐の位置を指定するオルト、メタ、パラの接頭辞が付けられる可能性があります。
|
構造 |
正式名称 |
代替の公式命名法 |
|
|
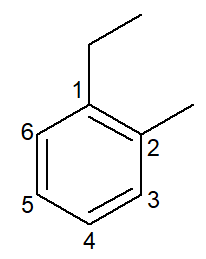
1-エチル-2-メチルベンゼン |
オルト-エチル-メチル-ベンゼン |
|
|
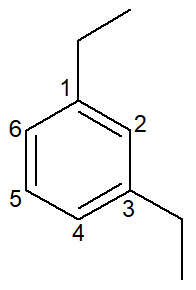
1,3-ジエチルベンゼン |
メタ-ジエチル-ベンゼン |
|
|
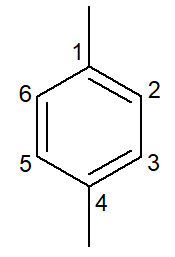
1,4-ジメチルベンゼン |
パラジメチルベンゼン |
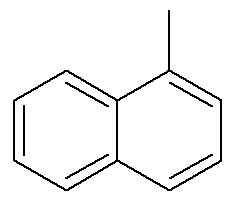
ナフタレンに関しては、前の画像はその位置の代替および伝統的な表示を示しています。矢印で示された芳香環の交点の炭素は参照炭素です。基準炭素の左または右に隣接する最初の炭素は、α炭素と呼ばれます。基準炭素の左または右に隣接する 2 番目の炭素は、β 炭素と呼ばれます。以下の構造はα-メチル-ナフタレンの構造です。
炭化水素はどこにありますか?
炭化水素は石油中に自然に存在し、分別蒸留、接触改質、分解などのプロセスでこの製品を精製することによって石油から抽出されます。
メタンなどの一部の軽い炭化水素は、地球の下層土に存在し、有機物の嫌気性分解から生じる天然ガスにも発生します。
特にメタンは、一部の動物の消化生成物であるだけでなく、埋め立て地やゴミ捨て場からの有機廃棄物の分解でも発生する可能性があります。さらに、湿地などの生態系でも自然に発生する可能性があります。
エテンガスは植物内で自然に発生し、果物の熟成に関与します。
炭化水素の働き
炭化水素には独特で多様な用途があります。それらの主な用途はエネルギーの観点からであり、天然ガス、液化石油ガス (LPG)、ガソリン、ディーゼルの場合のように、その大部分が燃料として使用されます。
これらは、発泡スチロールだけでなく、さまざまな容器、包装紙、プラスチックフィルムの製造に使用されるポリエチレン、ポリプロピレン、ポリスチレンなどの重要なポリマーを生成するため、プラスチック産業でも重要です。
炭化水素は、ヘキサンの場合のように溶媒として、またはベンゼンの場合のようにより複雑な化合物を合成するための基本的な化学構造としても使用できるため、化学産業でも重要です。