エンタルピー変化の計算は、化学反応が吸熱反応 (熱を吸収する反応) であるか発熱反応 (熱を放出する反応) であるかを判断するために熱化学で使用される重要な数学的ツールです。
化学プロセスのエンタルピー変化を計算するには、次の数式を使用する必要があります。
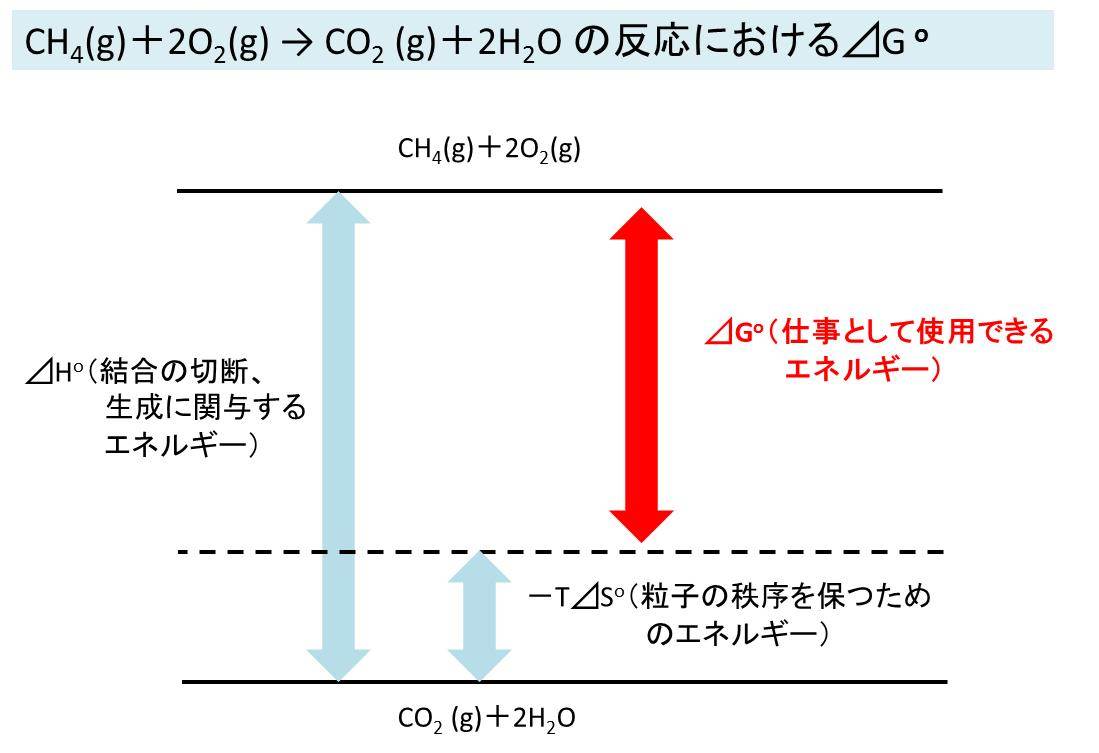
ΔH = H p – H r
ΔH はエンタルピー変化を表す頭字語です。
Hr は反応物のエンタルピーを表す頭字語です。
HP は生成物のエンタルピーを表す頭字語です。
エンタルピー変化の計算を実行できるのは、演習または問題で、反応における各参加者のエンタルピーが提供される場合のみです。このような場合、エンタルピーはゼロに等しいため、この演習では通常、単純な物質(1 つの化学元素だけで形成される) のエンタルピーは得られません。
複数の種類の単体物質を形成する化学元素が存在することを覚えておくことが重要です。これらは同素体と呼ばれます。このような場合、エンタルピーがゼロになるのは最も安定した同素体だけです。したがって、最も不安定な同素体が演習に現れた場合、そのエンタルピーの値にアクセスできるようになります。いくつかの化学元素の最も安定な同素体をご覧ください。
酸素: 最も安定な同素体は酸素ガス (O 2 ) です。
リン: 最も安定な同素体は白リン (P 4 ) です。
炭素: 最も安定な同素体はグラファイト (C gまたは Cグラファイト) です。
硫黄: 最も安定な同素体は斜方晶系硫黄 ( S8 ) です。
化学反応のエンタルピー変化を計算する手順
第 1 ステップ: 反応の化学方程式が平衡しているかどうかを分析します。そうでない場合は、バランスをとってください。
第 2 ステップ: 演習で得られたエンタルピー値を確認します。
第 3 ステップ:方程式に複数の反応物がある場合は、合計によって反応物のエンタルピーを計算します (反応物の係数にエンタルピー値を掛けることを忘れないでください)。注: 係数は、反応物の式の左側に書かれた値です。
4 番目のステップ: 方程式に複数の生成物がある場合は、合計を使用して生成物のエンタルピーを計算します (反応物の係数にそのエンタルピーの値を掛けることを忘れないでください)。
5 番目のステップ:ステップ 3 と 4 で見つかった値を数式に使用して、エンタルピーの変化を計算します。
エンタルピー変化の計算例
1 番目: スクロースが酸素と反応すると、燃焼反応が起こり、次の方程式が示されます。
C 12 H 22 O 11 + 12 O 2(g) → 12 CO 2(g) + 11 H 2 O (l)
この反応のエンタルピー変化の値はいくらですか?次のエンタルピー値を考慮してください。
CO 2 生成のΔH (g) = -94.1 kcal
H 2 O 生成の ΔH (l) = -68.3 kcal
C 12 H 22 O 11の生成ΔH = -531.5 kcal
演習によって提供されたデータは次のとおりです。
CO 2 生成のΔH (g) = -94.1 kcal
H 2 O 生成のΔH (l) = -68.3 kcal/mol
C 12 H 22 O 11の生成ΔH = -531.5 kcal/mol
C生成のΔH = 0 kcal/mol

注: 酸素ガスのエンタルピーは、酸素の最も安定な同素体であるため、ゼロの価値があるため、ステートメントには記載されていません。
第 1 ステップ:製品のエンタルピー値を計算します。
H p = 12.(CO 2 ) + 11.(H 2 O)
H p = 12.(-94.1) + 11.(-68.3)
Hp = – 1129.2 – 751.3
H p = -1880.5 カロリー

第 2ステップ:反応物のエンタルピー値を計算します。
Hr = 1.(C 12 H 22 O 11 ) + 12.(O 2 )
Hr = 1.(-531.5) + 12.0
時間 = – 531.5 カロリー
第 3ステップ:生成物と反応物のエンタルピーを次の式で使用します。
ΔH = H p – H r

ΔH = – 1880.5 – (-531.5)
ΔH = – 1349 カロリー
ΔH の結果が負であるため、反応は発熱的です。
2 番目:光合成反応 (光と熱の存在下) を表す化学式は次のとおりです。
6 CO 2 + 6 H 2 O → C 6 H 12 O 6 + 6 O 2
CO 2 (-94 kcal/mol)、H 2 O (-58 kcal/mol)、およびグルコース (-242 kcal/mol)の生成エンタルピーを考慮すると、プロセスのエンタルピーの変化の値はいくらになりますか? ?
第 1 ステップ:製品のエンタルピー値を計算します。
H p = 1.(C 6 H 12 O 6 ) + 6.(O 2 )
H p = 1.(-242) + 6.(0)
Hp = – 242 + 0
Hp = – 242 カロリー
第 2ステップ:反応物のエンタルピー値を計算します。

H r = 6.(CO 2 ) + 6.(H 2 O)
H r = 6.(-94) + 6.(-58)
H r = – 564 + (-348)
H r = – 564 – 348
時間 = – 912 カロリー
第 3ステップ:生成物と反応物のエンタルピーを次の式で使用します。

ΔH = H p – H r
ΔH = – 242 – (-912)
ΔH = – 242 + 912
ΔH = + 670 カロリー
注: ΔH の結果が正であるため、反応は吸熱反応です。
