状態図は、3 つの異なる領域を分離する 3 つの曲線を表すグラフと呼ばれます。x 軸の温度は摂氏 ( ° C) 単位、y 軸の圧力は通常水銀柱ミリメートル (mmHg) 単位です。

このグラフは、物質の物理的状態を変化させる、または物質を単一の物理的状態にするために必要な温度と圧力の条件を決定するために使用されます。
以下に、状態図で分析できる物理状態の変化を示します。
融合:固体状態から液体状態への遷移。
固化:液体から固体への変化。
気化: 液体から気体状態への変化。
凝縮:気体状態から液体への変化。
昇華:固体から気体状態への遷移。
再昇華: 気体状態から固体への転移。
1- 状態図の基本的な特性

すべての物質は、提案されたモデルと同様の状態図を示します。
したがって、この状態図には常に次のコンポーネントが含まれます。
エリア 1:物質が固体状態で見つかる温度と圧力の条件を決定するエリア。
エリア 2:液体状態の物質が見つかる温度と圧力の条件を決定するエリア。
エリア 3:物質が気体または蒸気の状態で発見される温度と圧力の条件を決定するエリア。
凝固曲線 (曲線 1):物質が溶融または凝固する温度と圧力の条件を決定する曲線。
沸騰曲線 (曲線 2):物質が凝縮または蒸発する温度と圧力の条件を決定する曲線。
昇華曲線 (曲線 3) : 物質が再昇華または昇華を受ける温度と圧力の条件を決定する曲線。
臨界点: 物質が気体状態でのみ存在する温度と圧力の条件を決定する点です。
三重点:すべての曲線が交わる状態図の領域であり、温度と圧力の固有の状態が決まります。この領域では、物質が 3 つの物理状態 (固体、液体、気体) にあることが同時にわかります。

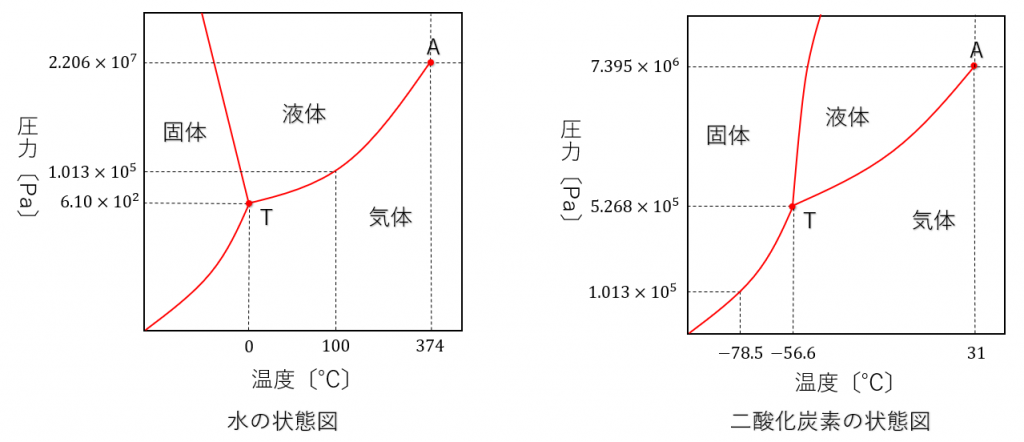
2- 特定の物質の状態図の解析例
二酸化炭素の状態図から次のことがわかります。
5.185 バールの圧力と –56.57 ℃では、この物質は固体、液体、気体の状態であり、同時に、
73.8 バール 31 および 31 ℃からは、CO 2 はもっぱら気体の状態で見つかります。
温度を-78.5 ℃に維持し、圧力を1.013バールから73.8バールまで変化させると、CO 2 はもっぱら固体状態で存在することがわかります。
CO 2の昇華または再昇華は、1.013 ~ 5.185 bar、および -78.5 ~ -56.57 ℃の任意の圧力および温度値で実行されます。
CO 2の溶融、固化、気化、凝縮は、5.185 ~ 73.8 bar、-56.57 ~ 31 ℃の圧力と温度で実行できます。
関連するビデオレッスン:



