「還元剤」と「酸化剤」のテキストで説明されているように、これら 2 つの用語は、それぞれ、酸化還元反応において、互いの還元と酸化を引き起こす物質を指します。これは、還元剤が、酸化または電子を失った化学種を含む物質であり、これらの電子を別の化学種に「供与」し、その化学種が還元(電子の獲得)を受けることを意味します。
医学では、還元剤として作用する物質は酸化されやすいため、抗酸化物質とも呼ばれます。このようにして、他の化学種を保護し、代わりに酸化します。
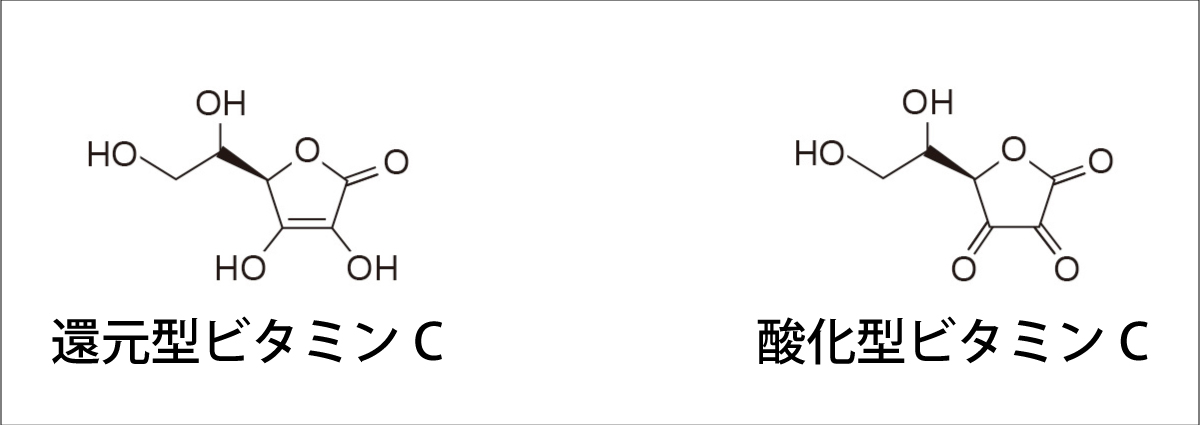
強力な還元剤はアスコルビン酸(またはL-アスコルビン酸) で、ビタミン Cとしてよく知られています。その式は、この記事の冒頭の図に示されています。
しかし、ビタミンCはどのようにして還元剤として作用するのでしょうか?
これがどのように起こるかを理解するには、次の状況を考えてください。リンゴ、バナナ、梨などの果物を切り、一定時間空気に触れさせておくと、色が濃くなることに気づいたことがありますか?しかし、これらを使ってフルーツサラダを作り、オレンジジュースを加えると、色が濃くなることはありません。なぜこのようなことが起こるのでしょうか?
酸化により黒くなったリンゴ
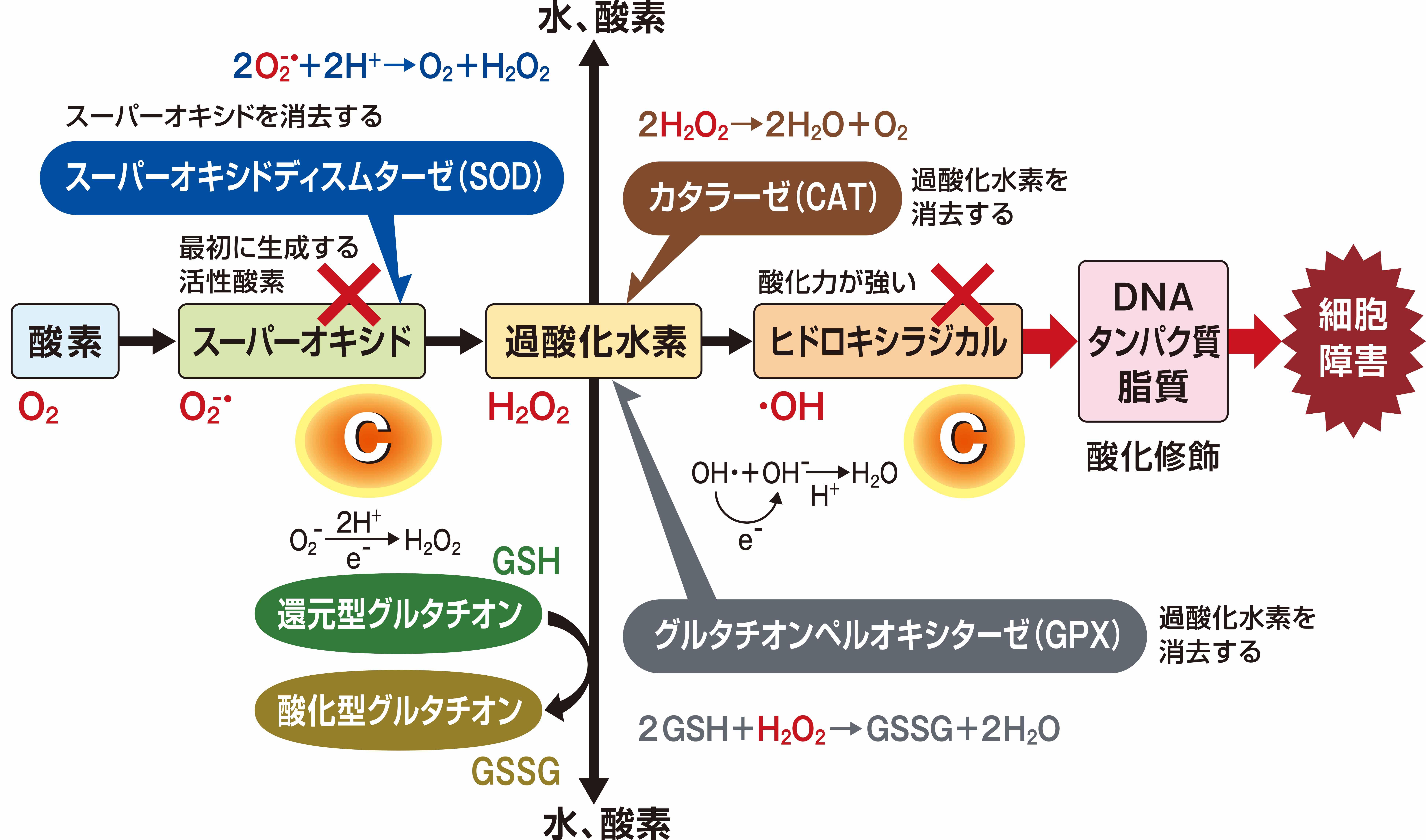
最初のケースでは、果物が空気中の酸素と接触して酸化しました。しかし、オレンジジュースを加えると、リンゴ、洋ナシ、バナナの成分の代わりにアスコルビン酸が酸化します。
これらはどのようなコンポーネントですか?
特定の果物、野菜、塊茎の褐変は、酵素ポリフェノールオキシダーゼ (PFO) と空気中の酸素の存在下で天然のフェノール化合物が酸化することによって起こります。この酸化では、重合反応を起こすことができるキノン分子が形成され、連続して結合し、その結果、黒く不溶性の色素分子であるメラニンが形成されます。
酵素ポリフェノールオキシダーゼと酸素の存在下でのフェノール化合物の酸化反応

世界中のトロピカルフルーツの損失の約50%はこのポリフェノールオキシダーゼ酵素の存在によるものと推定されているため、これは食品産業にとって問題となっています。したがって、ビタミン C はキノンをフェノール型に還元するため、果物の褐変を防ぐ代替手段として考えられます。
還元剤としてのアスコルビン酸の作用によるキノンのフェノール体への還元
ビタミンCは環境のpHを下げ、酸素と触媒の存在下で酸化するため、果物を酸化から守ることができます。アスコルビン酸の酸化型はデヒドロアスコルビン酸であり、pH 4 以下では非常に安定です。このように果物組織の pH が低下すると、褐変反応の速度が低下します。ポリフェノース酵素が作用するのに最適な pH は 6 ~ 7 ですが、pH 3 未満では酵素活性がありません。
アスコルビン酸の酸化
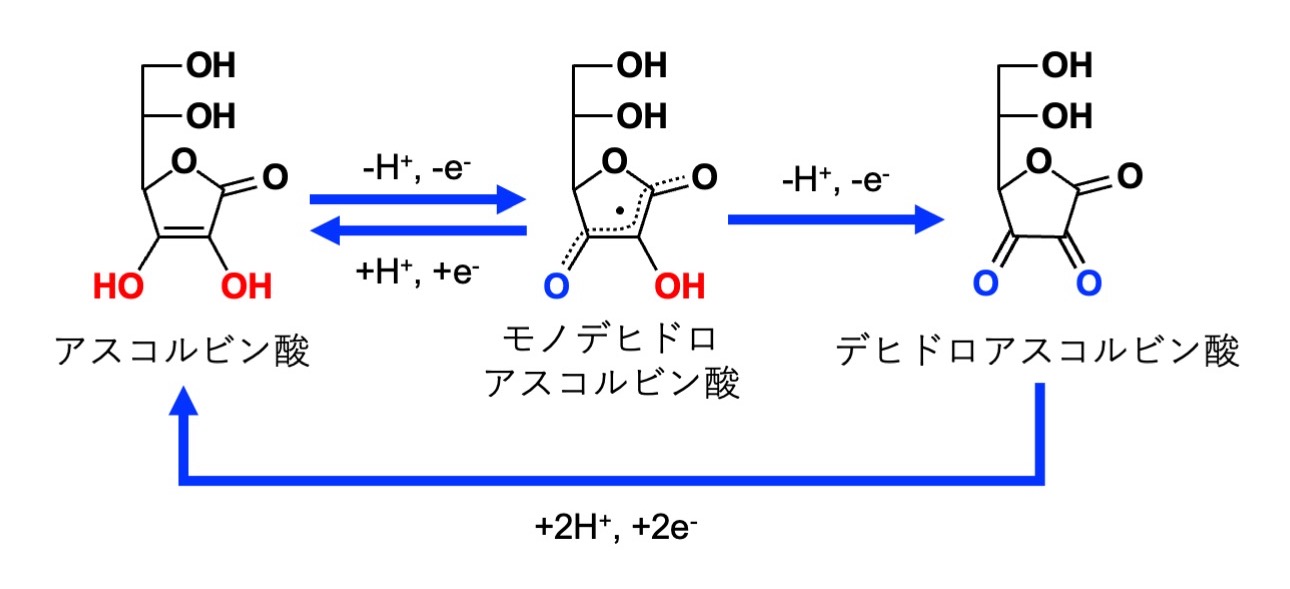
抗酸化物質としてのアスコルビン酸の役割は、食品業界で広く使用されています。ただし、この化合物は水溶性(水に溶ける)であり、脂溶性(脂肪に溶けない)ではないため、脂肪の多い食品には使用できません。




