火成電気分解は、直流発電機からの電流を純粋なイオン液体(水が存在せず、中央にイオンを含む溶融物質)に流し、電子の移動を伴う化学反応(酸化還元反応)を引き起こすプロセスです。 )。火成電気分解を使用すると、商業的に大きな関心のあるガスや金属などの単純な物質を得ることができます。
重要な火成電気分解は、食塩である塩化ナトリウム(NaCl) の電気分解です。これにより、自然界では単独では存在しない 2 つの化学生成物を得ることができます。これらの生成物は、金属ナトリウム (Na (s) ) と塩素ガス (Cl (g) ) です。
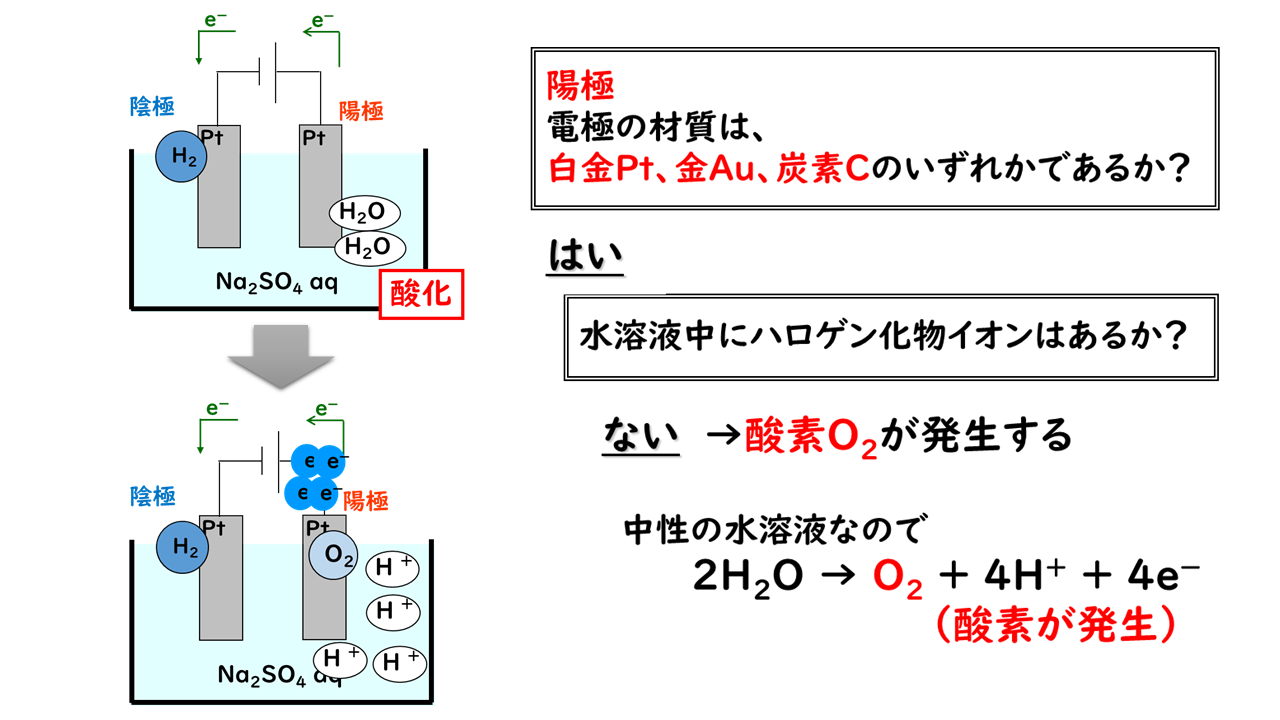
塩化ナトリウムの火成電気分解がどのように起こるかを見てみましょう。まず、塩化ナトリウムを800.4℃の温度で溶かします。この液相では、中央で Na +イオンと Cl –イオンが解離しています。
NaCl (s) → NaCl (l)
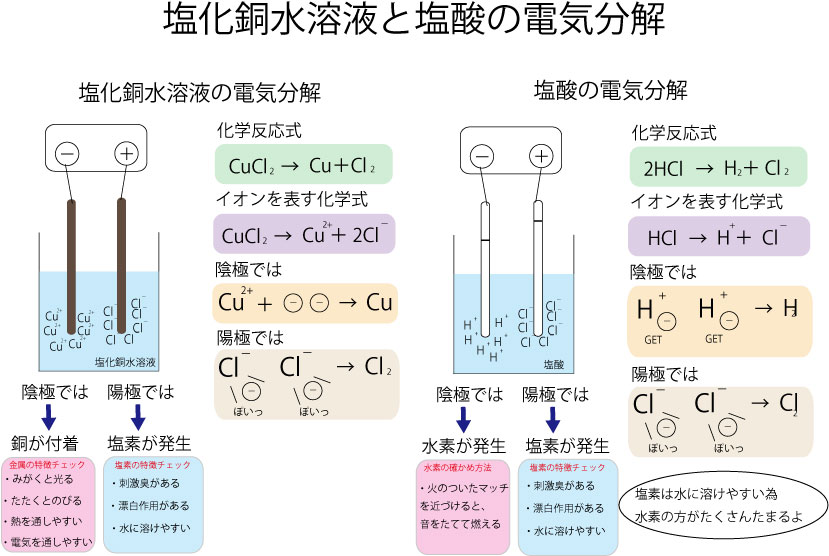
NaCl (l) → Na + (l) + Cl – (l)
この溶融塩は電解槽の中にあり、発電機に接続された2つの電極が電解槽に接続されています。負極はカソード、正極はアノードです。発電機の電源を入れると、次のような半反応が起こります。
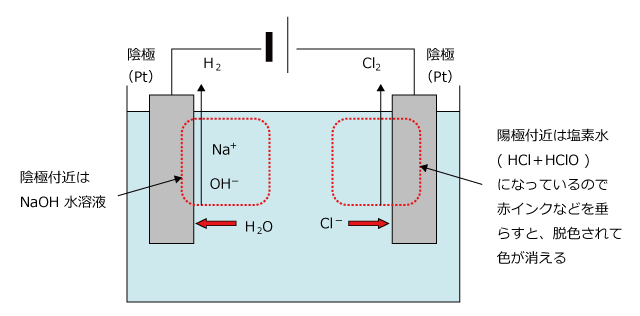
* 陰極: Na +イオンがこの陰極に引き寄せられます。この各イオンは電子を受け取り (還元を受け)、金属ナトリウムを形成します。
還元: Na + (l) + e – → Na (s)

※陽極: Cl –イオンが陽極に引き寄せられます。この各イオンは電子を供与し(酸化を受け)、塩素ガスを形成します。
酸化: 2Cl – (l) → 2e – + 1Cl 2(g)
塩化ナトリウム(食塩)の火成電気分解プロセスのスキーム
塩化ナトリウムの火成電気分解の全体的な反応は次のように与えられます。

カソード:Na + (l) + e – → Na (s)
アノード: 2Cl – (l) → 2e – + 1Cl 2(g)
全体的な反応: Na + (?) + 2Cl – (?) → Na (s) + 1Cl 2 (g)
形成された金属ナトリウムは塩化ナトリウムより密度が低いため、電極の上部に集められ、リザーバーに送られます。この金属は非常に反応性が高いため、これは空気の不在下で行われます。塩素は陽極で泡立つガスなので、システムに適合したガラス管を通して収集されます。

.jpg)