分子の極性は、溶解度や沸点を研究する際に非常に関係します。今日のテキストの焦点は、極性分子とそれを正しく識別する方法です。さあ行こう?
非極性分子とは、極(負と正の両方)を形成しない分子です。極性分子にはこれらの極があります。分子の極性の決定は、次のような要因に関連します。

1st) 物質を形成した化学結合の種類:
イオン結合:このタイプの結合には、2 つの原子 (電気陰性度が異なる) 間の電子の喪失と獲得が含まれます。また、1 つの原子が電子を失い、もう 1 つの原子が電子を獲得するため、正極が形成されます (損失)と負極(ゲイン)。したがって、イオン結合によって形成されるすべての物質は自動的に極性を持ちます。
共有結合 :異なる化学元素の 2 つの原子のみで形成される場合、 分子は電気陰性度が異なるため、自動的に極性になります。例: H 2と O 2 。原子の数が 2 つを超える場合は、原子と電子雲の数を考慮して、より慎重な評価が必要です。
2番目)分子内に存在する原子の数。
3番目)分子を構成する元素の種類。
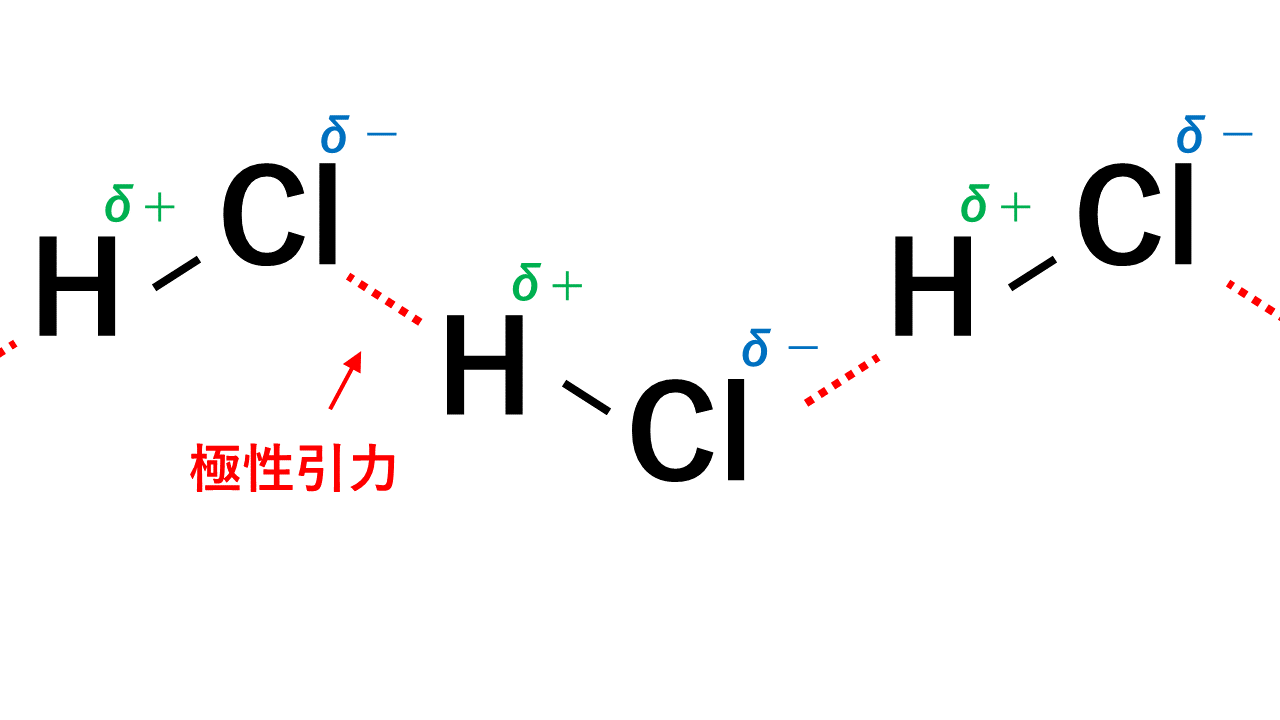
4th) 関与する原子間の電気陰性度の違い。
5番目) 分子を形成する中心原子内の電子雲*の量。
*電子雲とは、原子の価電子殻に存在する電子に直接関係する、結合に存在するかどうかに関係なく存在する電子のグループを指します。単結合、二重結合、または三重結合は電子雲であり、2 つの原子 (同じまたは異なる) の価電子殻からの電子が含まれています。いくつかの例を参照してください。
例 1: HCl
私たちは単純な結合を持っているので、それは雲 (2 つの共有電子) であり、1 つは水素からの電子、もう 1 つは 2 番目の塩素からのものです。
H-Cl
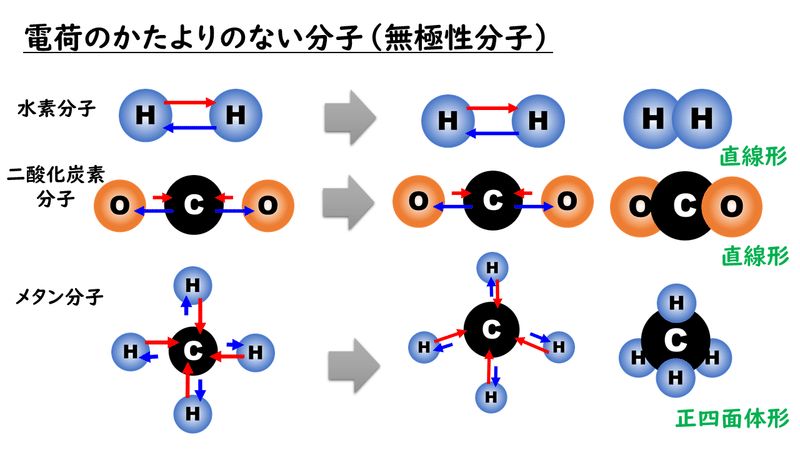
2番目の例: O 2
酸素原子間には二重結合があるため、酸素ごとに 2 つの電子、合計 4 つの電子が関与します。
○=○
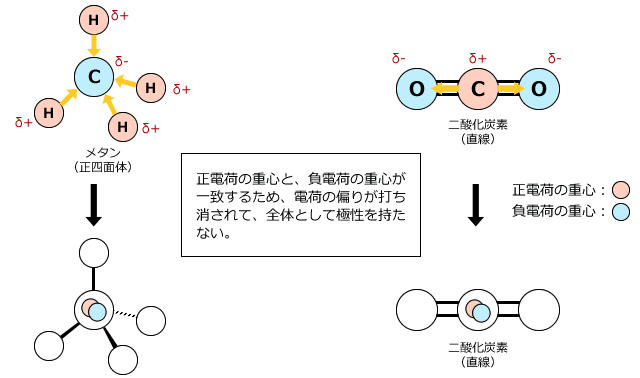
原子の非結合電子は、価電子殻に属しますが、別の原子との結合には関与しない電子です。周期表を通じて、価電子殻に存在する電子の数がわかり、それらが属する電子族を分析するだけで済みます。ファミリー番号は、シェル内の電子の数を示します。同じ例を使用すると、それらが持つ非結合電子の数を簡単に視覚化できます。
H-Cl
塩素は VIIA 族に属し、その価電子殻に 7 つの電子を持ち、結合には 1 つの電子のみを使用します。このため、6 つの非結合電子があり、3 つの電子雲が生じます。 IA族に属する水素は電子を1つだけ持ち、非結合性雲を持ちません。
○=○
酸素は VIA ファミリーに属し、その価電子殻に 6 つの電子を持ち、結合には 2 つだけを使用します。したがって、4 つの非結合電子があり、2 つの電子雲が生じます。

分子の極性を研究する場合、中心原子に存在する雲の数と、存在する類似の原子の数を分析します。雲の数が中心原子に結合している同じ原子の数と異なる場合、分子は常に極性になります。
クラウドの数 ≠ 等しいリガンドの数
いくつかの例を参照してください。
H2S

H-S-H
この物質には、2 つの等しい原子と 4 つの電子雲が存在します。残りの硫黄には 2 つの単純な結合 (2 つの雲) と 4 つの電子 (2 つの雲) があり、結合に関与するのは 6 つの電子のうち 2 つだけであるため、雲が 4 つあります。雲の数は分子内の同じ原子の数とは異なるため、それは極性分子です。
4 つのクラウド ≠ 2 つの等しいリガンド
CH3Cl

CL
|
H-C-H
|
H
この物質には 3 つの同一の原子と 4 つの電子雲があります。単純な結合が 4 つ (4 つ) あるため、雲が 4 つあります。炭素は族 IV に属するため、価電子が 4 つしかありません。雲の数は分子内の同じ原子の数とは異なるため、それは極性分子です。
4 つのクラウド ≠ 3 つの等しいリガンド
この主題に関連するビデオ レッスンをぜひご覧ください。
