無機機能の紹介というテキストでは、無機物質が酸、塩基、塩、酸化物の 4 つのグループまたは機能に分類されることが示されました。ただし、これらの無機機能を定義する概念は、水媒体中に放出されるイオンに従ってこれらの物質 (酸化物を除く) を分類するイオン解離のアレニウス理論に基づいています。
ただし、これらの無機物質の一部が水性環境にない場合、それらはこれらの機能のいずれにも当てはまらない、いくつかの異なる特性を示します。たとえば、硫化水素ガス (H 2 S) は水性媒体中で H +カチオンを放出し、硫化水素を形成します。しかし、それが元の気体状態にあり、まだイオンのない分子化合物である場合、その性質がそれが形成する酸とは異なることを考慮すると、どのグループに当てはまりますか?
このため、高校ではほとんど勉強されない 5 番目のグループが出現しました。これらは水素化物です。
水素化物は、2 種類の化学元素のみによって形成される無機化合物であり、そのうちの 1 つは必ず水素です。
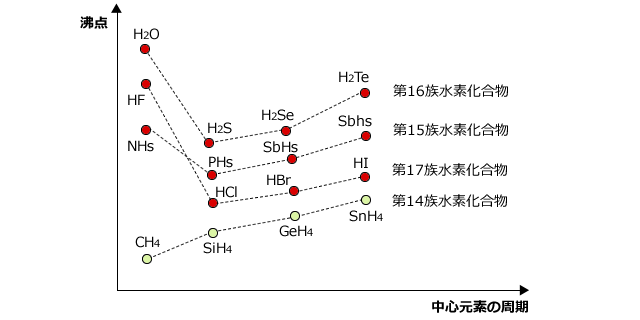
水素化物は、イオン性水素化物と分子性水素化物に分類できます。硫化水素ガスの場合、水素と非金属(半金属の場合もあります)との共有結合(または電子対を共有する分子結合)によって形成されるため、分子状水素化物です。

分子状水素化物の場合、水素は +1 の電荷を持ちます。他の例としては、 HF、CH 4 、H 2 O、および NH 3があります。
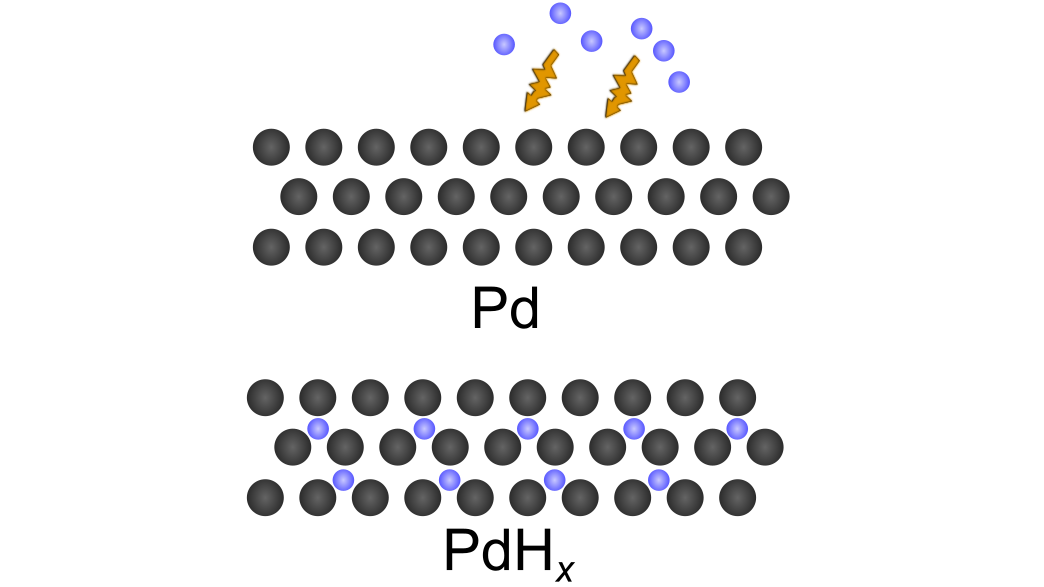
イオン性水素化物は、水素と金属の間にイオン結合が発生し、水素の電荷が -1 になると形成されます。これらの水素化物は、周囲条件で固体の結晶構造と高い融点を持って存在し、水と激しく反応して塩基性溶液を生成します。

一例は水素化リチウム (LiH) で、その構造はこの記事の冒頭で説明しました。この固体を水に加えると、形成された Li +カチオンが水中の OH –アニオンと結合し、塩基性の水酸化リチウム (LiOH) を形成します。
さらに、水素化物の H –アニオンは水の H +カチオンと反応し、水素ガス H 2を形成します。水素ガスの生成は、イオン性水素化物の主な用途でもあります。たとえば、救命ボートには水素化物が使われているため、ボートが水に落ちると水素ガスが発生してボートが膨張します。
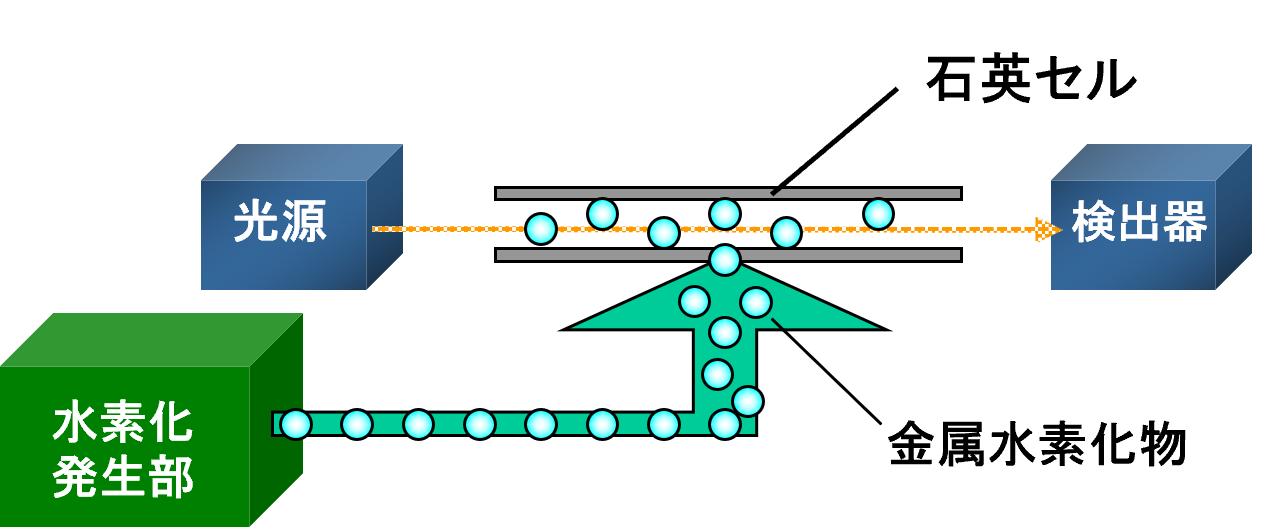
イオン性水素化物の他の例としては、NaH および CaH 2 があります。
関連するビデオレッスン:
