希釈溶液の計算を理解する前に、このプロセスの実行方法を知ることが重要です。溶液を希釈するには次の 2 つの方法があります。
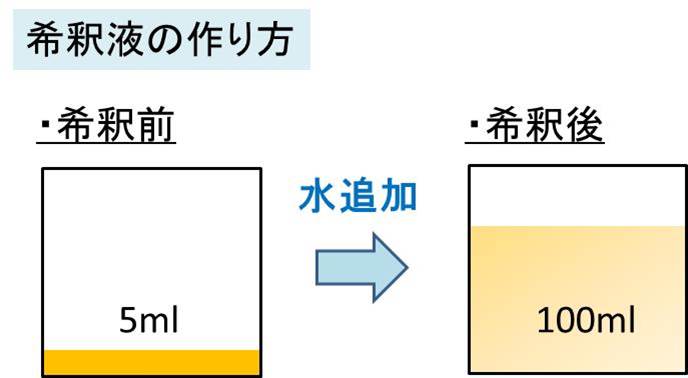
既製溶液への溶媒の添加(例えば、濃縮カシューナッツジュースに水を添加)。
注:完成した溶液に新しい量の溶媒が加えられると、溶質に比べてはるかに多くの量の溶媒が含まれるようになります。したがって、最初の溶液よりも濃度が低くなったり、より希釈された溶液になります。
完成した溶液からの溶媒の除去(たとえば、スープを長時間熱の上に放置して、水分の一部を蒸発させる場合)。

注:既製の溶液が蒸発によって溶媒の一部を失うと、溶質の量に近い量の溶媒が含まれます。したがって、最初の溶液よりも濃縮または薄められた溶液になります。
どちらの場合も、希釈計算を実行するために使用できる式は次のとおりです。
C i .V i = C f .V f
C i = 初期共通濃度。
V i = 初期ボリューム;
C f = 最終共通濃度;
V f = 最終ボリューム。
M i .V i = M f .V f
Mi = 初期モル濃度;
V i = 初期ボリューム;
M f = 最終モル濃度;
V f = 最終ボリューム。
最終体積は、初期体積と追加体積 (V a ) の合計、または初期体積から蒸発体積 (V e ) を引いたものです。

V f = V i + V aまたは V f = V i – V e
希釈計算例
ジュースを作るときは、溶液に水を加えます。したがって、希釈です
1 番目) 化学者は 1000 mg/L の濃度の溶液を持っており、その濃度が 5.0 mg/L に低下するまで 500 mL の溶液で希釈する必要がありました。望ましい値を得るには、最初の溶液にどのくらいの量の水を加えるべきでしょうか?
運動データ:
C i = 1000 mg/L
V i = 初期ボリューム
C f = 5 mg/L
V f = 500 mL
この問題を解決するには、次の式で初期体積を決定する必要があります。
C i .V i = C f .V f
1000.V i = 5,500
1000V i = 2500
V i = 2500
1000

V i = 2.5 mL
この演習では追加する水の量を求めるため、次を使用します。
V f = V i + V a
500 = 2.5 + Va
V a = 500 – 2.5
V a = 497.5 mLの水
2) 初期濃度が 20 g/L の KOH 水溶液から、7.5 g/L の溶液 150 mL を得ることが望ましい。この希釈に必要な初期溶液の量をリットル単位で求めます。
運動データ:
C i = 20 g/L
V i = 初期ボリューム
C f = 7.5 g/L
V f = 150 mL
この問題を解決するには、次の式で初期体積を決定する必要があります。
C i .V i = C f .V f
20.V i = 7.5,150
20V i = 1125
V i = 1125
20
Vi = 56.25 mL
この演習では体積をリットル単位で求めるので、求められた値を単純に 1,000 で割ります。
V i = 56.25
1000
V i = 0.05625 L
3) 200 mL の 2.0 mol/L NaOH 溶液から蒸発して濃度が 4.5 mol/L に上昇した水の体積をリットルで求めます。
運動データ:
Mi = 2 モル/L
V i = 200 mL
M f = 4.5 モル/L
V f = ?
この問題を解決するには、次の式で最終的な体積を決定する必要があります。
M i .V i = M f .V f
2,200 = 4.5.V f
400 = 4.5V f
V f = 400
4.5
V f = 88.88 mL
この演習では蒸発する水の量が必要となるため、次のものを使用します。
V f = V i – V e
88.88 = 200 – V e
V e = 200 – 88.88
V e = 111.12 mLの蒸発水
4) 0.20M 塩化ナトリウム溶液 25mL に水 75mL を加えると、モル濃度は何倍になりますか?
運動データ:
M i = 0.20M
V i = 25 mL
V a = 75 mL
M f = ?
V f = は、V i (25 mL) と Va (75 mL) の合計です。したがって、V f は100 mL になります。
この問題を解決するには、最終的なモル濃度を決定する必要があります。
M i .V i = M f .V f
0.2.25 = M f .100
5 = M f .100
M f = 5
100
M f = 0.05 mL
関連するビデオレッスン:

