分子の極性の問題は、この特性が物質の溶解度に直接関係しているため、化学において非常に重要です。
⇒極性物質は極性物質を溶解します。
⇒無極性物質は無極性物質を溶解します。
したがって、ある物質が別の物質を溶解するかどうかを知るためには、その分子の極性を評価することが非常に重要です。一般に、分子は極性または非極性の場合があります。
極性分子: 構造内にマイナス極とプラス極を持つ分子。
非極性分子:構造内に極を持たない分子。
この記事では、分子が非極性かどうかを判断する方法に焦点を当てます。研究を補完するために、記事「極性分子」を研究することが重要です (リンクにアクセスするだけです)。非極性分子の決定は、いくつかの重要なルールに基づいています。彼らです:
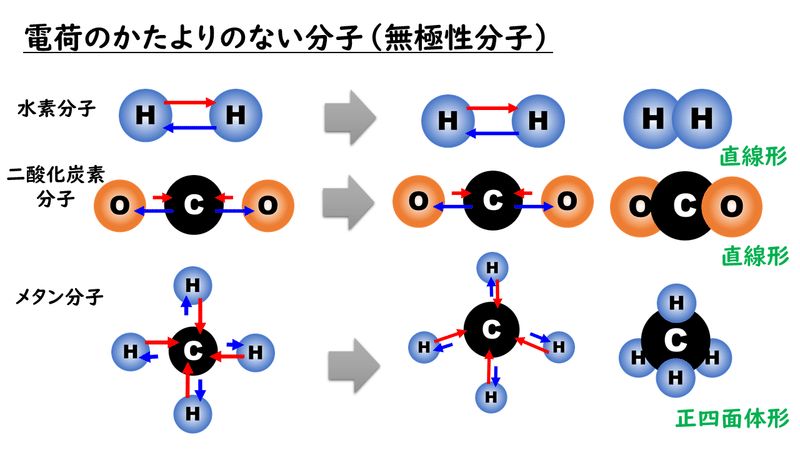
二原子分子
二原子分子とは、原子を 2 つだけ持つ分子です。分子が無極性になるのは、その構成に存在する 2 つの原子が等しい場合、つまり同じ化学元素に属する場合のみです。例: H 2 、Cl 2 、F 2 、Br 2 、O 2 、N 2など。
2つ以上の原子を持つ分子
2 つ以上の原子を持つ分子では、中心の原子の周囲に存在する電子雲の数を評価し、それに結合している同様の原子の数と比較する必要があります。雲は、結合や 2 つの原子間に存在する結合に関与していない電子のペアです。中心原子の周囲の電子雲の数が、それに結合している同じ原子の数と等しい場合、その分子は無極性であるとみなされます。いくつかの例を参照してください。
例 1: CO 2
この分子では、中心原子は炭素 (IVA ファミリーに属する) であり、最も多くの結合を形成します。この元素は価殻に 4 つの電子を持ち、4 つの結合を形成します。各酸素原子 (VIA ファミリーに属する) は、オクテットに到達するためにさらに 2 つの電子を必要とするため、2 つの二重結合を作成します。

炭素の 4 つの電子は 2 つの二重結合で使用されているため、中心原子には (結合の外側に) 自由電子はありません。中心原子の周りには電子雲が 2 つだけあり、それに結合している同一の原子が 2 つだけあります。このため、問題の分子は非極性です。
2 番目の例: BF3
この分子では、中心原子はホウ素であり、最も多くの結合を形成するため、ファミリー IIIA に属します。この元素は価殻に 3 つの電子を持ち、3 つの結合を形成します。各フッ素原子 (VIIA 族に属する) は、オクテットに到達するためにさらに 1 つの電子を必要とするため、単結合を形成します。
ホウ素の 3 つの電子は 3 つの単結合で使用されているため、中心原子には自由電子 (結合の外側) はありません。中心原子の周囲には電子雲が 3 つだけあり、それに付着している同一の原子が 3 つあるため、問題の分子は無極性になります。
3例目: CH4
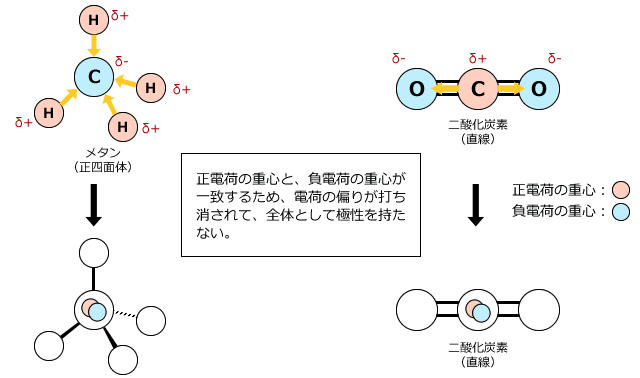
中心原子は炭素であり、IVA 族に属しており、したがって価電子殻に 4 つの電子を持ち、4 つの結合を形成します。各水素原子 (ファミリー IA) は、オクテットに到達するのに電子が 1 つだけ必要なだけであるため、単結合を形成します (ヘリウムと同じ)。
炭素の 4 つの電子は 4 つの単結合で使用されているため、中心原子には自由電子 (結合の外側) はありません。中心原子の周囲には電子雲が 4 つだけあり、それに結合している同一の原子が 4 つあるため、問題の分子は無極性になります。
4番目の例: SO3
分子内のすべての原子は VIA ファミリーに属し、価電子殻に 6 つの電子を持ち、オクテットに到達するにはさらに 2 つの電子を必要とします。硫黄は最小の元素で最も電気陰性度が低いため、中心原子になります。したがって、硫黄と酸素の間には二重結合があり、硫黄と他の酸素原子の間には他の 2 つの配位結合が存在します。それぞれの与格において、硫黄はその価電子殻から 2 つの電子を使用します。
構造配置を分析すると、中心の原子に3 つの電子雲とそれに結合した3 つの同一の原子があることがわかります。このため、この分子は無極性です。




